Clear Sky Science · tr
Deubiquitination ile ilişkili genler, kolorektal kanserin immün alt tiplerini tanımlar ve prognoz ile immünoterapiyle ilişkili imzalara bağlıdır
Bu çalışma insanların yaşamı için neden önem taşıyor
Kolorektal kanser, dünya genelinde en yaygın ve ölümcül kanserlerden biridir; ancak mikroskop altında benzer görünen tümörlere sahip kişiler, modern tedaviler—özellikle immünoterapi—konusunda çok farklı sonuçlar ve yanıtlar gösterebilir. Bu çalışma yeni bir soru soruyor: tümör hücrelerinin protein “yeniden kullanımı”nı nasıl yönettiklerine ve bunun vücudun bağışıklık savunmalarıyla nasıl bağlantılı olduğuna bakarak kolorektal kanserleri daha net gruplara ayırabilir miyiz? Bu sorunun yanıtı gelecekte doktorların prognozu daha iyi tahmin etmesine ve daha akıllı tedavi kombinasyonları tasarlamasına yardımcı olabilir.
Protein temizliği ve kanser davranışı
Her hücrenin içinde, yıpranmış veya hasarlı proteinler etiketlenir ve birikmemeleri için geri dönüştürülür. Bu sistemin bir kolu olan deubiquitination, bu etiketleri çıkarır ve hangi proteinlerin yok edileceği hangilerin korunacağı konusunda ince ayar yapılmasına yardımcı olur. Yazarlar, bağırsak tümörleri ve sağlıklı dokuya ait geniş halka açık veri setlerini topladı ve bu protein temizliği sistemi ile hasta sağkalımı arasında bağlantı gösteren binlerce geni taradı. Listeyi hücre bölünmesi kontrolü, DNA hasar onarımı ve hücreleri çevreleyen matriksin yapısı ile güçlü biçimde ilişkili 17 ana gene daralttılar. Bu genler kolorektal kanserleri gruplayan yeni yaklaşımın omurgasını oluşturdu.
İki ana tümör tipi ortaya çıkıyor
17 genin etkinlik desenlerini kullanarak araştırmacılar tümörleri iki ana alt tipe ayırdı. Bir gruptaki kişiler genellikle daha uzun yaşadı ve daha erken evrede hastalığa sahipti. Diğer grubun prognozu daha olumsuzdu. Ekip her alt tipte hangi genlerin daha fazla veya daha az etkin olduğuna daha geniş ölçekte baktığında, kötü sonuçlu grubun hızlı hücre çoğalması, hasarlı DNA’ya karşı stres yanıtları ve tümörü çevreleyen doku iskeletinin yoğun yeniden düzenlenmesi gibi güçlü sinyaller gösterdiğini gördü. Buna karşın iyi sonuçlu grup bu agresif yeniden düzenlemeden daha az etkilenmiş ve daha dengeli bir hücre büyümesi ve onarım deseni sergilemişti.
Tümörün mahallesi ve bağışıklık yanıtı
Kanser izole olarak büyümez; bağışıklık hücreleri, destek hücreleri ve yara benzeri dokudan oluşan bir mahalle içinde yaşar. Çalışma, her tümörde hangi bağışıklık hücrelerinin bulunduğunu tahmin etmek için hesaplamalı araçlar kullandı. İki alt tip çarpıcı şekilde farklı immün manzaralar gösterdi. Kötü sonuçlu alt tip yoğun kollajen ve fibröz doku bakımından zengindi; bu, kanserle savaşan T hücrelerinin erişimini engelleyebilen fiziksel ve kimyasal bir bariyer oluşturuyordu. Ayrıca immün baskı sinyalleri ve immünoterapiye direnç öngören ölçümlerde daha yüksek skorlar taşıyordu. İyi sonuçlu alt tipte ise matriks birikimi daha zayıftı, katil T hücreleri ve yardımcı T hücreleri gibi daha elverişli immün hücre karışımları vardı ve immün temelli tedavilere daha duyarlı olabileceğini gösteren skorlar mevcuttu.
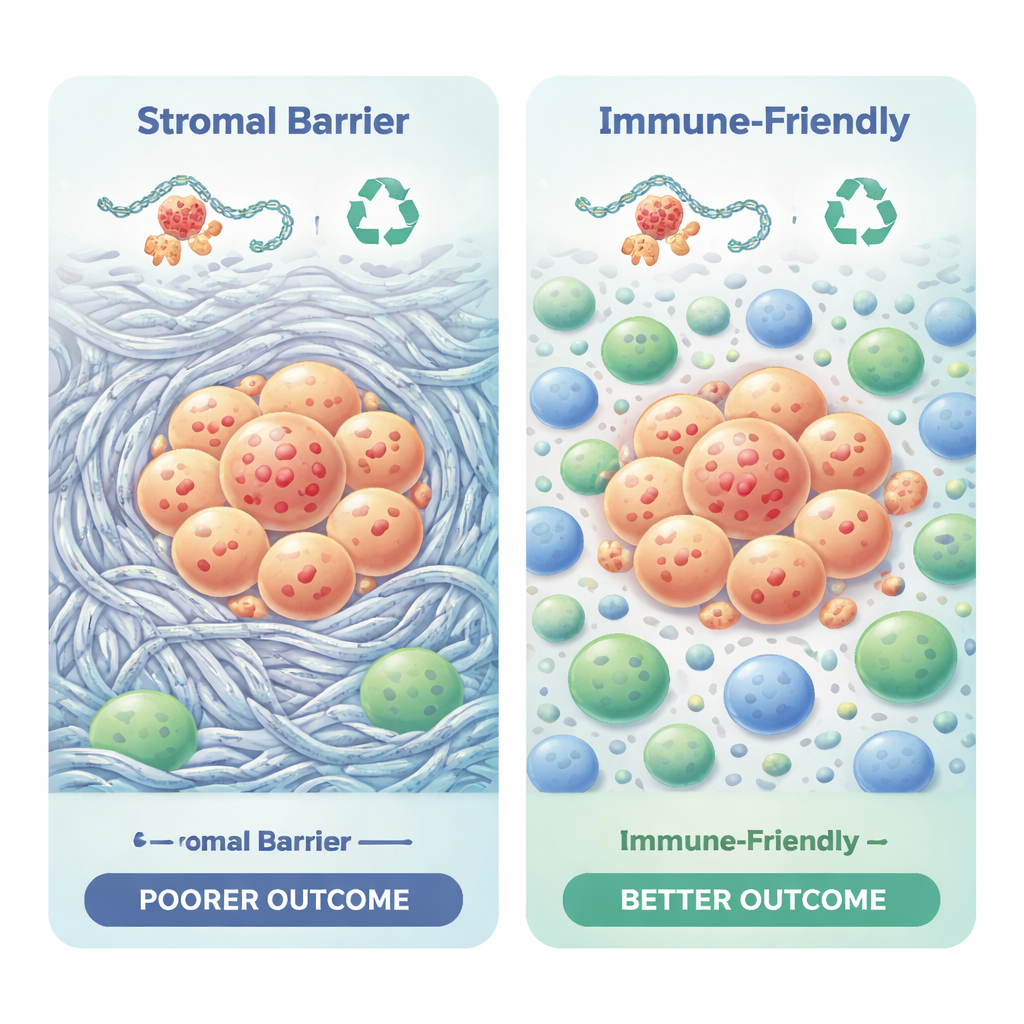
Uyarı işaretleri olarak ana yapısal genler
Geniş desenlerden pratik belirteçlere geçmek için yazarlar etkileşen protein ağları kurdu ve merkezi “düğüm” genleri aradı. Tümörü çevreleyen iskeleti inşa etme ve yeniden düzenlemeyle büyük ölçüde ilişkili dokuz gen belirlediler; bunlar arasında birkaç kollajen ile fibronectin ve periostin gibi moleküller yer aldı. Özellikle BGN, FN1 ve POSTN’in yüksek etkinliği, iki bağımsız hasta grubunda tutarlı şekilde daha kötü sağkalım ile ilişkilendirildi. Bu düğüm genleri mekanik sertlik, kimyasal sinyalizasyon ve immün hücre çekilmesinin kesişim noktasında yer alır; bu da onları gelecekte riski tahmin etmeye veya tedavi seçimlerini yönlendirmeye yardımcı olabilecek testler için cazip adaylar yapar.
İleriye dönük anlamı
Bu çalışma henüz hasta tedavisini değiştirmiyor; çünkü yeni klinik denemeler yerine mevcut verilerin bilgisayar analizine dayanıyor. Yine de, uzman olmayanlar için net bir büyük resim çıkarımı sunuyor: bir kolorektal tümörün protein yenilemesini nasıl yönettiği ve yerel ortamını nasıl yeniden şekillendirdiği, bağışıklık sisteminin ona erişip saldırıp saldıramayacağını belirlemeye yardımcı oluyor gibi görünüyor. Protein kontrolünün ağır biçimde bozulduğu ve kalın, fibröz bir kabuğa sahip tümörler immün hücreleri geri püskürtme eğiliminde ve daha kötü sonuçlarla ilişkili; daha az skarlaşma ve immün hücreler için daha açık erişim sağlayan tümörler ise daha iyi seyrediyor. Gelecekte DNA onarımı veya fibröz matriksi hedefleyen ilaçların immünoterapi ile birleştirilmesi, bu çalışmada tanımlanan yüksek riskli grup için özellikle faydalı olabilir.
Atıf: Xu, Y., Mo, Z., Jiang, Q. et al. Deubiquitination-related genes define immune subtypes of colorectal cancer and are associated with prognosis and immunotherapy-related signatures. Sci Rep 16, 4862 (2026). https://doi.org/10.1038/s41598-026-35271-5
Anahtar kelimeler: kolorektal kanser, tümör mikroçevresi, immün alt tipler, protein yıkımı, immünoterapi