Clear Sky Science · tr
Çinko dengesinin bozulması, normal ve tümör hücrelerinde histon asetilasyon düzeylerini azaltır
Yararlı Bir Metal Zararlı Hale Geldiğinde
Çinko, çoklu vitaminlerde bağışıklık sistemimizi ve yara iyileşmesini destekleyen besin olarak en çok bilinir. Ancak hücrelerimizin içinde çinko çok dar bir “tam yerinde” aralıkta tutulmalıdır. Bu çalışma, hücre içi çinko düzeyleri çok yükseldiğinde, DNA paketlenmesini sıkılaştırarak önemli genleri sessizce kapatabileceğini ve hatta hücreleri otofaji adı verilen bir kendi‑temizleme sürecine yönlendirebileceğini gösteriyor. Çinko takviyeleri, kepek karşıtı bileşenler ve deneysel kanser ilaçlarının çinko düzeylerini değiştirebilmesi nedeniyle, bu gizli kontrol mekanizmasını anlamak hem günlük sağlık hem de gelecekteki terapiler için önem taşır.
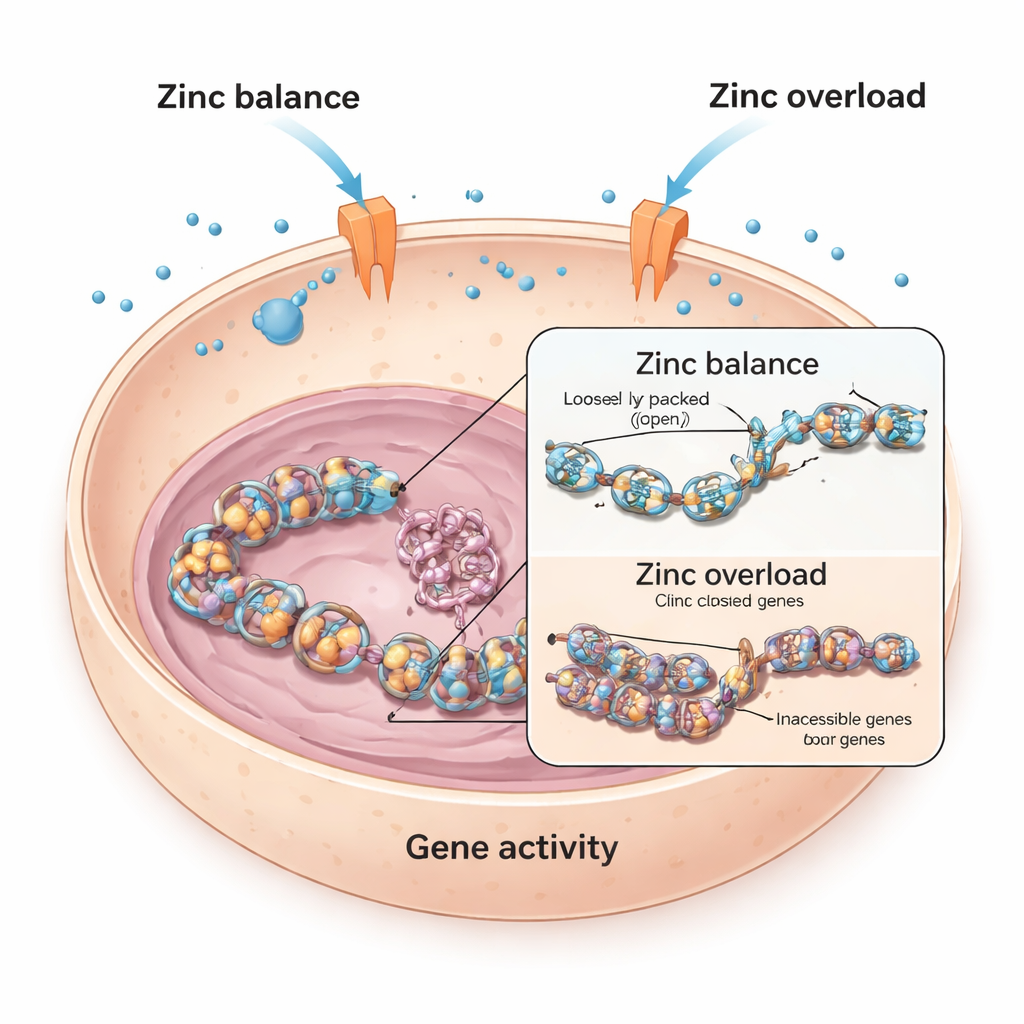
Yaşayan Hücrelerde Çinkonun Dengelenmesi
Her hücre, binlerce proteinin görevlerini yapmasına yardımcı olan çinkoya güvenir. Hem eksiklikten hem de fazlalıktan kaçınmak için hücreler, çinkoyu içeri ve dışarı taşımak üzere zarlarında özel “kapılar” olan çinko taşıyıcılarını kullanır. Araştırmacılar, fare ve insan kalp kası hücrelerinden başlayarak, bu hücrelere ekstra çinko verildiğinde ne olduğunu sordular. Fare kalp hücrelerinde yüksek çinko düzeylerinin, kalp gelişimi ve işlevinde rol oynayan önemli bir gen olan Bmp4'ün aktivitesini güçlü biçimde azalttığını buldular. Buna karşılık, insan kalp hücreleri çok daha az etkilendi; bu da farklı hücrelerin çinko aşırı yüklenmesine karşı farklı savunma yolları kullandığını düşündürüyor.
Çinko DNA Paketlenmesini Nasıl Sıkılaştırır
Bmp4 gibi genlerin nasıl susturulduğunu ortaya çıkarmak için ekip, DNA'nın sarıldığı makara benzeri proteinler olan histonlara baktı. Histonlara asetil grupları gibi küçük kimyasal etiketler eklendiğinde DNA gevşer ve okunması kolaylaşır; bu etiketler çıkarıldığında DNA daha sıkı paketlenir ve genleri açmak zorlaşır. Çalışma, fare kalp hücrelerinde fazla çinkonun belirli bir bölgede (H3K9 olarak bilinen yerde) histon asetilasyonunda düşüşe yol açtığını ve bunun Bmp4 aktivitesindeki düşüşle yakından izlendiğini gösterdi. Histon de‑asetilaz enzimlerini engelleyen ilaçlar çinkonun etkisini geri çevirebiliyor ve Bmp4'ü eski haline getirebiliyordu; bu da çinkonun bu kimyasal etiketleme dengesini kaydırdığını düşündürüyor.
Önemli Olan Hücre İçi, Sadece Dış Ortam Değil
Belirleyici adımın, çevre sıvısındaki çinko değil hücrenin sulu sitoplazmasındaki serbest çinko olduğu ortaya çıktı. Serbest çinkoyla varlığında ışıldayan bir floresan prob kullanan araştırmacılar, tedavi sonrası fare kalp hücrelerinde içerde bir çinko patlaması gördüler. Çinkoyu doğrudan hücre içine zorlamak için bir çinko taşıyıcı molekül kullandıklarında, dış ortamda çok daha düşük çinko olsa bile aynı histon asetilasyon ve gen aktivitesi düşüşünü gözlemlediler. Buna karşılık insan kalp hücrelerinde, hücre zarındaki taşıyıcılar hızla ayarlandı: bazı çinko alıcıları kapanırken ihracatçılar arttı, bu da iç çinkoda büyük bir yükselmeyi önleyip histon asetilasyonunu korudu. Fare kalp hücreleri daha “yanlış bağlanmış” bir taşıyıcı tepkisi gösterdi ve daha fazla çinkonun hücre içine akmasına izin vererek gen kontrolünü bozdu.
Gen Kontrolünden Kendi‑Temizlemeye: Normal ve Tümör Hücrelerinde
Araştırmacılar sonra bu çinko kaynaklı DNA paketlenmesi sıkılaşmasının yalnızca kalp hücrelerine özgü olup olmadığını sordular. Bir dizi normal insan hücresi ve mide, uterus ve over kaynaklı kanser hücre hatlarını test ettiler. Çinkonun bir taşıyıcı yardımıyla hücre içinde birikmesine izin verildiğinde, bu hücrelerin neredeyse tümü histon asetilasyonunda belirgin bir düşüş gösterdi. Bazı tümör hücrelerinde, örneğin mide kanseri hücrelerinde, bunun özellikle düşük çinko dozlarında bile gerçekleşmesi, bazı kanserlerin çinko dengesizliğine olağanüstü duyarlı olabileceğini düşündürüyor. Ekip ayrıca asetilasyon düşüşünü otofaji ile ilişkilendirdi; otofaji hücrelerin yıpranmış parçaları geri dönüştürdüğü bir süreçtir. Orta düzeyde iç çinko artışları otofajiyi artırırken, çok yüksek çinko seviyeleri sonunda otofajiyi zayıflattı; bu da çinkonun bu kendi‑temizleme yolunu hassas bir şekilde ayarlamak için dar bir pencereye sahip olabileceğini gösteriyor.
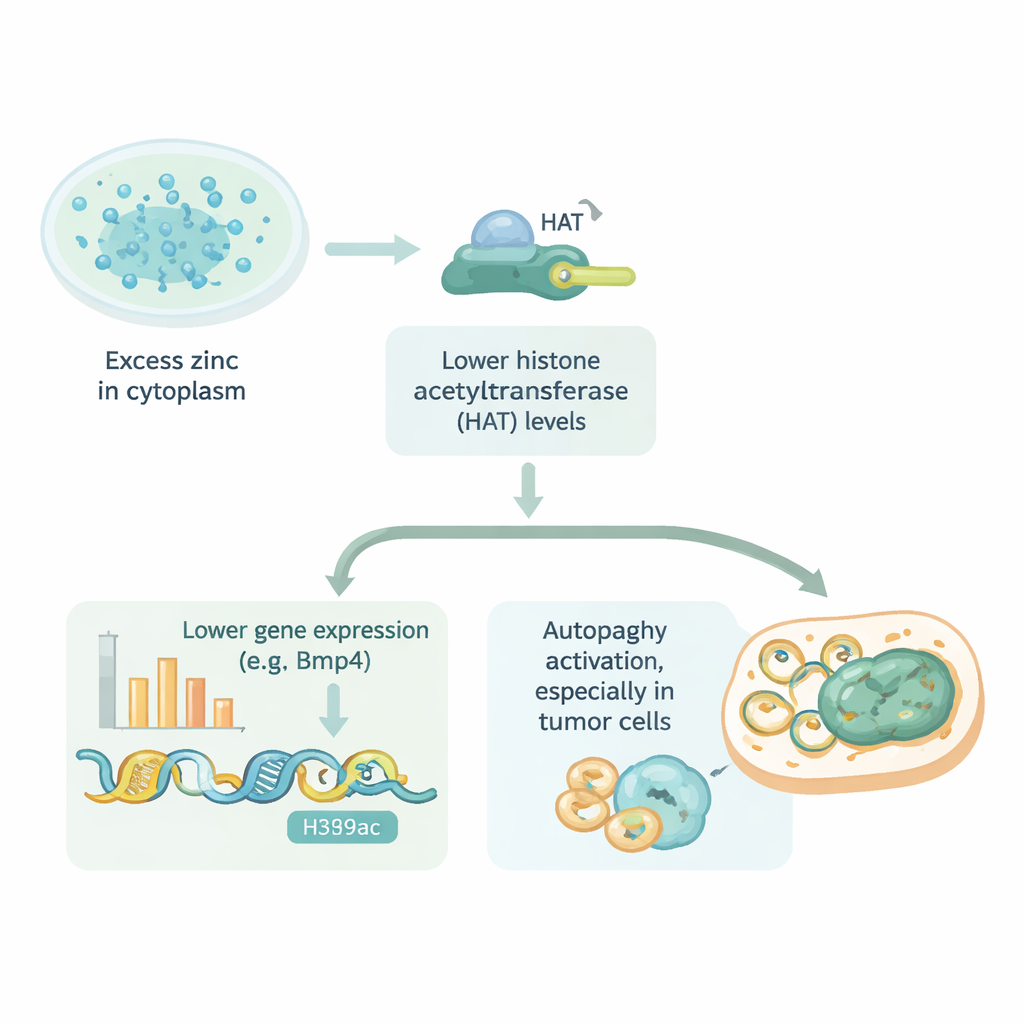
Sağlık ve Tedavi Açısından Ne Anlama Geliyor
Basitçe söylemek gerekirse, bu çalışma hücre içinde çok fazla çinkonun DNA'ya erişimi zorlaştırarak genleri kısabileceğini ve aynı yolun hücrelerin kendi temizliğini ne kadar aktif yaptığını da etkileyebileceğini ortaya koyuyor. Etki yalnızca kalp hücreleriyle sınırlı değil; farklı normal ve kanser hücrelerinde görülüyor, ancak bazıları çinko aşırı yüklenmesine karşı diğerlerinden daha iyi savunma yapabiliyor. Bu bulgular, hücre zarındaki küçük çinko taşıyıcı “kapılarının” umut verici ilaç hedefleri olabileceğini; ya sağlıklı dokuları çinko‑ilişkili hasardan korumak ya da savunmasız tümör hücrelerini ölüme itmek için kullanılabileceğini öne sürüyor. Bulgular hücre kültürü deneylerinden gelse de, günlük bir besinin hassas dengesi bozulduğunda gen aktivitesi ve hastalık üzerinde nasıl etkili olabileceğine dair yeni bir bakış açısı sağlıyor.
Atıf: Xu, S., Hu, Y., Tang, C. et al. Disruption of zinc homeostasis reduces histone acetylation levels in normal and tumor cells. Sci Rep 16, 4983 (2026). https://doi.org/10.1038/s41598-026-35270-6
Anahtar kelimeler: çinko homeostazı, gen regülasyonu, histon asetilasyonu, otofaji, kanser hücreleri