Clear Sky Science · tr
Metabolik yeniden programlanma, farklılaşan kardiyomiyositlerde oksidatif stres direncini artırır
Kalp hücrelerinin oksijenle mücadelesinin önemi
Kalbin her atışı, kardiyomiyosit adı verilen özelleşmiş kas hücrelerine dayanır. Gelişim sırasında bu hücreler dramatik bir yaşam değişimi yaşar: anne karnındaki düşük oksijen, şeker odaklı ortamdan doğum sonrası oksijen açısından zengin bir dünyaya geçerler. Oksijen hayati önemdedir, ancak aynı zamanda DNA’yı zarar verebilecek ve hücreleri öldürebilecek zararlı yan ürünler de üretir. Bu çalışma, olgunlaşan kalp hücrelerinin daha fazla oksijenle başa çıkmak, daha fazla enerji üretmek ve yine de oksidatif hasara karşı kendilerini korumak için metabolizmalarını nasıl yeniden düzenlediklerini inceliyor—bu, gelecekte kalp hastalıkları ve rejenerasyon için yeni yaklaşımlar geliştirmeye ışık tutabilir.
Basit inşa edicilerden dayanıklı enerji atletlerine
Olgunlaşmamış kalp hücreleri, kardiyomiyoblastlar, küçük ve bölünen hücrelerdir ve enerji için ağırlıklı olarak glukoz parçalanmasına güvenirler. Olgun kardiyomiyositlere farklılaştıkça bölünmeyi bırakır, daha büyük hale gelir ve genellikle güçlü kasılmaya daha uygun çok çekirdekli, uzamış hücrelere dönüşürler. Araştırmacılar, yüksek çözünürlüklü mikroskopi kullanarak bu dönüşümü laboratuvar hücre modelinde on gün boyunca izlediler. Hücre proliferasyon belirteçleri azaldı, hücreler uzadı ve fibröz, kalbe benzer yapılar oluşturacak şekilde yeniden düzenlendi; bu da daha yetişkin benzeri, kasılabilir bir duruma geçtiklerini doğruladı. 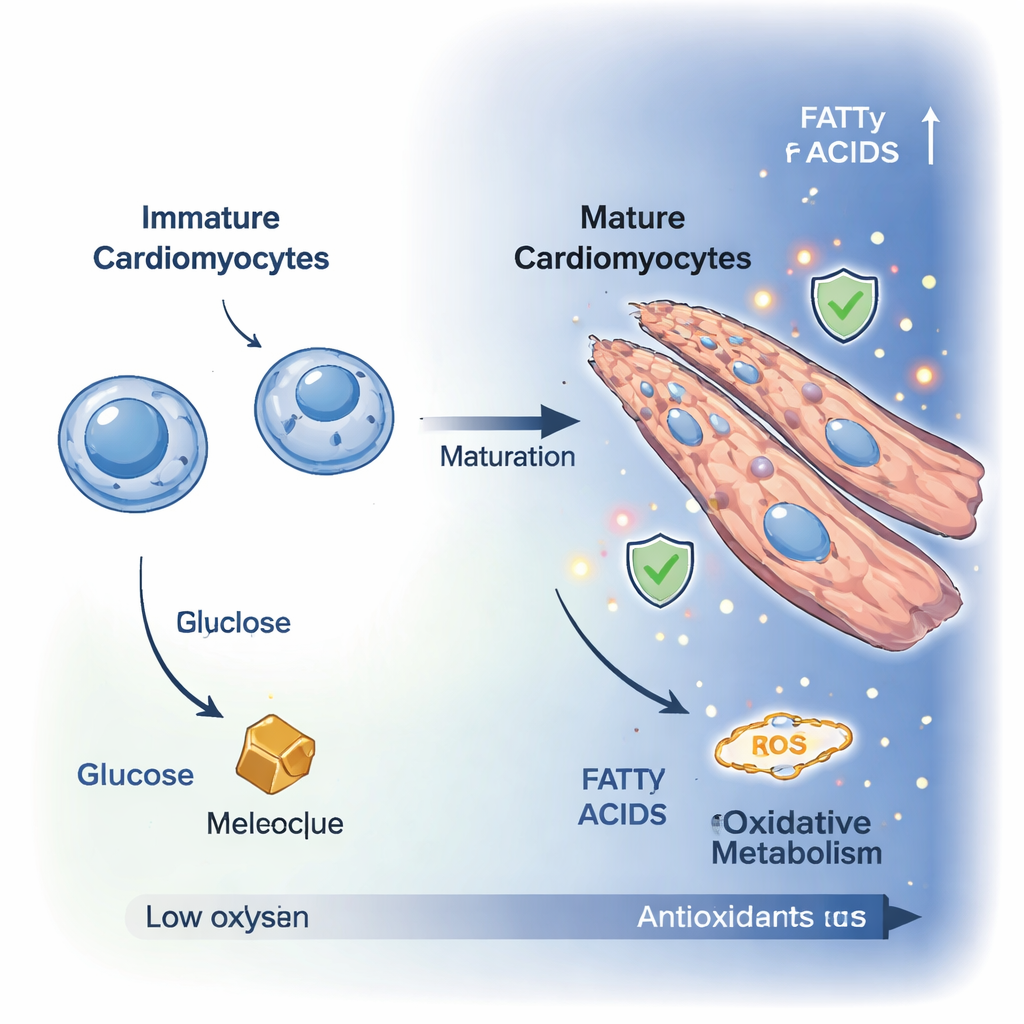
Yakıt kaynaklarını değiştirmek ve yeni enerji yolları kurmak
İşin perde arkasında neler olduğunu anlamak için ekip hücre içindeki yüzlerce küçük molekülü ölçtü ve enerji kullanımını gerçek zamanlı izlemek için hücrenin doğal floresansını gelişmiş görüntüleme ile takip etti. Bu tekniklerin bir arada kullanımı glikolitik, yani hücrelerin ağırlıklı olarak glukozu yaktığı bir durumdan mitokondriyal solunumun hakim olduğu oksidatif bir duruma net bir geçiş olduğunu gösterdi. Glukoz ve fruktoz seviyeleri düştü, sitrik asit, malik asit ve oksoglutarat gibi trikarbonik asit (TCA) döngüsü ara ürünleri arttı. Yol analizleri, malat–aspartat taşıyıcısı ve amino asit yıkımı gibi yakıtın mitokondrilere beslenmesini sağlayan yolların daha güçlü şekilde aktif olduğunu ortaya koydu; bu, olgun kardiyomiyositlerin yakıt seçeneklerini genişlettiğini ve enerjiyi güç istasyonlarına daha verimli yönlendirdiğini gösteriyor.
Daha fazla oksijenle yaşamak—ve daha fazla stres
Yakıtı mitokondrilerde daha verimli yakmak bir bedelle gelir: reaktif oksijen türlerinin (ROS) daha yüksek üretimi; bunlar lipitlere, proteinlere ve DNA’ya zarar verebilen kimyasal olarak agresif moleküllerdir. Araştırmacılar, kardiyomiyositler olgunlaştıkça mitokondrilerinin daha büyük ve daha uzamış hale geldiğini ve oksidatif stres belirteçlerinin arttığını buldu. Floresans tabanlı görüntüleme, oksitlenmiş lipitlerin bir işareti olan daha fazla lipofuscin-benzeri granül ortaya koydu ve nükleer bir prob farklılaşmış hücrelerde daha yüksek ROS seviyelerini gösterdi. Metabolomik veriler, glutatyon metabolizmasında değişikliklere işaret etti; glutatyon, glutamat ve glisin gibi amino asitlerden inşa edilen ve ROS’u nötralize etmek için merkezi bir antioksidan sistemdir. Bu bulgular, kalp hücreleri oksidatif metabolizmayı artırırken, hasarı kontrol altında tutmak için antioksidan yolaklarını da ayarladıklarını gösteriyor. 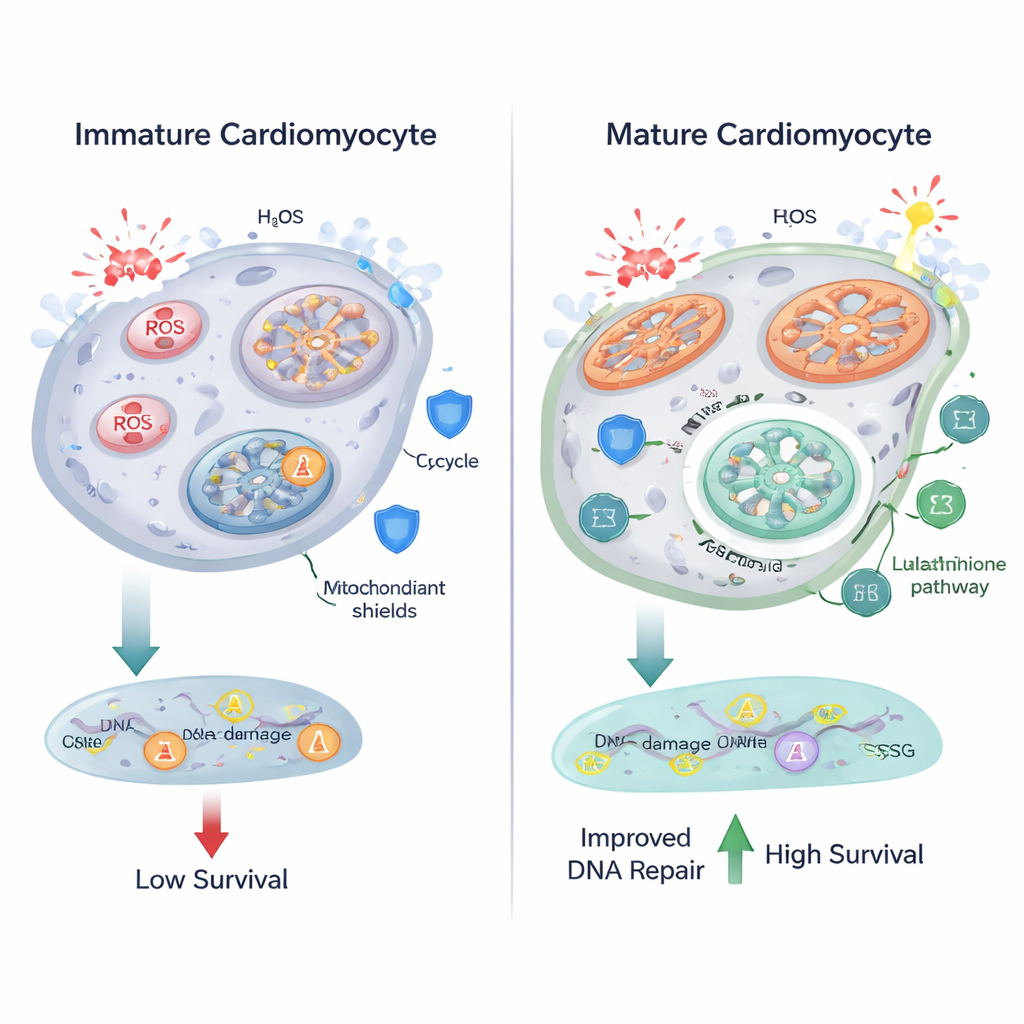
Hasar sınırlı, savunma güçlendi
Sürpriz bir şekilde, daha yüksek ROS’a rağmen farklılaşmış kardiyomiyositler, hassas bir DNA hasarı belirteci olan γ-H2AX odakları ile ölçüldüğünde, olgunlaşmamış karşıtlarına göre daha fazla DNA kırığı göstermedi. Ekip hücreleri güçlü bir oksitleyici ajan olan hidrojen peroksite maruz bıraktığında, hem olgun hem de olgunlaşmamış hücreler ROS ve DNA kırıkları biriktirdi—ancak olgun hücreler daha iyi dayanabildi. Daha yüksek ROS seviyelerine göre orantısal olarak daha az DNA lezyonu gösterdiler, PUMA gibi hücre ölümüyle ilişkili sinyallerin etkinleşmesine daha az yatkındılar ve belirgin şekilde daha yüksek hayatta kalma oranları sergilediler. Bu sonuçlar, olgunlaşan kardiyomiyositlerin sadece metabolizmalarını ayarlamakla kalmayıp aynı zamanda DNA onarım ve hayatta kalma mekanizmalarını da güçlendirdiklerini; böylece daha sert oksidatif koşullara dayanabildiklerini gösteriyor.
Kalbi korumak için ne anlama geliyor
Basitçe söylemek gerekirse, bu çalışma kalp hücreleri olgunlaştıkça yanmadan daha yüksek performans göstermeyi öğrendiklerini gösteriyor. Şeker ağırlıklı, düşük oksijenli bir yaşam tarzından oksijen yoğun, mitokondri sürümlü bir yapıya geçiyorlar ve aynı zamanda oksidatif strese karşı koymak için daha iyi kalkanlar ve onarım ekipleri inşa ediyorlar. Enerji üretimi ile özkoruma arasındaki bu hassas dengelerin anlaşılması, hasar görmüş yetişkin kalp dokusunu daha dirençli hale getirecek stratejiler geliştirmek veya kök hücreleri rejeneratif tedaviler için daha güvenli, daha dayanıklı kardiyomiyositlere yönlendirmek isteyen bilim insanlarına yardımcı olabilir.
Atıf: Novais, L.B., Rodrigues, B.R.I., Pereira, F.O.B. et al. Metabolic reprogramming enhances oxidative stress resistance in differentiating cardiomyocytes. Sci Rep 16, 5534 (2026). https://doi.org/10.1038/s41598-026-35263-5
Anahtar kelimeler: kardiyomiyosit farklılaşması, oksidatif stres, mitokondri, hücre metabolizması, kalp hastalığı