Clear Sky Science · tr
Deglikozilasyon, mannoz reseptörü CD206’da yeni bir distal konformasyon oluşturur
İmmün algılayıcıların üzerindeki şeker örtüler neden önemli
İmmün hücrelerimiz, mikroplar ve kanser hücreleri gibi tehditleri algılamak için moleküler “antenler”e güvenir. Bu antenlerden biri olan mannoz reseptörü CD206, immün hücrelerin şekerle kaplı molekülleri yakalamasına ve hatta tümörlere yönelmesine yardımcı olur. Birçok protein gibi CD206 da küçük şeker zincirleriyle kaplıdır. Bu çalışma, büyük çıkarımları olabilecek görünümsüz basit bir soruyu sorar: o şekerler çıkarıldığında CD206’nın şekli ve işlevi ne olur?
Şekerli sinyalleri okuyan esnek bir kol
CD206, özellikle dokularda ve tümörlerde devriye gezen makrofajlarda olmak üzere belirli immün hücrelerin yüzeyinde bulunur. Hücre zarından uzanan uzun, eklemlenmiş bir yapıya sahiptir ve uç kısmında geçen moleküllerdeki şekeri tanıyan birkaç “lektin” bölümü bulunur. CD206 ayrıca kana salınabilir; kandaki düzeyleri inflamasyon ve fibrozis gibi hastalıklarla ilişkilidir ve bu da onu hastalık için potansiyel bir belirteç yapar. Protein N-bağlantılı şeker zincirleriyle yoğun şekilde süslenmiştir; önceki çalışmalar bu şekerlerin reseptörün farklı bölümlerinin şekerleri ne kadar iyi tanıdığı üzerinde etkisi olabileceğini göstermişti. Bu şeker bağlanma yerlerinin çoğu ana bağlanma ceplerinden uzaktır, bu da onların basit engelleyicilerden ziyade uzak anahtarlar gibi davranabileceğini düşündürür.
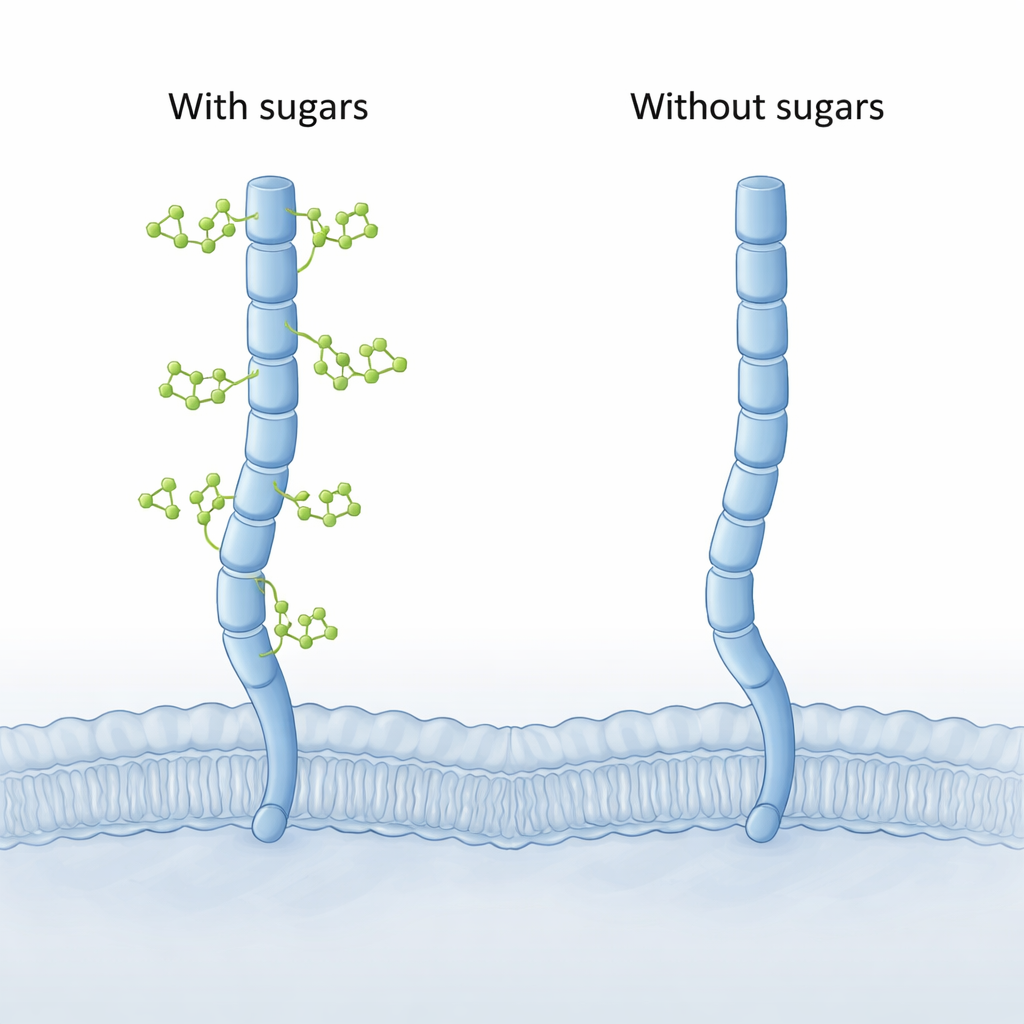
Bilgisayar modelleri gizli bir bükülme ortaya koyuyor
CD206’nın tam üç boyutlu yapısı henüz deneysel olarak yakalanmadığından, yazarlar modern hesaplamalı araçlara başvurdular. Önce AlphaFold kullanarak reseptörün tam uzunluk modellerini oluşturup sonra şekerli ve şekersiz hallerinin uzun, ayrıntılı moleküler dinamik simülasyonlarını çalıştırdılar. Her iki versiyon da uzamış bir moleküler kol gibi davrandı, ancak “şeker-siz” formun uç kısmında çarpıcı yeni bir hareket görüldü. Son iki lektin bölümü (CTLD7 ve CTLD8 olarak adlandırılan) içe doğru sallanarak konkav, içe kıvrık bir uç oluşturabiliyordu; bu şekil, daha dışa kıvrık veya konveks kalan şekerle kaplı versiyonda hiç görülmedi.
Küçük bir değişiklik hareketi nasıl yeniden şekillendirir
Bu farkı anlamak için ekip simülasyonlardaki baskın hareketleri analiz etti. İki formu ayıran ana hareketin distal ucun bu bükülmesi olduğunu ve bunun yalnızca şekerler yokken ortaya çıktığını buldular. Şekerlerin çıkarılması genel olarak reseptörü daha esnek hale getirdi; özellikle uzak lektin segmentlerinde ve daha az ölçüde N-terminus yakınında esneklik arttı. Proteinin farklı bölümlerinin birlikte nasıl hareket ettiğini gösteren korelasyon haritaları, şekerler olmadığında son iki lektin bölümünün daha uyumlu hareket ettiğini ve diğer bölgelerle daha sıkı bağlandığını gösterdi. Özetle, şekerler sadece yüzeyde oturmuyor; tüm kolun nasıl büküldüğünü ve uzunluğu boyunca nasıl haberleştiğini ayarlamaya yardımcı oluyorlar.
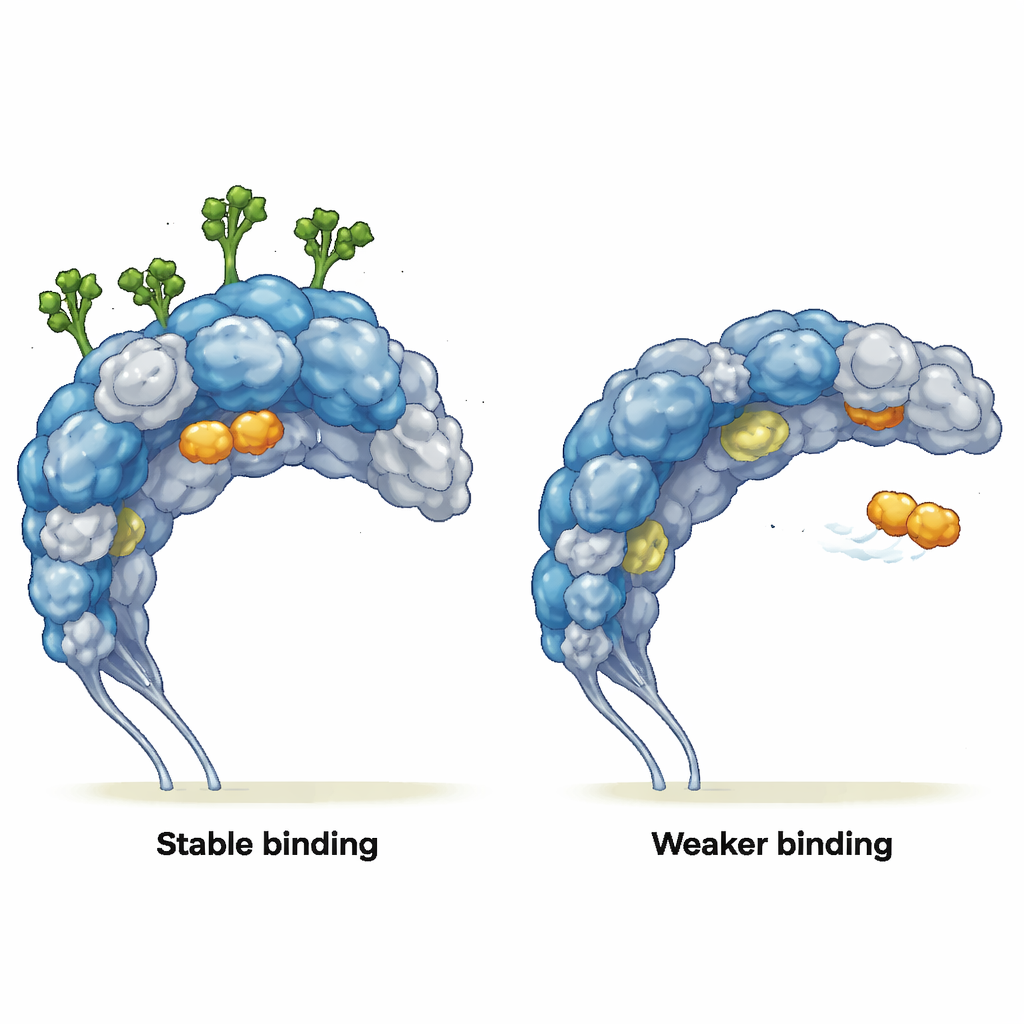
Eşlerin bağlanma biçimini değiştirmek
Yazarlar sonra bu değişmiş hareketin gerçek bağlanma ortaklarını nasıl etkilediğini sordular. İki ligandla etkileşimleri simüle ettiler: iyi tanımlanmış bir cebe oturan basit bir mannoz benzeri şeker (MMA) ve CD206-pozitif tümöre bağlı makrofajları hedefleyen bir tümör-yönlenimli peptid olan mUNO. Şekerler varken MMA tüm simülasyon boyunca bağlanma cebinde sıkıca kaldı ve ana temasları korudu; yakınındaki protein yapısı neredeyse değişmedi. Şekerler yokken MMA cebinden kaçtı, protein yüzeyi üzerinde kaydı ve yalnızca kısa, yüzeysel temaslar kurdu. mUNO için glikozile reseptör birkaç stabil bağlanma konformasyonu ve sık, uzun süreli temaslar sergiledi. Deglikozile reseptörde mUNO’nun bağlanması daha zayıf ve daha dağınıktı; ayrıca normalde şeker zincirleri tarafından engellenen bölgeleri keşfetmeye başlayarak daha önce gizli olan yeni etkileşim bölgelerini açığa çıkardı.
Hastalık ve terapi açısından ne anlama geliyor
Bir arada alındığında bu sonuçlar, CD206’ya bağlı şekerlerin onun şeklinin ve yapışkanlığının uzak düzenleyicileri olarak hareket ettiğini gösterir. Belirli bükülmeleri kısıtlayarak ve parçalarının nasıl birlikte hareket ettiğini düzenleyerek glikozilasyon, reseptörün bazı ligandları daha sıkı tutmasına ve diğerlerini tercih edilen kenetlenme noktalarına yönlendirmesine yardımcı olurken yüzeyinin bazı bölgelerini de korur. Proteinler üzerindeki genel şeker desenlerinin sıklıkla değiştiği kanser gibi hastalıklarda, CD206 farklı şekiller ve bağlanma davranışları benimseyebilir ve immün hücrelerin çevrelerini algılama şeklini değiştirebilir. Bu şeker-bağımlı “konformasyonel anahtar”ı anlamak, CD206’nın nasıl çalıştığını açıklamakla kalmaz, aynı zamanda tümörlerde ve diğer patolojik durumlarda değişen yüzeyini kullanan yeni ilaç veya görüntüleme ajanları tasarlamak için de yollar önerir.
Atıf: Alvarez, G., Di Lella, S., Pickholz, M. et al. Deglycosylation induces a novel distal conformation in the mannose receptor CD206. Sci Rep 16, 5239 (2026). https://doi.org/10.1038/s41598-026-35240-y
Anahtar kelimeler: mannoz reseptörü, protein glikozilasyonu, immün tanıma, tümöre bağlı makrofajlar, moleküler dinamikler