Clear Sky Science · tr
Entegre proteomik ve metabolomik, fitoseskiterpen laktonların TNBC hücre aktivitesini ATP sentezini tüketerek ve primer metabolizmayı yeniden programlayarak engellediğini ortaya koyuyor
Agresif Meme Kanserini Aç Bırakan Bitkisel Bileşikler
Triple-negatif meme kanseri, birçok ilacın hedeflediği tipik hormon “tutamaklarından” yoksun olduğu için tedavisi en zor olan meme kanseri türlerinden biridir. Bu çalışma, tıbbi bir bitkiden elde edilen iki molekülün bu kanser hücrelerinin iç enerji santrallerini kapatıyor gibi göründüğünü; enerji kaynaklarını keserken normal meme hücrelerini büyük ölçüde koruduklarını inceliyor. Bu mekanizmanın anlaşılması, şu anda sınırlı seçeneğe sahip hastalar için daha nazik ve hedefe yönelik tedavilere kapı açabilir.
Kanserin Güç Kaynağını Hedeflemenin Önemi
Her hücre, temel yakıtı ATP’yi üretmek için mitokondri adı verilen küçük yapılara dayanır. Özellikle agresif kanser hücreleri, hızlı büyüme, yayılma ve strese dayanma süreçlerini desteklemek için mitokondrilerine olağanüstü derecede bağımlı olabilir. Araştırmacılar, meme kanserlerinin yaklaşık %15–20’sini oluşturan ve diğer türlere göre daha sık nüks ve metastaz yapan triple-negatif hücrelere odaklandı. Çalışmada deoksyelefantopin (DET) ve onun rafine türevi DETD-35 adlı doğal moleküller incelendi; her ikisi de Elephantopus adlı tıbbi bitkiden elde edilen seskiterpen laktonlardır. Önceki çalışmalar bu bileşiklerin kanser hücrelerinde oksidatif stres ve alışılmadık hücre ölümü biçimlerini tetiklediğini göstermiştir, ancak enerji fabrikalarını nasıl bozdukları tam olarak anlaşılamamıştı.
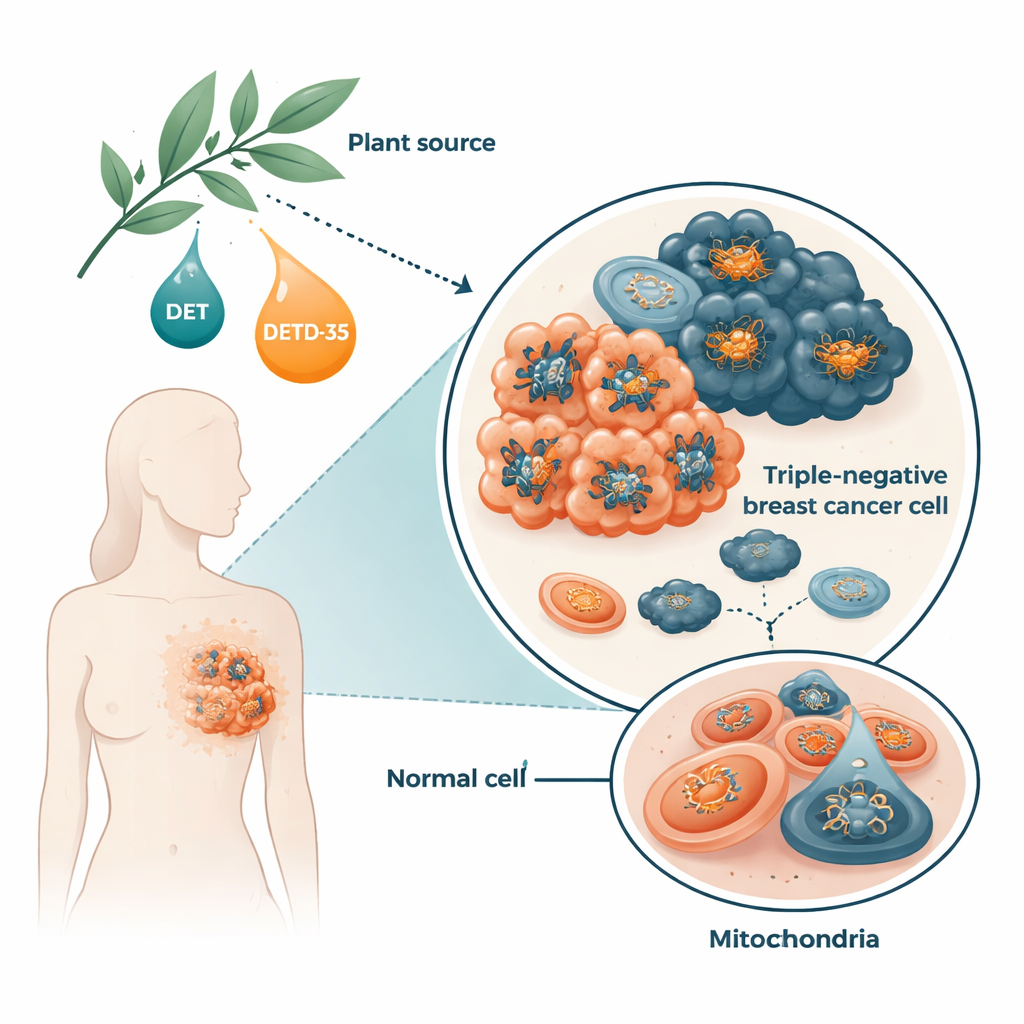
Bitkisel Moleküller Kanser Hücre Mitokondrilerini Nasıl Bozar
Laboratuvarda yetiştirilen insan triple-negatif meme kanseri hücrelerini kullanarak ekip, DET ve DETD-35’in reaktif oksijen türü üretimini hızla artırdığını buldu; bunlar enerji üretimi sırasında oluşan kimyasal olarak reaktif bir “egzoz” türüdür. Buna yanıt olarak hücreler bazı koruyucu enzimleri yükseltti, ancak dengeyi geri getirecek düzeyde değildi. Bu bileşikler ayrıca mitokondri zarında geçirgenlik geçiş gözenekleri olarak bilinen bir kanalın açılmasına neden oldu; bu değişim şişme, zar yükünün kaybı ve hücre ölümünün erken adımlarıyla ilişkilidir. Sadece birkaç saat içinde kanser hücrelerindeki ATP düzeyleri keskin şekilde düştü. Araştırmacılar önceden bir antioksidan eklediklerinde bu zararlı etkiler büyük ölçüde geri döndü; bu da oksidatif stresin sürecin kilit bir parçası olduğunu gösterdi.
Proteinler ve Metabolizmadaki Hasarı Haritalama
Büyük resmi anlamak için bilim insanları iki güçlü “omiks” yaklaşımını birleştirdi. Muamele edilen ve edilmemiş hücrelerde binlerce mitokondriyal proteini katalogladılar ve birçok küçük metaboliti ölçtüler. Bu entegre görüntü, DET ve DETD-35’in mitokondrilerin ATP üretmek için kullandığı ana yol olan oksidatif fosforilasyonla ilişkili proteinleri bozduğunu ve ölümle ilişkili sinyallemeyi aktifleştirdiğini ortaya koydu. Aynı zamanda amino asitler, yağlar ve DNA için yapı taşlarını işleyen temel metabolik yollar yeniden düzenlendi. İç mitokondriyal zarı şekillendirmeye yardımcı olan belirli lipidler ile antioksidan savunmalar ve şeker yıkımıyla ilişkili moleküller, strese maruz kalmış ve enerji kıtlığı içindeki kanser hücreleriyle tutarlı şekilde değişti. Kritik olarak, bu yaygın değişiklikler aynı dozlara maruz kalan normal meme hücrelerinde görülmedi; bu da tümör hücrelerine karşı belli bir seçicilik olduğunu düşündürüyor.
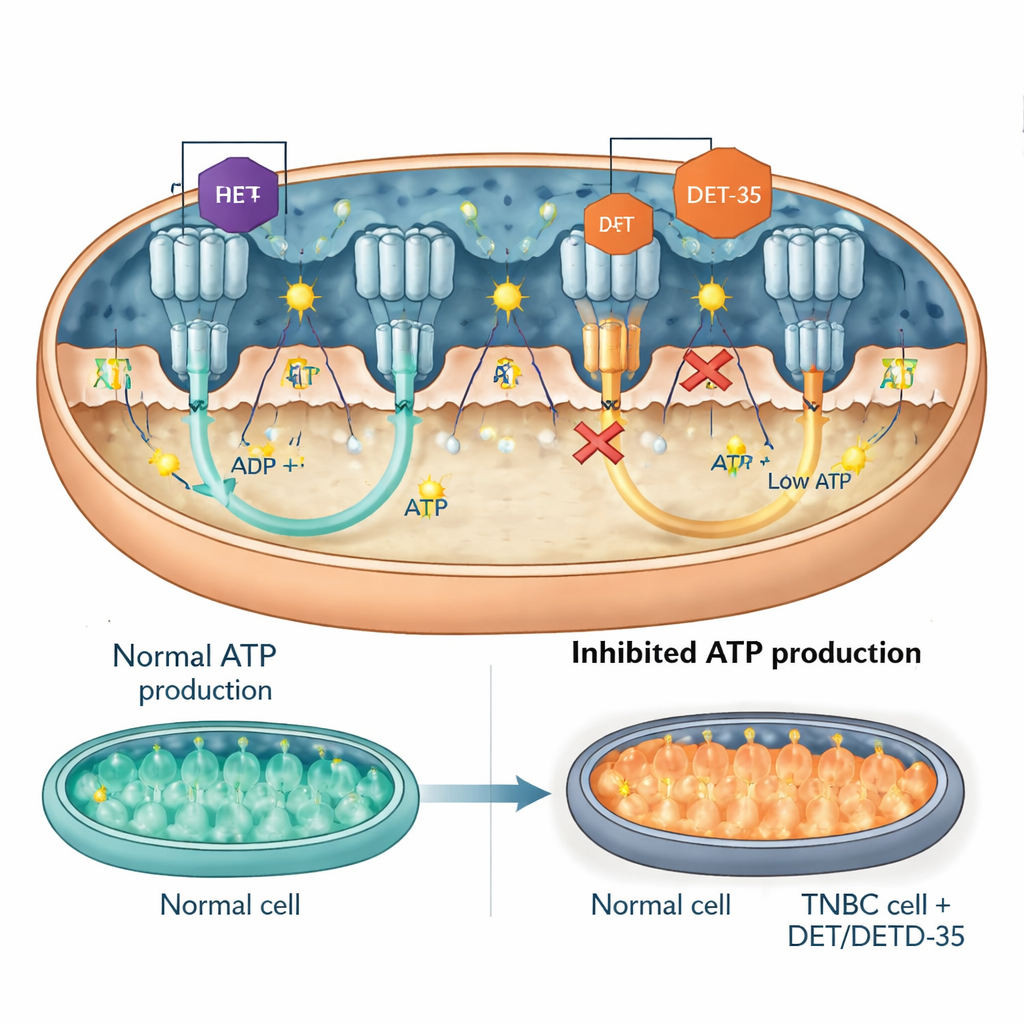
Anahtar Bir Sinyal Proteini ve ATP Türbini
Ekip daha sonra bu bozulmuş ağlardaki belirli oyunculara yoğunlaştı. Bunlardan biri, mitokondriye geçip hem enerji çıktısını hem de stres yanıtlarını etkileyebilen PRKCA adlı bir sinyal proteiniydi. DET ve DETD-35 kanser hücrelerinde PRKCA düzeylerini artırdı. Araştırmacılar PRKCA’yı genetik araçlarla azaltınca ilaçların toksisitesi azaldı: kanser hücreleri hayatta kalma olasılığı daha yüksek oldu, daha fazla ATP ürettiler ve mitokondriyal işlev bozukluğu ile apoptoz belirtileri daha az görüldü. Bir diğer odak noktası ise ATP üretmek için dönen moleküler “türbin” olan ATP sentazdı. Ölçümler, DET ve DETD-35’in kanser hücresi mitokondrilerindeki ATP sentaz aktivitesini doğrudan azalttığını gösterdi. Bilgisayar docking modelleri her iki bileşiğin de enzimin kritik ara yüzlerine yerleştiğini; bilinen ATP sentaz engelleyici ilaçların bağlandığı genel bölgelerle örtüştüğünü ve mekanik olarak hareketini engelleyerek ATP üretimini kestiğini öne sürdü. İnsan triple-negatif meme tümörü taşıyan farelerde yapılan tedaviler, her iki bileşiğin de tümör dokusundaki ATP sentaz bileşenlerinin düzeylerini düşürdüğünü gösterdi; bu bulgular hücre kültürü verilerini destekliyor.
Gelecek Kanser Tedavileri İçin Ne Anlama Gelebilir
Genel olarak çalışma tutarlı bir resim çiziyor: bu bitki kökenli bileşikler, triple-negatif meme kanseri hücrelerini oksidatif stresle aşırı yükleyerek, mitokondri gözeneklerini aralayarak ve ATP üreten makineyi doğrudan kilitleyerek enerji krizi içine itiyor. ATP tükenip metabolizma karışınca kanser hücreleri büyüme ve hayatta kalma yeteneklerini yitiriyor; aynı koşullar altında normal meme hücreleri büyük ölçüde zarar görmüyor. Bir okuyucu için çıkarım şudur: bilim insanları, dikkatle tasarlanmış moleküller—bazıları bitkilerden ilham alabilir—kullanarak kanserin iç enerji istasyonlarına olan güçlü bağı istismar edebilir ve tümör hücrelerinin pillerini boşaltırken sağlıklı dokuyu koruyabilir. Bu tür ajanların klinik kullanımına ulaşmadan önce daha çok çalışma gerekiyor, ancak proteinlerin, metabolitlerin ve enerji akışının entegre görünümü umut verici bir yol haritası sunuyor.
Atıf: Shiau, JY., Huang, HJ., Nakagawa-Goto, K. et al. Integrated proteomics and metabolomics reveal phytosesquiterpene lactones inhibit TNBC cell activity by depleting ATP synthesis and reprogramming primary metabolism. Sci Rep 16, 5264 (2026). https://doi.org/10.1038/s41598-026-35194-1
Anahtar kelimeler: triple-negatif meme kanseri, mitokondri, ATP sentaz, doğal ürünler, kanser metabolizması