Clear Sky Science · tr
Gıdalardan ve bağırsak mikrobiyotasından gelen bakteriler metilglioksal üretir ve bu metabolit biyolojik olarak aktif 1‑asetil‑β‑karbolin alkaloidlerinin oluşumuna yol açar
Bağırsaklarınızdaki kimya laboratuvarının önemi
Bağırsaklarımızın içinde ve birçok fermente gıdada, trilyonlarca bakteri yediğimiz şekerleri sürekli olarak bir dizi kimyasal yan ürüne dönüştürür. Bu çalışma, bu yolların birini ayrıntılı olarak inceliyor: bazı yaygın bakterilerin şekerleri nasıl yüksek reaktiviteye sahip bir bileşik olan metilglioksale dönüştürdüğünü ve bunun ardından 1‑asetil‑β‑karbolin adı verilen biyolojik olarak aktif molekül ailesine nasıl dönüştüğünü. Bu maddeler hem hastalık süreçleriyle hem de potansiyel yeni ilaçlarla ilişkilendirildiğinden, bakterilerin ne zaman ve nasıl bunları ürettiğini anlamak gıda, mikrobiyom ve sağlık konusundaki düşüncelerimizi yeniden şekillendirebilir.
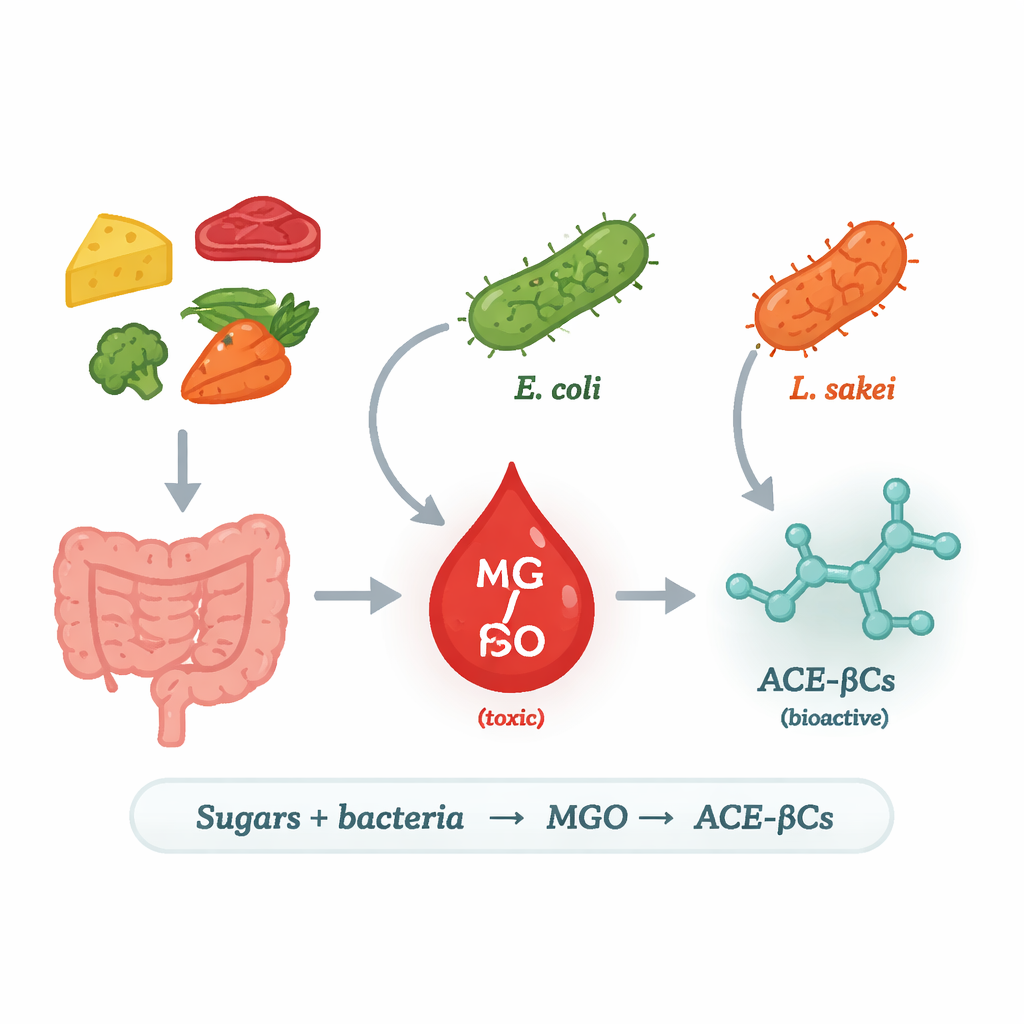
Günlük şekerlerden riskli bir moleküle
Araştırmacılar metilglioksal (MGO) üzerine odaklandı; şeker parçalanmasının çok reaktif, toksik bir yan ürünü. İnsanlarda aşırı MGO, proteinleri ve DNA’yı hasara uğratabildiği için diyabet, kalp hastalıkları ve nörodejenerasyonla ilişkilendiriliyor. Hücrelerimiz normalde detoks sistemleriyle MGO’yu kontrol altında tutar, ama tek kaynak onlar değildir: bakteriler de MGO üretebilir. Bazı mikroplarda, metilglioksal sentaz (MgsA) adlı bir enzim, şeker metabolizmasının bir ara ürününü doğrudan MGO’ya çevirerek enerji metabolizmasında bir “kısayol” yaratır. Ekip hangi gıda ve bağırsak bakterilerinin bu yolu kullandığını, hangi koşullarda kullandığını ve saldıkları MGO ile neler olduğunu sordu.
Bakteriyel üreticiler kimler?
Bunu yanıtlamak için bilim insanları, gıdalarda sık bulunan birkaç laktik asit bakteri suşunu ve laboratuvar suşu Escherichia coliyi, kontrollü bir ortamda glikoz veya galaktoz içeren besiyerinde büyüttüler. Ardından kültür sıvısında zaman içinde MGO ve iki ilgili alkaloidi yüksek hassasiyetli kromatografi ve kütle spektrometrisi ile izlediler. Yalnızca E. coli ve etle ilişkili Lactilactobacillus sakei anlamlı miktarda MGO ve alkaloidler üretti; test edilen diğer laktik asit bakterileri üretmedi. Bir genom araması önemli farkı ortaya koydu: E. coli ve L. sakei MgsA genini taşırken, laktik asit akrabalarının çoğu bunu taşımıyordu. Araştırmacılar L. sakeiden alınan mgsA genini üretmeyen bir suşa yerleştirdiklerinde, bu mühendislikli bakteri hem MGO hem de alkaloidleri üretmeye başladı ve böylece MgsA bu yol ile güçlü bir şekilde ilişkilendirildi.
MGO nasıl toksik olmaktan biyolojik olarak aktif alkaloidlere dönüşüyor
Bir sonraki soru, MGO yapıldıktan sonra ne olduğuydu. Ekip 1‑asetil‑β‑karbolin alkaloidleri (ACE‑βC’ler) üzerine odaklandı; bunlar antimikrobiyal, anti‑inflamatuar ve antikanser aktivitiler bildirilmiş küçük moleküller. MGO üreten bakteriler L‑triptofan amino asidi varlığında büyütüldüğünde, iki ACE‑βC — 1‑asetil‑β‑karbolin ve onun 3‑karboksilik asit formu — düzeylerinin hızla arttığını gösterdiler. Ortama ek MGO ilavesi de bunların oluşumunu artırdı. Bu, MGO’nun hücrelerden sızdığını ve çevredeki sıvıda herhangi bir ek enzim olmaksızın L‑triptofana kendiliğinden reaksiyona girerek bu biyolojik olarak aktif bileşikleri oluşturduğunu gösterir. Başka bir deyişle, MGO’yu tehlikeli kılan aynı kimya, onu potansiyel olarak yararlı etkileri olabilecek daha karmaşık moleküllere dönüştürüyor.
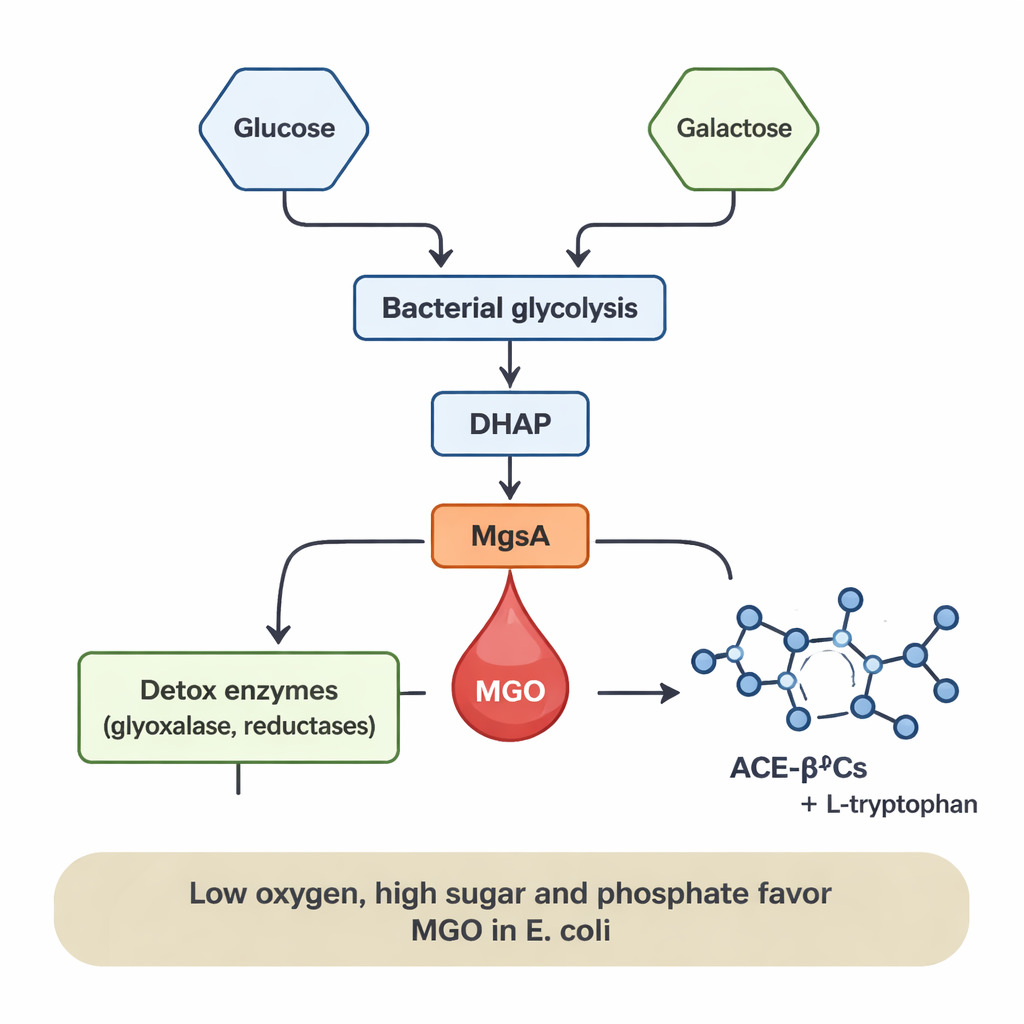
Ne üretimi artırır veya azaltır
MGO üretimi sabit değildi; büyük ölçüde bakterinin beslenmesine ve çevresine bağlıydı. E. colide MGO yalnızca glikoz varlığında ortaya çıktı ve düzeyleri glikoz konsantrasyonu arttıkça yükseldi. Fosfat eklenmesi, fosforlu şeker ara ürünlerinin birikimini teşvik ederek MgsA kısayolunu beslediği için MGO oluşumunu birkaç kat artırdı. İnsan bağırsağına benzer düşük oksijen (anaerobik) koşullar da MGO salınımını desteklerken, iyi havalandırılmış yüksek oksijen koşulları bakteriler iyi büyüse bile bunu keskin şekilde azalttı. Buna karşılık, L. sakei esas olarak galaktoz üzerinde büyütüldüğünde MGO üretti ve üretim daha yüksek galaktoz düzeyleriyle arttı. Bu desenler, bakteriyel metabolizma üzerinden şeker akışı yüksek ve oksijen sınırlı olduğunda, biriken şeker ara ürünlerinin oluşturduğu yükü hafifleten bir “basınç tahliye valfi” olarak MGO’nun iş görebileceğini düşündürüyor.
Gıda ve sağlık için olası anlamları
Bu bulgular, tüm bağırsak veya gıda bakterilerinin MGO ve ACE‑βC üretme yeteneği açısından eşit olmadığını gösteriyor. MgsA enzimi taşıyan türler — belirli L. sakei suşları ve E. coli gibi — özellikle bağırsak veya bazı fermantasyonlarda olduğu gibi şeker açısından zengin, düşük oksijenli ortamlarda önemli katkıda bulunabilir. Salgıladıkları MGO, konak dokular üzerindeki kimyasal yükü artırabilir, ancak MGO’nun ACE‑βC alkaloidlerine dönüşümü aynı zamanda bu reaktif bileşiği kısmen “temizlerken” kendi biyolojik etkilerine sahip moleküller üretebilir. Bu çalışma laboratuvar kültürlerinde yapılmış olsa da, diyet, mikrobiyota bileşimi ve bakteriyel metabolizmanın bir araya gelerek vücudumuzdaki zararlı ve potansiyel olarak faydalı kimyasallar arasındaki dengeyi nasıl şekillendirebileceğine dair makul bir yol gösteriyor ve ACE‑βC’leri gıdalarda ve bağırsakta bakteriyel MGO üretiminin olası belirteçleri olarak işaret ediyor.
Atıf: Herraiz, T., Sánchez-Arroyo, A., de las Rivas, B. et al. Bacteria from foods and gut microbiota produce methylglyoxal and this metabolite leads to the formation of bioactive 1-acetyl-β-carboline alkaloids. Sci Rep 16, 4905 (2026). https://doi.org/10.1038/s41598-026-35162-9
Anahtar kelimeler: bağırsak mikrobiyotası, metilglioksal, bakteriyel metabolizma, gıda fermantasyonu, beta‑karbolin alkaloidleri