Clear Sky Science · tr
Laktat, kardiyomiyosit ferroptozunu teşvik etmek ve miyokard iskemi-reperfüzyon hasarını ağırlaştırmak için YTHDF2-FTH1 eksenini düzenliyor
Kalp hastalarının bu kimya ile neden ilgilenmesi gerekiyor
Doktorlar kalp krizi sonrası tıkalı bir koroner arterin yeniden açılmasını sağladığında, taze kan kası kurtarır ancak aynı zamanda iskemi–reperfüzyon hasarı olarak bilinen ek zarara yol açabilir. Bu çalışma, kalp hücrelerinin içinde şaşırtıcı bir suçluyu ortaya koyuyor: yaygın bir metabolik yan ürün olan laktat. Yazarlar, laktatın kalp hücrelerini demire bağlı belirli bir hücre ölümü türüne iten moleküler bir anahtarı çevirabildiğini ve böylece hasarı ağırlaştırdığını gösteriyor. Bu gizli yolun anlaşılması, acil tedavi sırasında kalbi daha iyi koruyacak yeni ilaçlara işaret edebilir.
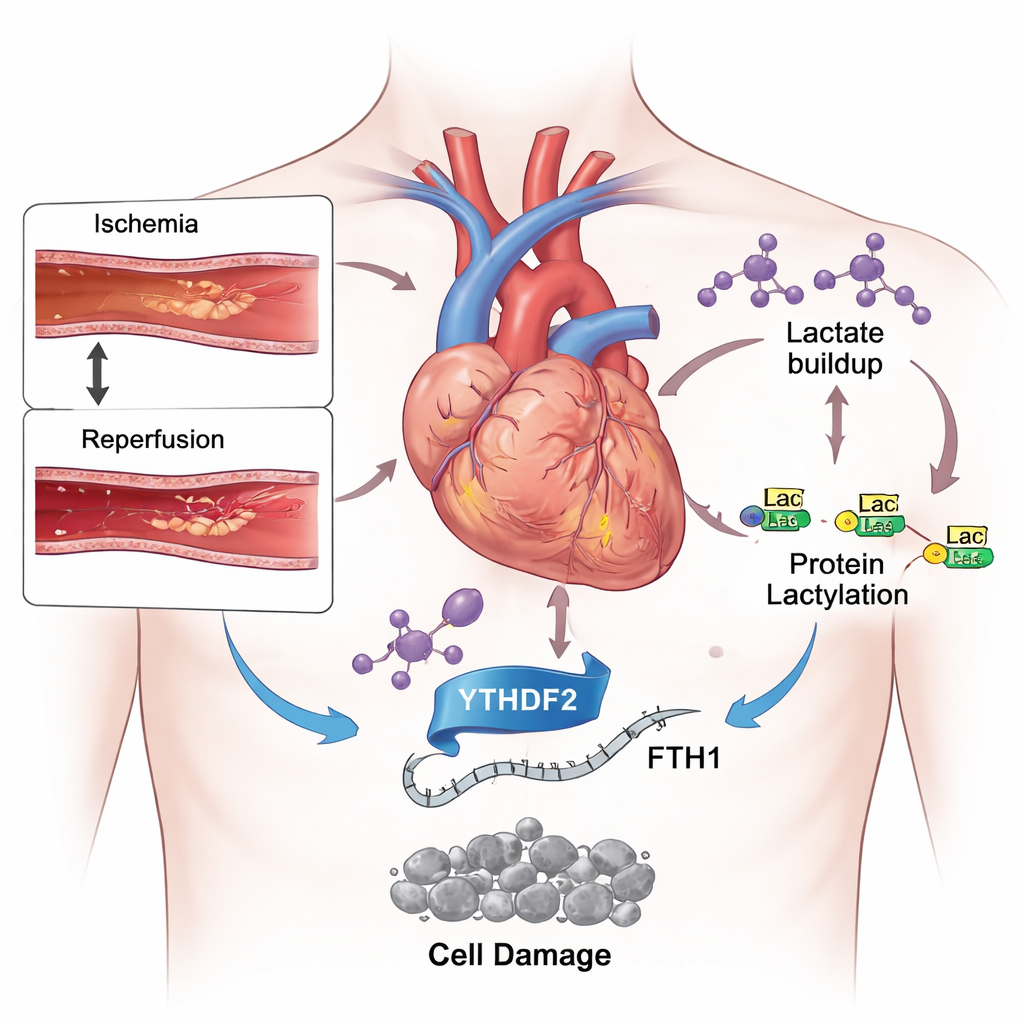
Kalp krizi tedavisinde çift taraflı bir kılıç
Modern tıp tıkalı koroner arterleri hızla yeniden açmada çok başarılı hale geldi ve kalp krizinin ilk zararını sınırlıyor. Yine de kan akışı yeniden sağlandıktan sonra hastalar büyük miktarda kalp kasını kaybedebiliyor. Bunun bir nedeni, oksijen ve besinlerin ani geri dönüşünün kalp hücreleri içinde kimyasal bir stres fırtınası yaratmasıdır. Bu ortamda tetiklenen çeşitli hücre ölümü türleri arasında, ferroptoz adı verilen daha yeni bir tür dikkat çekiyor. Apoptoz gibi daha tanıdık formlardan farklı olarak ferroptoz demire ve hücre zarlarındaki yağların kontrolden çıkan oksidasyonuna bağlıdır; bu da kalbi kalıcı olarak zayıflatabilir.
Laktatın yalnızca “kas yanması” olmanın ötesine geçmesi
Bir kalp krizi sırasında, aç kalan kalp kası yakıt kullanımını glikolize kaydırır; bu, şekeri hızla parçalayan bir yedek sistemdir ancak büyük miktarda laktat üretir. Kısa süreli bir arter tıkanması ve yeniden açılmaya maruz bırakılan farelerde ve düşük oksijene ardından yeniden oksijenlenmeye tabi tutulan kültüre edilmiş kalp benzeri hücrelerde araştırmacılar keskin şekilde artmış laktat seviyeleri buldular. Aynı zamanda birçok proteinde ve DNA’yı düzenleyen iskelet olan histonlarda laktileşme adı verilen kimyasal işaretlerin arttığı tespit edildi. Hayvanlara glikolizi yavaşlatan ve laktat üretimini azaltan bir ilaç verildiğinde, kalp hasarı küçüldü, hasar kan belirteçleri azaldı ve zararlı demir ile koruyucu antioksidanlar arasındaki denge iyileşti. Bu sonuçlar, aşırı laktatın yalnızca stresin bir yan ürünü olmadığını, aynı zamanda etkin bir zarar sürücüsü olduğunu öne sürüyor.
Demirin tasmasını gevşeten moleküler bir anahtar
Daha derine inen ekip, RNA üzerindeki kimyasal işaretleri okuyup belirli mesajların ne kadar hızlı yok edileceğine karar veren bir protein olan YTHDF2’ye odaklandı. İskemi–reperfüzyon ve eklenen laktatın her ikisinin de YTHDF2 seviyelerini artırdığını ve onu kodlayan gen çevresinde laktileşmeyi yükselterek üretimini çoğalttığını keşfettiler. YTHDF2’nin ana hedeflerinden biri, hücrenin demir depolama kafesinin çekirdeğini oluşturan ferritin ağır zincir 1 (FTH1) RNA’sı çıktı. FTH1 normalde demiri güvenli bir biçimde saklayarak zararlı reaksiyonların yakıtını oluşturmasını engeller. Stres altındaki kalp hücrelerinde YTHDF2, FTH1 RNA’sına daha sıkı bağlandı ve onun bozulmasını hızlandırdı; bunun sonucu olarak hücrelerde daha az ferritin kafesi, daha fazla serbest demir, artmış oksidatif stres ve ferroptozun tipik işaretleri ortaya çıktı.
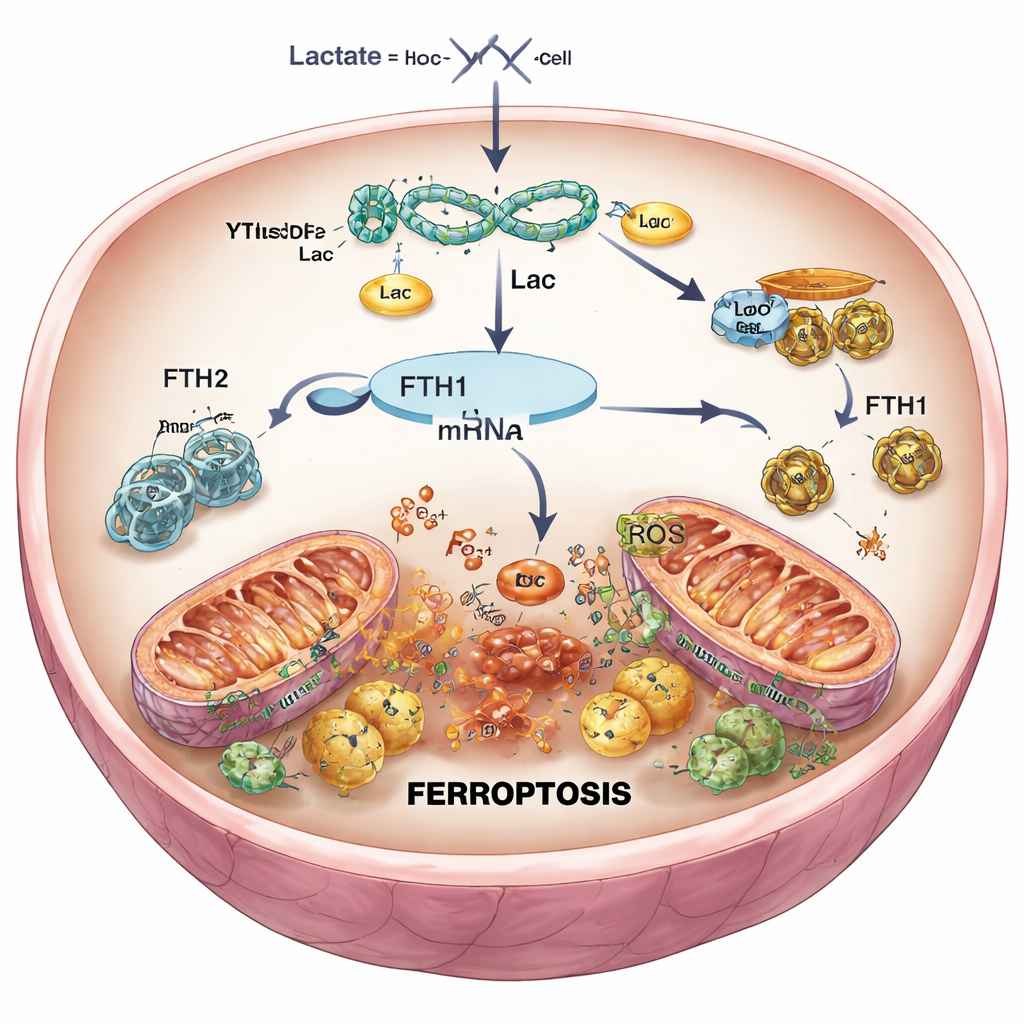
Hücrelerde ölüm sinyalini kısmak
Nedeni ve sonucu test etmek için araştırmacılar kalp hücrelerinde ve farelerde seçici olarak YTHDF2’yi azaltmak için genetik araçlar kullandılar. YTHDF2 baskılandığında, FTH1 seviyeleri toparlandı, demir ve reaktif oksijen türleri düştü, mitokondriler daha normal bir şekil korudu ve simüle edilmiş reperfüzyondan sonra genel hücre sağkalımı iyileşti. Farelerde daha az YTHDF2, daha küçük kalp krizi skarları ve daha sağlıklı görünen doku anlamına geldi. Ancak FTH1 eşzamanlı olarak azaltıldığında, bu faydalar büyük ölçüde ortadan kalktı: demir yeniden yükseldi, oksidatif hasar geri döndü ve enfarktüs büyüklüğü arttı. Bu, YTHDF2’nin esas olarak FTH1’i baskılayarak kalp hücreleri içindeki demir kontrolünü gevşettiği ve ferroptozu teşvik ettiği sonucunu doğruladı.
Gelecekteki kalp tedavileri için anlamı
Parçaları birleştirdiğinde çalışma yeni bir olay zincirini ortaya koyuyor: tıkalı ve sonra yeniden açılan bir arter laktat birikimine yol açıyor; laktat laktileşme yoluyla YTHDF2’yi artırıyor; YTHDF2 ardından demiri koruyan protein FTH1’in RNA talimatlarını yok ediyor; ve ortaya çıkan demir yükü ferroptozu tetikleyerek kalp hasarını derinleştiriyor. Hastalar için mesaj umut verici: bu yol birkaç yeni müdahale noktası sunuyor. Zararlı laktat sinyalini sınırlayan, YTHDF2’nin spesifik modifikasyonunu engelleyen veya FTH1 fonksiyonunu koruyan ilaçlar acil reperfüzyonu daha güvenli hale getirebilir ve daha fazla kalp kasını koruyabilir. Bu bulguların insan dokularında doğrulanması gerekse de, kalp krizi geçirenler için daha nazik ve etkili tedavilere doğru umut verici bir yol açıyor.
Atıf: Xiang, Z., Xiang, B., Ouyang, T. et al. Lactate regulates the YTHDF2-FTH1 axis to promote cardiomyocyte ferroptosis and aggravate myocardial ischemia-reperfusion injury. Sci Rep 16, 4865 (2026). https://doi.org/10.1038/s41598-026-35130-3
Anahtar kelimeler: kalp krizi, laktat, demir kaynaklı hücre ölümü, iskemi reperfüzyon hasarı, kardiyomiyosit koruması