Clear Sky Science · tr
Kolon histopatolojisinde performans ve genelleştirme zorluklarına odaklanan kompakt derin öğrenme modelleri
Bu araştırma hastalar ve doktorlar için neden önemli
Kolon kanseri, dünyadaki en ölümcül kanserlerden biridir; ancak teşhis hâlâ doku örneklerinin mikroskop görüntülerini uzmanların dikkatle incelemesine dayanıyor; bu süreç yavaş ve uzlaşmazlığa açık. Bu çalışma, çok küçük ve verimli yapay zeka (YZ) modellerinin, sınırlı hesaplama gücü olan klinikler de dahil olmak üzere günlük uygulamalarda kanserli kolon dokusunu yeterince doğru şekilde işaretleyip işaretleyemeyeceğini araştırıyor. Ayrıca gizli bir zayıflığı ortaya koyuyor: geliştirme aşamasında neredeyse mükemmel görünen modeller, gerçek dünyadaki yeni verilerde hâlâ ağır şekilde aksayabiliyor.
Bilgisayarlara mikroskop görüntülerini okutmak
Bir kolon biyopsisi alındığında, patologlar boyanmış ince doku kesitlerini mikroskop altında inceler. Kanserli dokuda bozulmuş bez yapıları, düzensiz hücre şekilleri ve çevre dokulara invazyon görülebilir; sağlıklı doku ise düzenli, sıra hâlinde desenler sergiler. Yazarlar, kanser (kolon adenokarsinomu) ve benign doku arasında eşit olarak dağıtılmış 24.000 dijital görüntü içeren halka açık bir koleksiyon kullandı. Tüm görüntüler standart küçük bir boyuta yeniden boyutlandırıldı ve kesitlerin kesilme, boyanma ve taranma biçimlerindeki doğal varyasyonu taklit etmek için küçük döndürmeler, yatay/dikey çevirmeler, yakınlaştırmalar ve hafif renk değişiklikleri gibi gerçekçi düzenlemeler uygulandı. Bu özenli hazırlık, YZ modellerinin kesin yönelim veya parlaklık gibi yüzeysel ayrıntılar yerine anlamlı doku desenlerine odaklanmasına yardımcı olur.
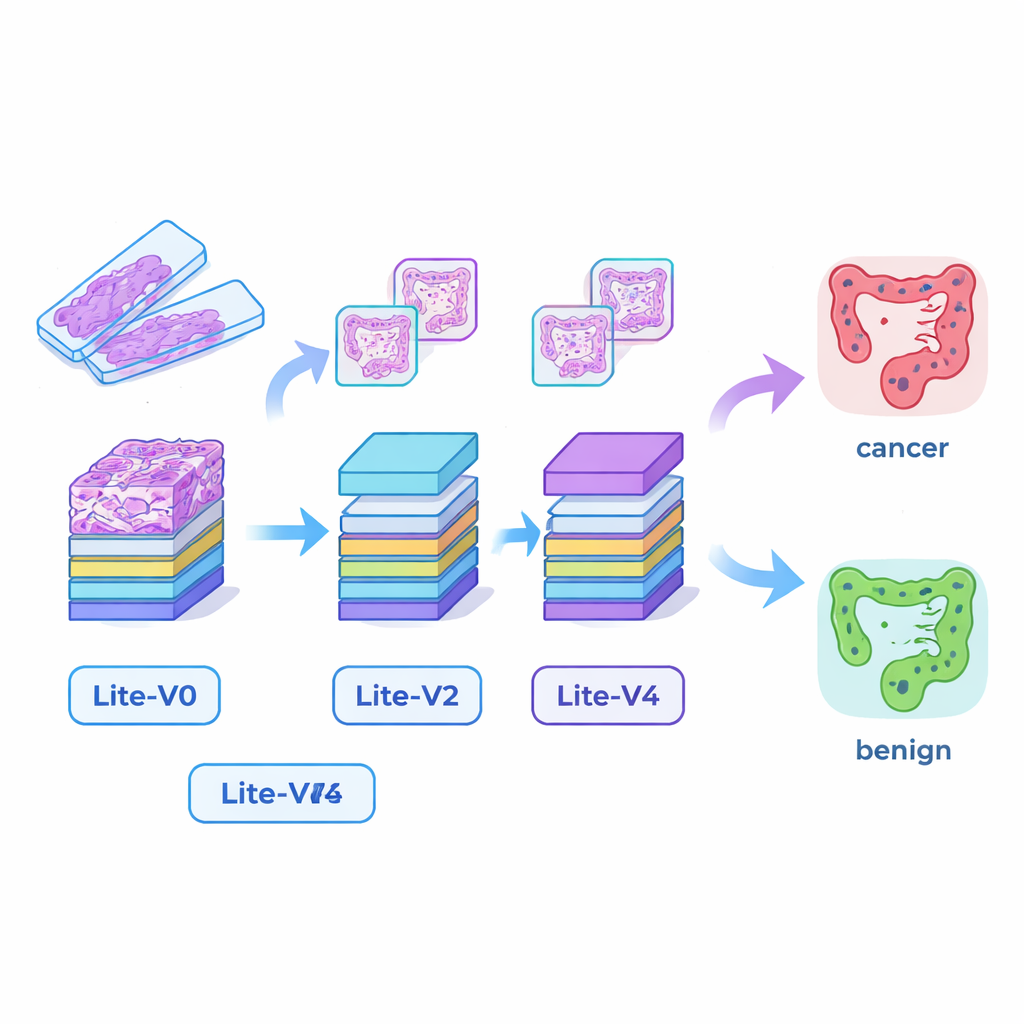
Küçük ama yetkin YZ “gözleri” oluşturmak
Birçok başarılı tıbbi YZ sistemi, güçlü grafik kartları ve çokça bellek gerektiren çok büyük derin öğrenme modellerine dayanır; bu da onları daha küçük hastanelerde veya yatak başında kullanımı zorlaştırır. Bu uçurumu kapatmak için araştırmacılar dört kompakt konvolüsyonel sinir ağı tasarladı—Lite‑V0, Lite‑V1, Lite‑V2 ve Lite‑V4. Her biri aynı giriş görüntü parçalarını inceliyor, ancak kenar, doku ve bez şekilleri gibi görsel özellikleri tespit etmek için kullandıkları katman ve filtre sayıları farklılık gösteriyor. Dört model de tekrarlı standart konvolüsyon, normalizasyon ve havuzlama blokları ve ardından kanser veya benign doku olasılığını veren küçük bir “karar başı” içeren basit, şeffaf bir tasarımı paylaşıyor. Amaç, temel klinik donanımda rahatça çalışabilecek kadar küçük modellerden ne kadar doğruluk elde edilebileceğini görmekti.
Laboratuvar içindeki etkileyici puanlar
Ekip, veri setinin sabit bir bölünmesi üzerinde tüm dört modeli eğitti ve karşılaştırdı; kabul görmüş ölçütler kullanıldı: doğruluk, her iki sınıf hatasını eşit tartan dengeli F1‑skoru, karmaşıklık matrisleri ve ROC ile precision–recall gibi tanısal eğriler. Orta boyutlu bir model olan Lite‑V2 öne çıktı. Yaklaşık 1,5 megabayt boyutunda ve yaklaşık 128.000 eğitilebilir parametreye sahip olmasına rağmen, dahili doğrulama setinde neredeyse kusursuz performans gösterdi; makro F1‑skoru yaklaşık 0,999 ve duyarlılık ile özgüllük neredeyse mükemmeldi. Başka bir deyişle, bu özenle hazırlanmış ortam içinde Lite‑V2, kanserli ile benign kolon dokusunu neredeyse her zaman ayırt edebiliyor ve mütevazı bilgisayarlarda kullanım için yeterince hızlı ve hafif kalıyordu.
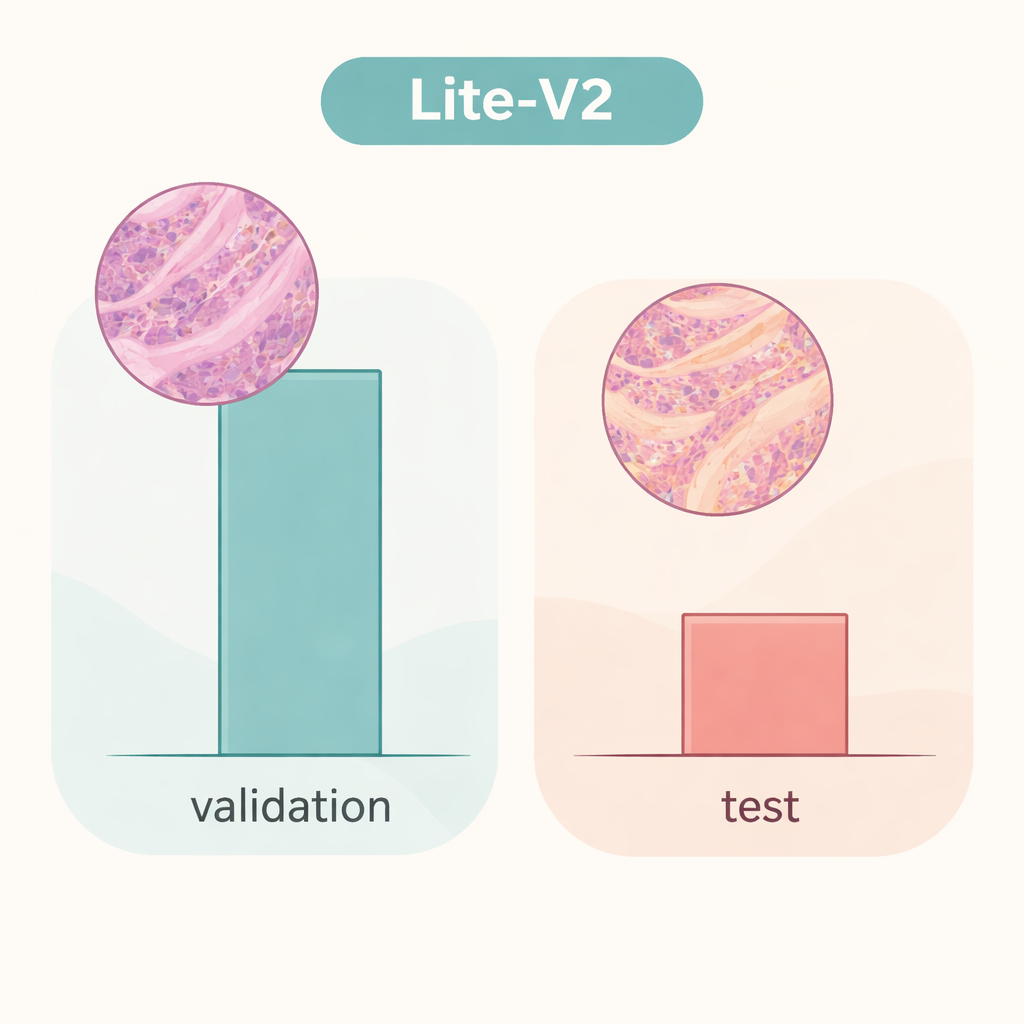
Gerçek dünyadaki farklılık büyüyü bozduğunda
Ancak aynı Lite‑V2 modeli, slaytların başka bir laboratuvardan geliyormuş gibi ince farklılıklar içeren bağımsız bir görüntü setinde test edildiğinde tablo dramatik şekilde değişiyor—araştırmacıların “alan kayması” dediği durum. Bu görülmemiş test setinde, genel doğruluk yaklaşık %50’ye düştü ve dengeli F1‑skoru yaklaşık 0,33’e geriledi. Model birçok kanser örneğini tanımaya devam etti, fakat benign doku ile ciddi şekilde zorlandı ve büyük bir kısmını malign olarak yanlış etiketledi. Bu, ağın hastalığın dayanıklı, taşınabilir imzalarından ziyade orijinal veri kaynağına sıkı sıkıya bağlı ayrıntıları—örneğin boyama stili veya tarayıcı özellikleri—öğrendiğini gösteriyor. Çalışma, iç doğrulamadaki parlak sonuçların, modeller gerçekten farklı verilerle sınanmadıkça yanıltıcı bir güven hissi verebileceğini vurguluyor.
Gelecekteki YZ tanı araçları için anlamı
Genel okuyucu için çıkarımlar iki yönlü. Birincisi, kompakt YZ sistemleri kolon doku görüntülerinde gerçekten uzman düzeyinde performansa ulaşabilirken aynı zamanda geniş dağıtım için yeterince küçük ve verimli kalabilir; bu, daha hızlı tarama ve aşırı yüklenmiş patologlara destek olma olanağı sağlar. İkincisi ve aynı derecede önemli olarak, kendi veri kümesinde “mükemmel” görünen bir model, yeni bir hastanenin görüntüleriyle karşılaştığında ciddi şekilde başarısız olabilir. Yazarlar, gelecekteki çalışmaların bu hafif modelleri boyama, tarayıcılar ve hasta popülasyonlarındaki değişikliklere karşı dayanıklı hale getirmeye odaklanması gerektiğini savunuyor—boyamaya dayanıklı eğitim, alan uyarlama ve daha geniş çok merkezli veri kümeleri gibi stratejiler kullanılarak. O zamana kadar YZ, kanser tanısında tek başına karar verici olarak değil, umut verici bir yardımcı olarak görülmelidir.
Atıf: Hanif, F., Raza, A. & Mohammed, H.A. Compact deep learning models for colon histopathology focusing performance and generalization challenges. Sci Rep 16, 5489 (2026). https://doi.org/10.1038/s41598-026-35119-y
Anahtar kelimeler: kolon kanseri, histopatoloji, derin öğrenme, hafif CNN, alan kayması