Clear Sky Science · tr
DYRK2 için bağlanma afinitesini kestirmek üzere fizik bilgili bir grafik sinir ağı: Alzheimer ilaç yeniden kullanımı
Alzheimer için neden önemli
Alzheimer hastalığı dünya genelinde artıyor; ancak mevcut ilaçların çoğu hastalığı durdurmak yerine yalnızca semptomları hafifletiyor. Yeni ilaçların laboratuvar ortamında test edilmesi yavaş ve maliyetli; bu durum, bellek ve nöral sağlıkta önemli olabilecek daha az çalışılmış beyin proteinleri için özellikle geçerli. Bu çalışma, akıllı bir kestirme yol sunuyor: fiziksel ilkeleri göz önünde bulunduran bir yapay zeka modeli kullanarak, mevcut Alzheimer ilaçlarının az çalışılmış bir protein olan DYRK2’ye ne kadar iyi tutunabileceğini tahmin etmek — bu da potansiyel olarak tedavi için yeni yollar açabilir.
Eski ilaçlara yeni bir bakış
Sıfırdan yeni bileşikler tasarlamak yerine araştırmacılar, zaten onaylanmış ve görece güvenli olduğu bilinen ilaçların yeni kullanımlarını bulmaya odaklanan ilaç yeniden kullanımı yaklaşımını benimsiyor. Dört tanıdık Alzheimer ilacını (brexpiprazol, donepezil, galantamin ve rivastigmin) inceliyor ve her birinin DYRK2’ye ne kadar sıkı bağlanabileceğini sorguluyorlar. DYRK2, nöron büyümesi ve işlevinde rol oynayan bir protein kinaz; Alzheimer’da çok az araştırıldı, ama erken kanıtlar sinapslar, aksonlar ve bellekle bağlantılı olduğunu gösteriyor, bu da onu mevcut terapilere tamamlayıcı olabilecek ilginç bir hedef yapıyor.
Molekülleri ağlara dönüştürmek
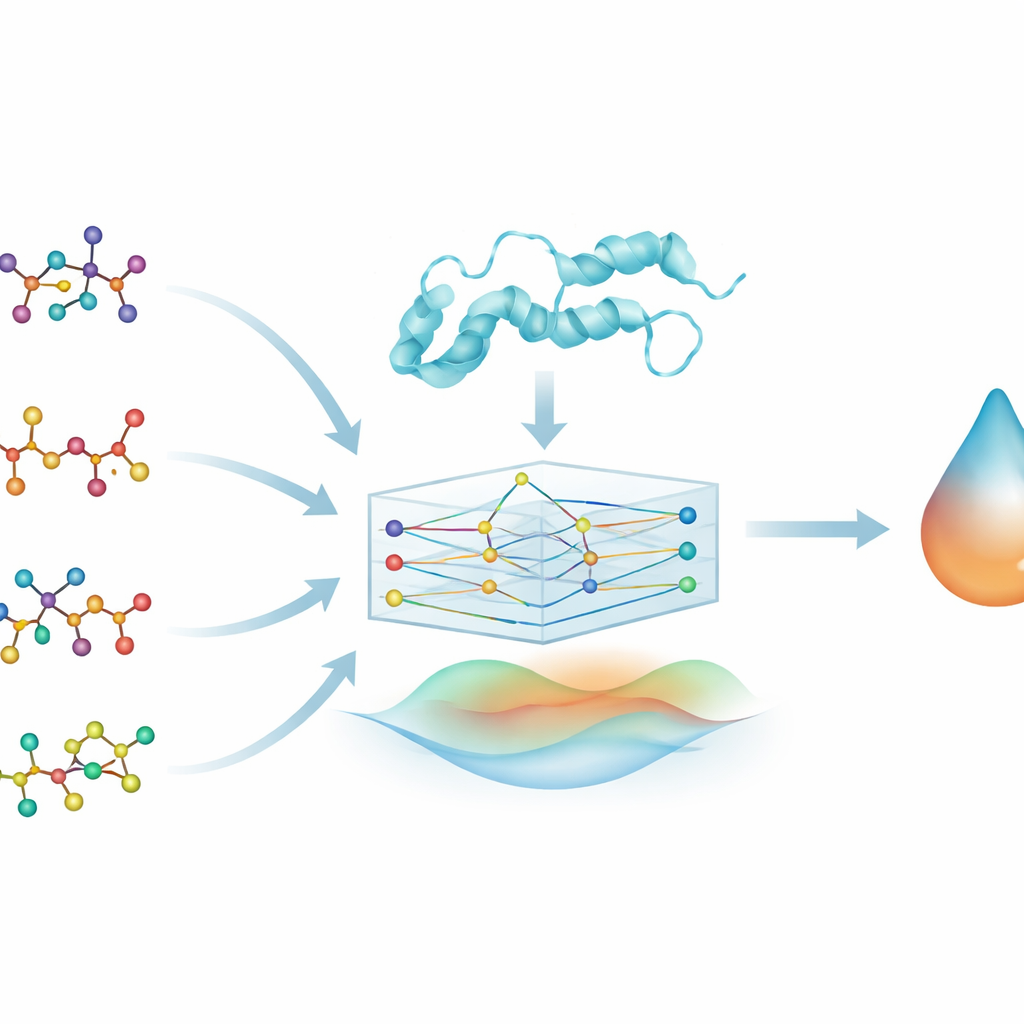
Bu ilaç–protein ilişkilerini incelemek için ekip her ilaç molekülünü bir graf olarak temsil ediyor: atomlar düğümler, kimyasal bağlar ise bunları birbirine bağlayan kenarlar oluyor. DYRK2 proteini için de benzer bir yaklaşım uygulanıyor; amino asit dizisi birbirine bağlı birimlerden oluşan bir zincir olarak temsil ediliyor. Grafik sinir ağı (GNN) adı verilen bir makine öğrenimi türü, bu grafik biçimli girdilerle doğal olarak çalışabiliyor; bağlantılar boyunca bilgi aktararak şekil ve kimya örüntülerini öğreniyor. Bu, PhysDual‑GCN adlı modelin ilacı ve DYRK2’yi basit dizi veya özellik listeleri yerine etkileşen ağlar olarak “okumasına” olanak tanıyor.
Fiziği yapay zekayla harmanlamak
İlaç keşfindeki çoğu derin öğrenme aracı yalnızca veriden öğrenir; bu da içyapılarının yorumlanmasını zorlaştırabilir. Bu çalışmada yazarlar, atomların nasıl etkileştiğine dair temel fiziksel fikirleri kasıtlı olarak modele dahil ediyor. Öğrenilmiş grafik özelliklerinin yanında PhysDual‑GCN iki klasik enerji terimini de hesaplıyor: kısmi yükler arasındaki elektriksel çekim ve itimi yakalayan bir terim ile van der Waals kuvvetlerinin itme‑çekme etkisini tanımlayan bir diğer terim. Bu fizik tabanlı enerjiler, GNN’nin içsel temsil ile birleştirilip modelin tahmini bağlanma gücünü çıkarmadan önce ekleniyor. Etkili biçimde model, özellikle AutoDock Vina ve benzeri araçların davranışını taklit edecek şekilde eğitiliyor—ancak bunu daha hızlı ve tanıdık fiziksel ilkelere dayalı kalarak yapıyor.
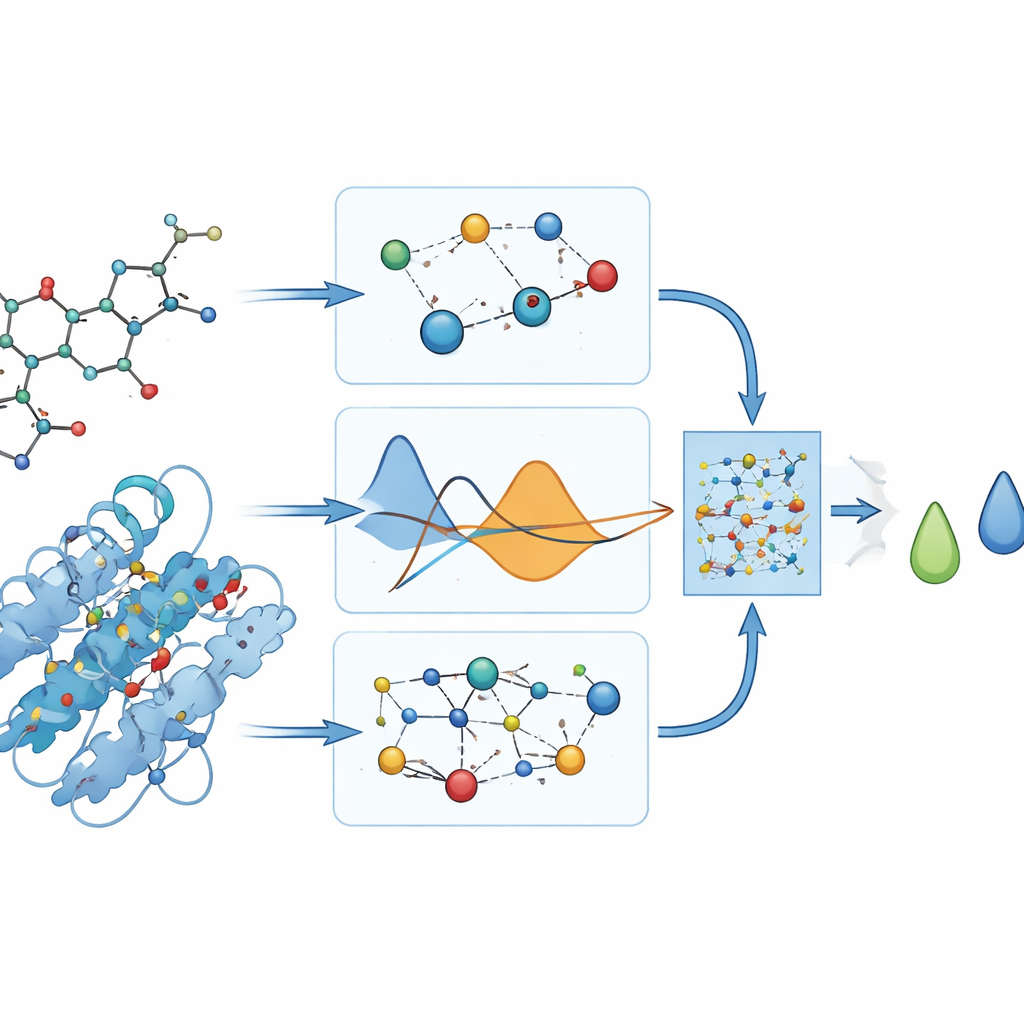
Modelin gerçekte neyi tahmin ettiği
Bu ilaçların DYRK2’ye ne kadar güçlü bağlandığına dair laboratuvar ölçümleri olmadığından yazarlar, referans bağlanma skorları olarak enerji birimlerinde verilen değerleri sağlamak için docking programlarına güveniyor. Bu skorları eğitim sürecine vermekten kaçınıyorlar ve bunun yerine PhysDual‑GCN’in ne kadar iyi öğrendiğini değerlendirmek için yalnızca sonrasında kullanıyorlar. Dört Alzheimer ilacı için model, docking değerlerini ortalama olarak küçük hatalarla (yaklaşık üçte bir kilokalori/mol civarında) yeniden üretiyor ve bileşikleri doğru sıralıyor: donepezil ve brexpiprazol en güçlü bağlayıcılar olarak öne çıkıyor, galantamin ve rivastigmin daha zayıf görünse de hâlâ makul derecede kararlı. Bu sonuçlar, fizikle bilgilendirilmiş GNN’nin daha yavaş docking çalışmalarına hesaplamalı bir ikame olarak hizmet edebileceğini gösteriyor.
Yaklaşımın vaatleri ve sınırları
Bu cesaret verici sayılara rağmen yazarlar çalışmalarının kesin sınırları olduğunu vurguluyor. Sadece dört ilaç incelendi ve tüm değerlendirmeler gerçek biyokimyasal deneyler yerine diğer bilgisayar programlarına dayanıyor. DYRK2 proteini ağırlıklı olarak tek boyutlu bir dizgi grafı olarak modellenmiş; tam üç boyutlu yapı olarak değil, bu yüzden model henüz bağlanma cebi gibi ayrıntılı şekilleri hesaba katamıyor. Fiziksel enerji terimleri de basitleştirilmiş; standart kuvvet alanı parametreleri ve kesme değerleri kullanılıyor. Sonuç olarak çalışma bir kavram kanıtı olarak görülmeli: fizik rehberli grafik sinir ağlarının düşük veri koşullarında klasik docking skorlarını yakından izleyebileceğini gösteriyor, ancak tahminlerin deney tüpünde veya klinikte gerçeğe uyduğunu henüz kanıtlamıyor.
Gelecekteki Alzheimer araştırmaları için ne anlama geliyor
Uzman olmayanlar için ana mesaj, fizik‑bilinçli akıllı algoritmaların araştırmacıların DYRK2 gibi yeni Alzheimer hedeflerini geleneksel yöntemlere göre çok daha hızlı keşfetmesine yardımcı olabileceği. Donepezil ve brexpiprazolu umut verici DYRK2 bağlayıcıları olarak öne çıkarıp docking sonuçlarını yaklaşık olarak hesaplamaya şeffaf bir yol sunarak, PhysDual‑GCN daha derin laboratuvar çalışmalarına bir başlangıç noktası sağlıyor. Daha büyük ilaç kütüphaneleri, daha zengin 3B protein bilgisi ve deneysel doğrulama ile bu tür modeller, aday tedavileri taramak ve Alzheimer hastalığının seyrini yavaşlatmaya veya değiştirmeye yönelik ilaç yeniden kullanımı çabalarını yönlendirmek için pratik bir araç haline gelebilir.
Atıf: Gider, V., Budak, C. A physics-informed graph neural network to approximate docking-based binding affinity for DYRK2 in Alzheimer’s drug repurposing. Sci Rep 16, 8357 (2026). https://doi.org/10.1038/s41598-026-35102-7
Anahtar kelimeler: Alzheimer hastalığı, ilaç yeniden kullanımı, grafik sinir ağları, protein–ligand bağlanması, DYRK2 kinazı