Clear Sky Science · tr
NLRP3 inflammasom montajının ligand kaynaklı pirin domaini arayüzlerinin yeniden şekillenmesi yoluyla bozulması
Aşırı iltihabı yatıştırmanın önemi
Artrit ve guttan kalp hastalığına ve nörodejenerasyona kadar birçok kronik hastalık, hücrelerimizin içindeki aşırı aktif bir bağışıklık alarm sistemi tarafından beslenir. Bu alarmın kilit parçalarından biri olan NLRP3 inflammasom, enfeksiyonlarla savaşmamıza yardımcı olur ancak yanlış aktifleştiğinde zararlı iltihaba da yol açabilir. Bu çalışma, NLRP3 aktivasyonunun erken bir adımını hedefleyen ve E9 adını taşıyan yeni bir küçük molekülü tanımlıyor; bu yaklaşım, bağışıklık sistemini tamamen kapatmadan zararlı iltihabı soğutacak ilaç tasarımları için yeni bir açı sunuyor.
Karanlık bir yanı olan hücresel yangın alarmı
Vücudumuz tehlikeyi algıladığında, bağışıklık hücreleri moleküler bir yangın alarmı gibi davranan büyük bir protein kompleksi olan NLRP3 inflammasomu bir araya getirir. Bir kez oluştuğunda, bu yapı kaspaz-1 adlı bir enzimi açığa çıkarır; kaspaz-1 de IL-1β ve IL-18 dahil güçlü iltihapı tetikleyen habercileri aktive eder. Bu sinyaller enfeksiyonlarla savaşmak ve hasarlı dokuları temizlemek için hayati öneme sahiptir. Ancak inflammasom çok uzun süre açık kalırsa ya da yanlış zamanda aktive olursa eklemleri, damarları, beyni ve diğer organları etkileyen kronik inflamatuar durumlara katkıda bulunur. Bu yüzden araştırmacılar dünya genelinde, bağışıklığı geniş biçimde baskılamadan NLRP3'ü hassas biçimde kontrol etmenin yollarını arıyorlar.
Alışılagelmiş ilaç hedeflerinin ötesine bakmak
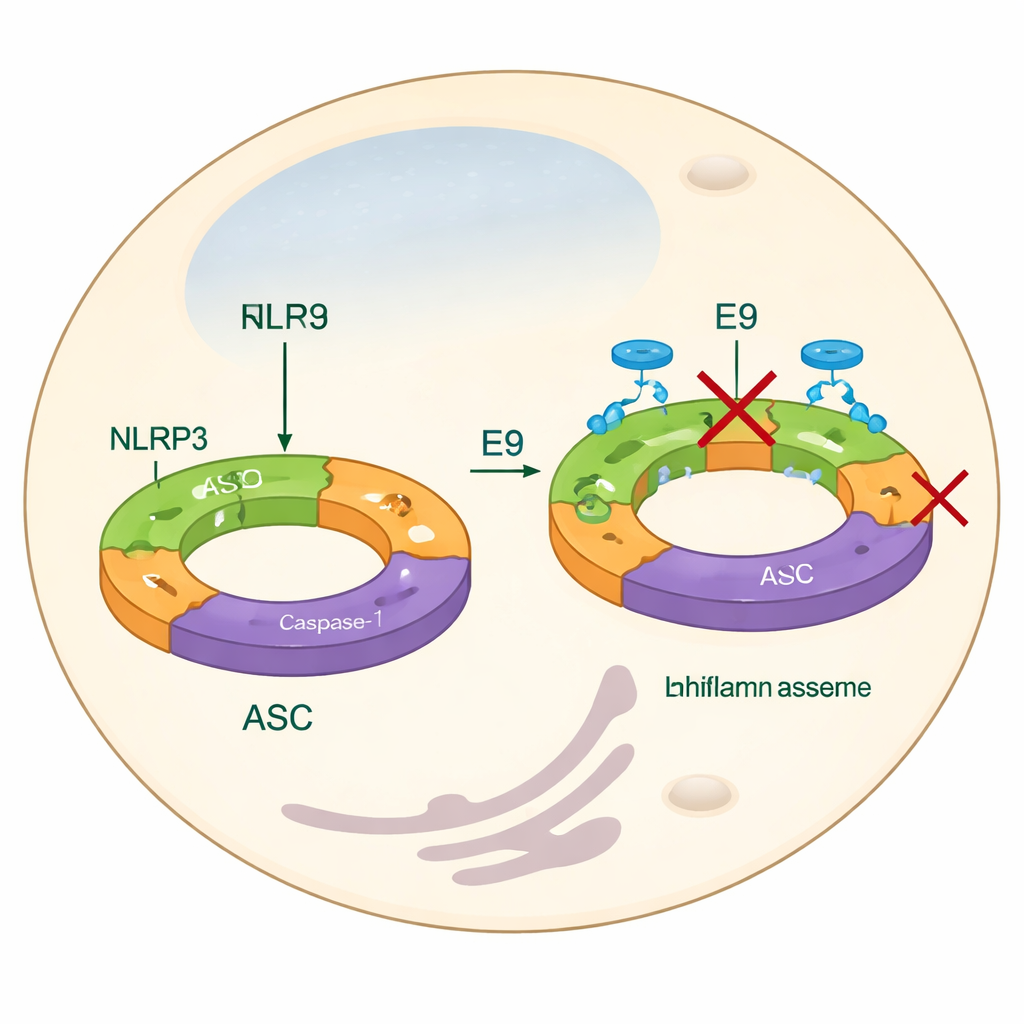
NLRP3’ü yatıştırmak için mevcut yaklaşımların çoğu, IL-1β gibi son ürünleri bloke etmeye veya ATP gibi enerji moleküllerini kullanan merkezi bir motor-gibi domaine müdahale etmeye odaklanır. Bu yaklaşımlar işe yarayabilir, ancak en erken montaj adımlarını gözden kaçırabilir ve NLRP3 proteinlerinin işlevsel bir makine oluşturmak için nasıl bir araya geldiğini tam olarak ele almayabilir. Bu çalışmada araştırmacılar bunun yerine pirin domainine odaklanıyor; bu parça NLRP3 birimlerinin uzun filamentler halinde birbirine tutunmasına yardımcı olur. Bu filamentler daha sonra ASC adı verilen başka bir adaptör proteini toplar; ASC hücre içinde parlak “nokta”lar halinde kümelenir ki bu inflammasom aktivasyonunun görsel bir işaretidir. Pirin domainlerinin düzgün şekilde birbirine uyum sağlamasını engelleyen kimyasallar bularak ekip, inflammasomun baştan oluşmasını önlemeyi hedefliyor.
Zinciri kıran bir molekül bulmak
Araştırmacılar, zekice tasarlanmış bir ışık tabanlı test kullanarak 1500 yeni sentezlenmiş küçük molekülden oluşan bir kütüphaneyi taradılar. NLRP3 pirin domainine bölünmüş luciferaz enzimi parçaları füze edildi; iki pirin domaini bir araya geldiğinde, enzim parçaları yeniden birleşip ışık üretiyordu. Pirin–pirin temasını engelleyen bileşikler ışık sinyalinin azalmasına neden oldu. Bu taramadan dört umut verici aday belirlendi ve bunların arasından E9, güçlü ve tutarlı inhibisyonu ile öne çıktı. Mikroskal termoforez adı verilen bir teknikle yapılan takip ölçümleri, E9’un pirin domainine çok düşük (submikromolar) konsantrasyonlarda sıkı bağlandığını gösterdi; bu da etkinin rastgele bir artefakt olmadığını, spesifik bir etkileşimin sonucu olduğunu doğruladı.
Canlı hücrelerde etkisini görmek
E9’un canlı bir sistemde de işe yarayıp yaramadığını test etmek için ekip, floresan işaretli bir ASC versiyonu üretmek üzere mühendislik yapılan insan bağışıklık-benzeri hücreleri kullandı. Bu hücreler bakteriyel bileşenler ve ikinci bir tetikleyici ile uyarıldığında NLRP3 aktive olur ve ASC proteinleri mikroskop altında sayılabilen parlak noktalarda kümelenir. E9 varlığında bu noktaların sayısı belirgin şekilde düştü; bazı bilinen NLRP3 bloke edicilerle karşılaştırılabilir veya daha iyiydi. Bu, pirin domaini temaslarına müdahale etmenin, en azından laboratuvar koşullarında, inflammasom montajını ve iltihaplı hücre ölümünün erken adımlarını azaltmak için yeterli olduğunu gösterdi.
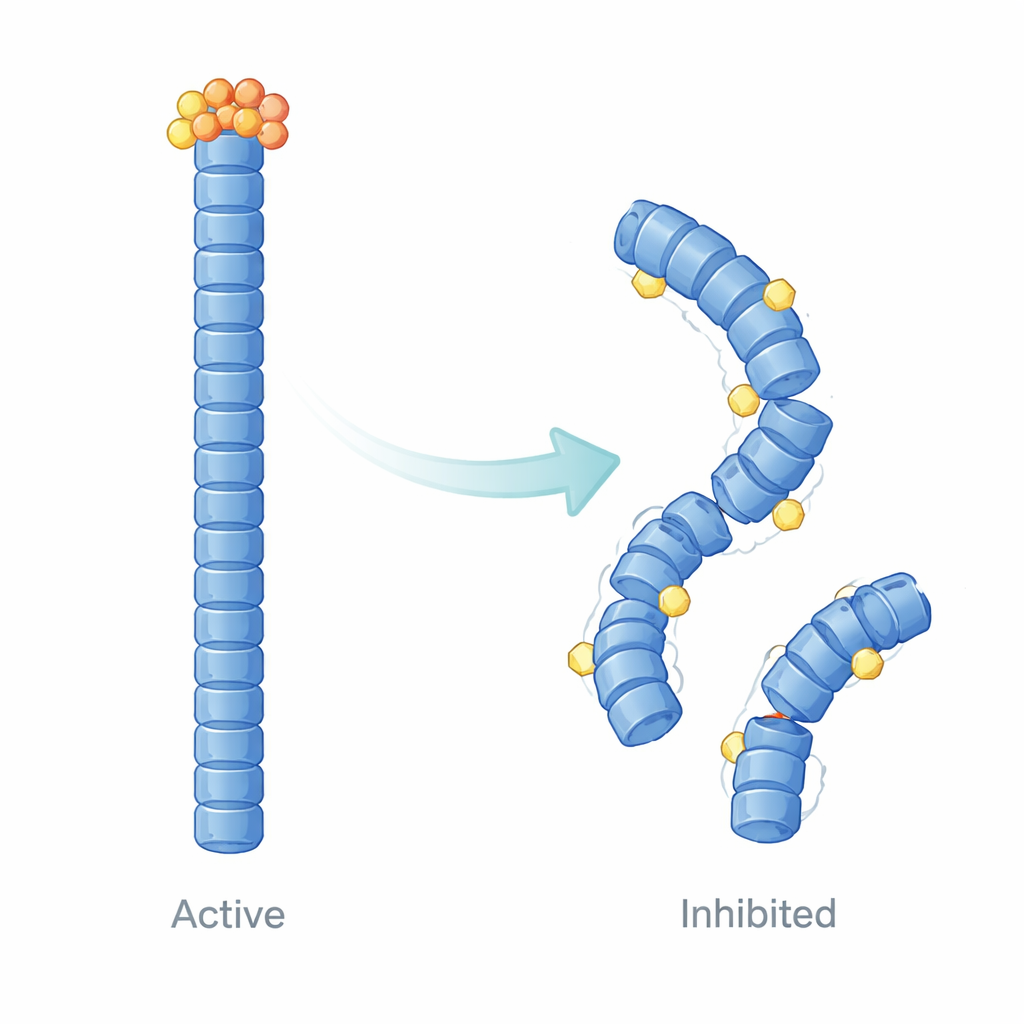
E9 inflammasom iskeletini nasıl yeniden şekillendiriyor
Yalnızca bağlanmayı ölçmenin ötesinde, yazarlar E9’un NLRP3 filamentlerinin davranışını zaman içinde nasıl değiştirdiğini görselleştirmek için bilgisayar tabanlı yapısal modelleme ve moleküler dinamik simülasyonlar kullandılar. Hesaplamaları E9’un pirin domainlerinin temas ettiği belirli yüzeylere yerleştiğini ve filamentleri ince bir şekilde gevşetip yeniden şekillendirdiğini öne sürüyor. Birbirine uyumlu, kararlı bir yapı yerine filament düzensiz hale geliyor: E9’un bağlandığı yakın bölgeler daha esnek oluyor ve hassas hizalanmayı kaybederken diğer kısımlar dinamik olarak izole hale geliyor. Bu değişimler, etkili ASC toplanması için gereken büyük ölçekli hareketleri ve sıkı iletişimi zayıflatıyor; hücrelerde gözlenen azalmış nokta oluşumuna böylece fiziksel bir açıklama sunuyor.
Gelecekteki tedaviler için taşıdığı anlam
Bu bulgular bir araya getirildiğinde, E9’u NLRP3 yapı taşları arasındaki arayüzleri bozarak etkili olan yeni bir inflammasom hedefli ilaç sınıfı için bir prototip olarak konumlandırıyor. Mevcut çalışma tüp deneyleri, bilgisayar simülasyonları ve kültürlenmiş hücrelerle sınırlı olmasına ve hayvanlar ile insanlarda ek çalışmalara ihtiyaç duyulmasına rağmen, özenle tasarlanmış küçük moleküllerin inflammasom iskeletini kendisini yeniden şekillendirebileceğini gösteriyor. Kontrolden çıkmış iltihap tarafından tetiklenen hastalığı olan hastalar için bu tür arayüz-odaklı ilaçlar bir gün zararlı bağışıklık aktivasyonunu kısmen azaltırken gerekli savunmaları büyük ölçüde koruyarak daha hassas kontrol sunabilir.
Atıf: Khosravifard, S., Hosseinkhani, S., Bakhtiary, N. et al. Disruption of NLRP3 inflammasome assembly via ligand-induced remodeling of pyrin domain interfaces. Sci Rep 16, 4951 (2026). https://doi.org/10.1038/s41598-026-35050-2
Anahtar kelimeler: NLRP3 inflammasom, pirin domaini, küçük molekül inhibitör, doğuştan gelen bağışıklık, pyroptoz