Clear Sky Science · tr
Sarkopeni hastalarının iskelet kaslarında anormal alternatif ekleme olaylarının transkriptomik karakterizasyonu
Yaşlanan kaslar neden güçlerini yitirir
Sarkopeni—yaşla birlikte kas kütlesi ve gücünün kademeli kaybı—yaşlı yetişkinlerin merdiven çıkmak veya market torbası taşımak gibi günlük işleri zorlaştırmasının başlıca nedenlerinden biridir. Bu çalışma, kas içinde RNA düzeyinde, hücrelere hangi proteinleri yapacaklarını söyleyen mesajlarda derinlemesine inceleme yapıyor. Yazarlar, sarkopenide bu RNA mesajlarının birçok kez anormal biçimde kesilip birleştirildiğini gösteriyor; bu durum kaslarda enerji üretimini bozabilir ve yeni tedavi hedeflerini işaret edebilir.
Kas kaybı ve vücudun gen “düzenleme” sistemi
Genlerimiz DNA'da yazılıdır, fakat hücreler bu genlerin RNA kopyalarından çalışır. Bir RNA mesajı kullanılmadan önce hücreler onu normalde bir filmi düzenler gibi kırpar ve ekler—böylece tek bir gen birden çok protein versiyonu üretebilir. Alternatif ekleme (alternative splicing) adı verilen bu süreç kasta özellikle aktiftir; kasın kasılmak, onarmak ve egzersize uyum sağlamak için hassas ayarlanmış proteinlere ihtiyacı vardır. Ekleme yanlış gittiğinde yanlış protein versiyonları üretilebilir veya önemli olanlar kaybolabilir; bu durum kas distrofisi ve bazı beyin hastalıkları gibi bozukluklara katkıda bulunur. Yazarlar, benzer bir gizli RNA yanlış düzenlemesinin sarkopeniye yol açıyor olabileceğinden şüphelenmişlerdi.
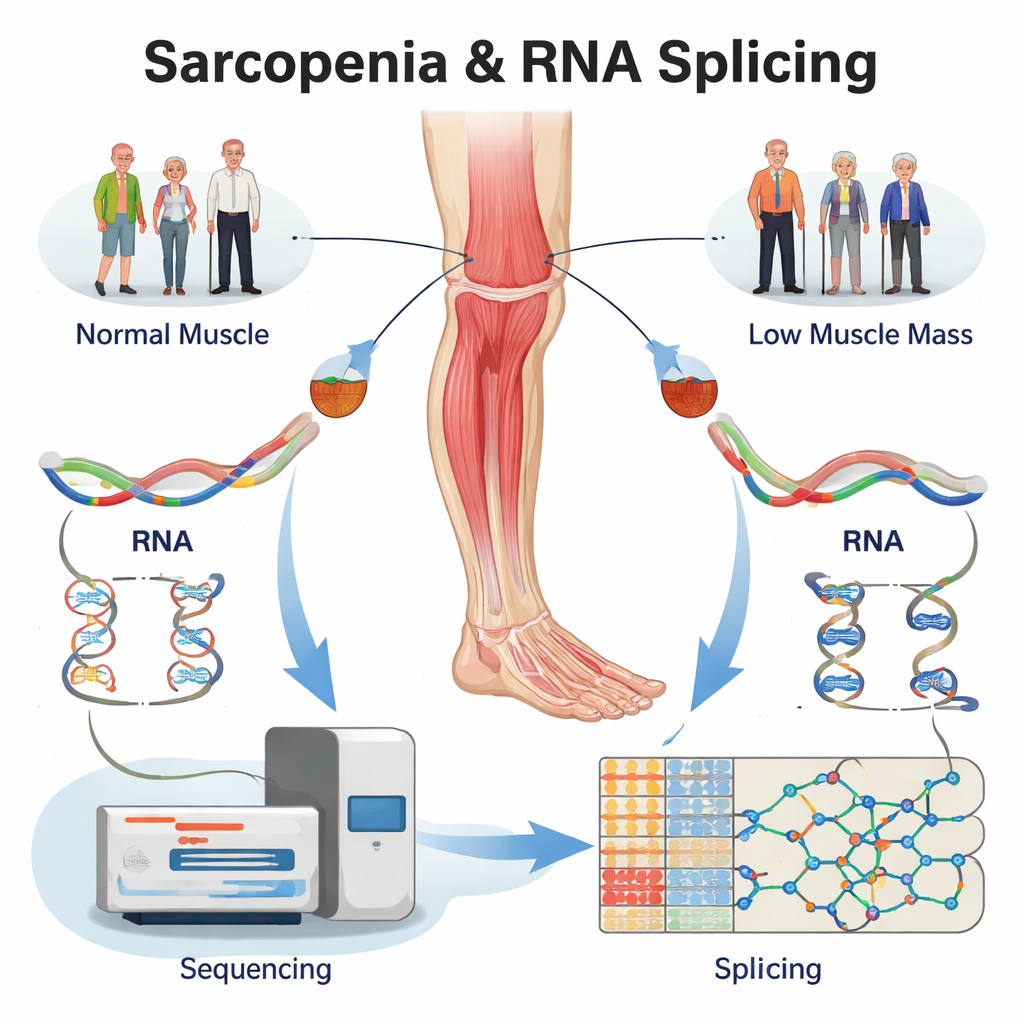
Gizli RNA hatalarını bulmak için mevcut veriyi yeniden okumak
Yeni gönüllüler toplamaktansa ekip, insan uyluk kası biyopsilerinden elde edilmiş büyük bir RNA dizileme veri setini yeniden analiz etti. Örnekler dört gruptan geliyordu: tam gelişmiş sarkopenisi olan yaşlı yetişkinler, yalnızca düşük kas kütlesi olanlar, yalnızca düşük kas gücü olanlar ve yaşça eşleştirilmiş sağlıklı kontroller. Uzman yazılımlar kullanarak önce hastalıklı kaslarda yüzlerce genin ifade düzeyinin artıp azaldığını doğruladılar. Daha da önemlisi, ardından her bir genin RNA'sının nasıl eklemlendiğine baktılar ve sağlıklı kasla karşılaştırıldığında üç problem grubunda 5.000'den fazla ekleme değişikliğini katalogladılar. Bu değişiklikler birkaç temel tipte yoğunlaşıyordu—örneğin bir eksonun atlanması veya alternatif kesim yerinin seçilmesi—protein yapısını güçlü biçimde değiştirdiği bilinen desenler.
Enerji fabrikaları ve hücrenin “yakıt göstergesi” yolları bozuluyor
Ekleme değişiklikleri kas biyolojisinin merkezindeki genlerde ortaya çıktı. Etkilenen birçok gen mitokondrileri, yani kas kasılmasını sağlayan küçük enerji fabrikalarını oluşturan parçalara aitti. Sarkopenik kaslarda, besinleri kullanılabilir enerjiye çeviren oksidatif fosforilasyon sürecine dahil 16 genin eklemesinde değişiklik gözlendi; özellikle elektron taşıma ve proton pompalama işlevlerini üstlenen mitokondri komplekslerinin bileşenlerinde. Diğer değişiklikler, hücresel enerji ve onarım için anahtar bir molekül olan NAD⁺ üreten veya kullanan genlerde görünüyordu. CD38, PARP2 ve birkaç sirtuin gibi önemli enzimler yalnızca miktar olarak değişmiyordu; farklı RNA varyantları üretiyorlardı; bu da NAD⁺ üretimi ile tüketimi arasındaki dengenin ekleme düzeyinde bozulduğunu düşündürüyor. Etkilenen genler ayrıca AMPK ve FoxO yolları da dahil olmak üzere iyi bilinen kas sinyal yollarında kümeleniyordu; bu yollar hücresel yakıt göstergeleri ve stres yanıtlayıcıları gibi davranır.
Farklı evrelerde ve türler arasında paylaşılan desenler
Çarpıcı biçimde, aynı genlerin birçoğu yalnızca tam sarkopenisi olan insanlarda değil, aynı zamanda yalnızca düşük kas kütlesi veya yalnızca düşük güç sahibi olanlarda da ekleme değişiklikleri gösterdi. Bu, anormal eklemenin erken başladığını ve hastalığın farklı klinik görünümlerini kestiğini öne sürüyor. Bu değişikliklerin bir hayvan modelinde tekrar üretilebilir olup olmadığını test etmek için araştırmacılar, kas erimesini taklit etmek üzere steroid deksametazon ile farelerde kas zayıflığı indüklediler; bu, sarkopeninin bazı özelliklerini taklit etmenin standart bir yoludur. Fareler zayıf kavrama gücü ve koşu ile denge testlerinde daha kötü performans geliştirdi. Ekip fare kası RNA'sını dizilediğinde yine yüzlerce genin eklemesinin değiştiğini buldular. Bunların yaklaşık beşte biri insan sarkopeni genleriyle örtüşüyordu ve birçoğu transkripsiyon, kromatin yapısı ve ekleme mekanizmasının kendisini kontrol eden genlerle ilgiliydi—bir hücrenin tüm protein çıktısını yeniden şekillendirebilecek daha üst düzey anahtarlar.
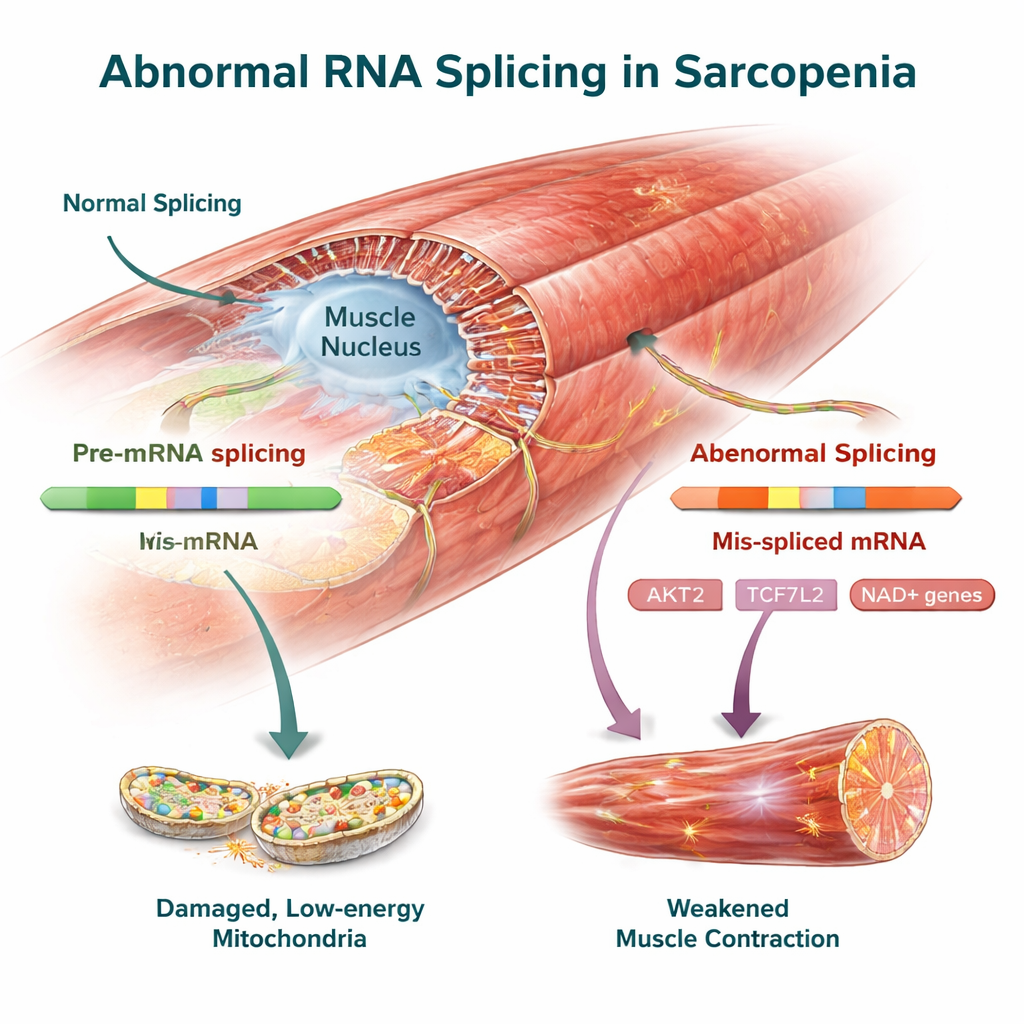
Tedavi hedefi olabilecek temel kas kontrol genleri
Türler arası değişiklikler arasında kas sağlığıyla daha önce ilişkilendirilmiş birkaç gen vardı. AKT2, kasta büyüme ve protein inşasını düzenleyen merkezi bir faktör, hem insanlarda hem de farelerde kas kütlesini koruma yeteneğini zayıflatabilecek belirgin ekleme değişiklikleri gösterdi. Wnt sinyal yolunun bir parçası olan TCF7L2 ile kasın iç iskeletini ve protein kalite kontrolünü organize etmeye yardımcı olan FMNL2 ve USP40 da değişmiş RNA varyantlarına sahipti. Ekip bu ekleme değişikliklerini fare kasında deneysel olarak doğruladı; bu da bunların veri analizinin bir yan ürünü değil, hastalığın gerçek özellikleri olduğuna dair kanıtı güçlendiriyor.
Kırılganlığı önleme açısından bunun anlamı
Uzman olmayanlar için mesaj şu: sarkopeni sadece kasların “aşınması” veya genlerin açık/kapalı olması meselesi değil. Ayrıca, kas hücrelerinin makinelerini nasıl yapıp sürdüreceğini yönlendiren RNA mesajlarının yaygın bir yanlış düzenlenmesi söz konusu; özellikle enerji üreten sistemler ve stres algılama mekanizmaları etkileniyor. Eklenmenin prensipte hassas tasarlanmış RNA bazlı ilaçlarla düzeltilebilmesi nedeniyle, burada keşfedilen korunmuş ekleme hataları—özellikle AKT2 ve TCF7L2 gibi genlerde—yaşlanan kasların daha uzun süre güçlü kalmasına yardımcı olacak terapilere yönelik yeni yollar sunuyor.
Atıf: Li, Y., Guo, X., Li, S. et al. Transcriptomic characterization of the aberrant alternative splicing in skeletal muscles of sarcopenia patients. Sci Rep 16, 5334 (2026). https://doi.org/10.1038/s41598-026-35002-w
Anahtar kelimeler: sarkopeni, kas yaşlanması, RNA eklenmesi, mitokondri, AKT2