Clear Sky Science · tr
Transtiretin stabilizasyonunun fenomenolojik modeli
Hastalar ve aileler için bunun önemi
Transtiretin amiloidozu, normal bir kan proteini olan transtiretinin (TTR) parçalanıp kalp ve sinirlerde zararlı birikintiler oluşturabildiği ciddi bir durumdur. Tafamidis ve acoramidis gibi yeni ilaçlar bu proteini güvenli, dört parçalı (tetramer) şeklinde tutmak üzere tasarlanmıştır ve birçok kişide sonuçları iyileştirmişlerdir. Yine de hekimler tedavi gören hastalarda şaşırtıcı bir etki gözlemliyor: kan TTR düzeyleri %30’dan fazla artıyor ve bunun nedeni açık değil. Bu makale, vücutta neler olup bittiğini ve bu ilaçların gerçekten nasıl çalıştığını sorgulamak için sadeleştirilmiş, matematik temelli bir model kullanıyor. 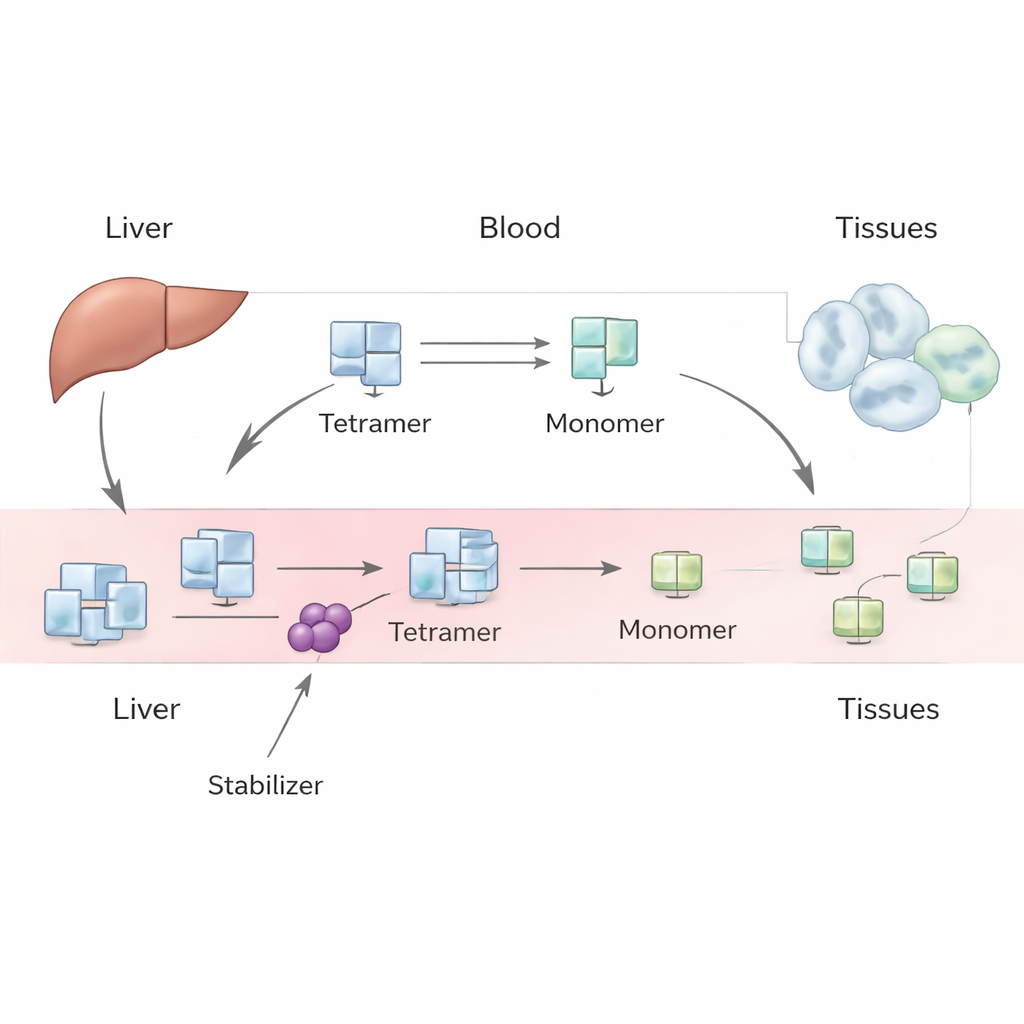
Yardımcı veya zararlı olabilen bir protein
TTR ağırlıklı olarak karaciğerde üretilir ve normalde dört özdeş alt birimin stabil bir demeti (tetramer) olarak kanda dolaşır. Tiroid hormonu ve A vitaminini taşır. Yaşlanma veya kalıtsal gen varyantları gibi bazı koşullarda bu tetramerler tek alt birimlere (monomerlere) ayrılabilir. Bu monomerler yanlış katlanıp amiloid fibriller halinde birbirine yapışabilir; bu dokulara zarar vererek transtiretin amiloidozuna bağlı kalp hastalığı (kardiyomiyopati) veya sinir hasarı (nöropati) oluşturur. Tafamidis ve acoramidis gibi ilaçlar tetramerlere bağlanıp onların parçalanmasını zorlaştıracak şekilde tasarlanmıştır; böylece hastalık ilerlemesi yavaşlar. Ancak hastalar bu ilaçlara başladığında, kanda ölçülen TTR düzeyleri güvenilir biçimde artmakta ve bu artış basit laboratuvar deneylerinin öngördüğünden daha büyüktür.
Karmaşık bir sistemin basit bir resmi
Yazarlar bu bilmeceyi, her mikroskobik detaya odaklanmak yerine tümüyle gözlemlenebilir davranışa yoğunlaşan bir fenomenolojik modelle ele alıyor. Çerçevelerinde karaciğer sabit bir hızla TTR tetrameri üretir ve bunlar kana girer. Dolaşımda tetramerler monomerlere ayrılabilir ve yeniden birleşebilir; hem tetramerler hem de monomerler dokuya alınma ve parçalanma yoluyla kandan uzaklaştırılabilir. Tetramerler ve monomerler için kütle dengesi denklemlerinin ikisini yazarak ekip farklı senaryoları inceliyor: monomerlerin çoğunlukla tekrar tetramere katıldığı bir durum; hızlıca uzaklaştırıldıkları bir durum; ve her iki sürecin de önemli olduğu bir ara durum. Tarihsel insan izleyici (tracer) çalışmaları ve modern laboratuvar verilerini kullanarak tetramerlerin ne kadar hızlı temizlendiği, ne kadar çabuk parçalandığı ve ilaçların bu ayrışmayı ne kadar yavaşlattığı gibi kilit nicelikleri tahmin ediyorlar.
Sadece tetramer stabilizasyonu yeterli değil
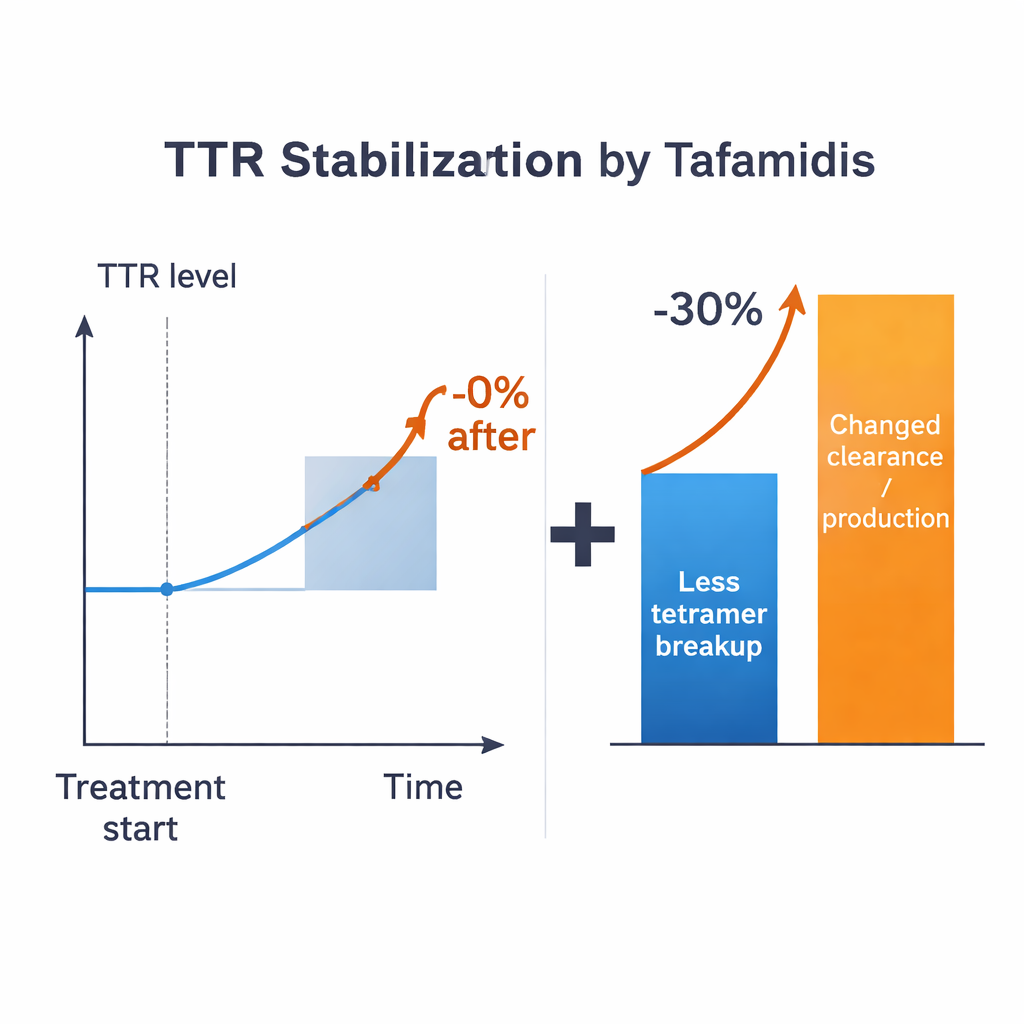
Bu tahminlerle araştırmacılar doğrudan bir soru soruyor: bir ilaç tetramerlerin tamamen parçalanmasını kesin olarak engelleyebilse, kanda TTR düzeyi ne kadar artardı? Tüm makul rejimler boyunca cevap ılımlı çıkıyor—tipik parametre değerleri için en fazla yaklaşık %15 düzeyinde ve monomerlerin nasıl işlendiğine bağlı olarak genellikle daha az. Bu, tedavi edilen hastalarda gözlenen %30’un üzerindeki artışın çok altında kalıyor. Bilinen parametrelerde cömert belirsizliklere izin verilse bile uyumsuzluk sürüyor. Model bu yüzden yalnızca tetramer ayrışmasını yavaşlatmanın klinik etkinin tamamını açıklayamayacağını öne sürüyor. TTR üretimini, hücrelerce alınmasını veya parçalanmasını kontrol eden diğer süreçlerin de stabilizatör ilaçlar var olduğunda değişmesi gerekiyor.
İlaç düzeyleri ve akıllıca deneylerden gelen ipuçları
İlaç maruziyetini TTR davranışına bağlamak için yazarlar, tafamidisin temel bir farmakokinetik modeliyle (ilaç vücutta zamana göre nasıl hareket eder) özel “alt birim değişimi” analizlerini birleştiriyor. Bu deneylerde işaretli ve işaretsiz TTR tetramerleri insan plazmasında karıştırılır ve alt birimlerin kademeli değişimi, tetramerlerin ne sıklıkla ayrıldığını ortaya koyar. Bu sürecin farklı ilaç konsantrasyonlarında ölçülmesi, tafamidis düzeyi ile efektif tetramer stabilitesi arasında doğrudan, veri odaklı bir bağlantı sağlar; albümin veya tiroid hormonu ile ne kadar ilacın bağlı olduğunun bilinmesine ihtiyaç bırakmaz. Bu fenomenolojik bağlantı modele girer ve birçok biyokimyasal bilinmezi temiz biçimde atlatır. Yine de bu avantajla bile hesaplamalar TTR’de beklenen artışı klinikte gözlemlenen artışın yaklaşık yarısıyla sınırlıyor; bu da temizleme, hücre içi alım, yıkım veya sentezdeki değişikliklerin hikâyenin bir parçası olması gerektiği fikrini güçlendiriyor.
İleriye dönük ne anlama geliyor
Uzman olmayanlar için temel mesaj şudur: bu stabilizatör ilaçlar muhtemelen yalnızca TTR tetramerlerini “yapıştırmaktan” daha fazlasını yapıyor. Büyük olasılıkla vücudun proteini üretme, uzaklaştırma veya geri dönüştürme biçimini de etkiliyorlar. Yazarlar, kendi gibi basit ve şeffaf modellerin, anlayışımızdaki bu tür boşlukları açığa çıkardıklarından ve doğrudan deneylere işaret ettiklerinden güçlü olduğunu savunuyor—örneğin monomerlerin ne kadar hızlı temizlendiğini doğrudan ölçmek, farklı TTR formlarının hücrelerce ne kadar çabuk alındığını belirlemek veya ilaç-bağlı TTR’nin bağsız proteinden farklı şekilde işlenip işlenmediğini test etmek. Bu sorulara daha iyi yanıtlar yalnızca transtiretin amiloidozu tedavisini rafine etmekle kalmayacak, normal proteinlerin zararlı agregalara dönüştüğü diğer hastalıklar hakkında da genel kurallar ortaya çıkarabilir.
Atıf: Lisowski, B., Ulaszek, S., Wiśniowska, B. et al. Phenomenological model of transthyretin stabilization. Sci Rep 16, 4904 (2026). https://doi.org/10.1038/s41598-026-35000-y
Anahtar kelimeler: transtiretin amiloidozu, protein stabilizasyonu, tafamidis, farmakokinetik modelleme, amiloid hastalıkları