Clear Sky Science · tr
Salinomisin kaynaklı hücre ölümünde otofaji ile p38 MAPK arasındaki etkileşim, sisplatin dirençli melanomda
Bu araştırma neden önemli
Melanom, cilt kanserlerinin en ölümcül biçimlerinden biridir; bunun bir nedeni tümörlerin sıklıkla sisplatin gibi standart kemoterapi ilaçlarına karşı direnç geliştirmesidir. Bu çalışma, sıra dışı bir antibiyotik olan salinomisinin bu direnci aşıp aşamayacağını araştırıyor ve ilacın nasıl işlediğini anlamak için hücrenin kendi geri dönüşüm ve stres yanıtı sistemlerini inceliyor. Tedavi sonrasında bazı kanserlerin neden geri döndüğü ve bunları nasıl alt edebileceğimizle ilgilenen herkes için bu çalışma, tümör hücreleri içinde gerçekleşen hayati kararların perde arkasına dair bir pencere sunuyor.
Kanser hücreleri tedaviyi dinlemeyi kestiğinde
Sisplatin, birçok solid tümöre karşı kullanılan etkili bir ilaçtır, ancak melanom hücreleri sıkça uyum sağlayarak öldürülmesi zor hale gelir. Araştırmacılar, sisplatin direnci kazanmış bir fare melanom hücre hattı oluşturdu ve üzerine salinomisini test ettiler. Kültürde, artan salinomisin dozları canlı melanom hücresi sayısını keskin şekilde azalttı, programlı hücre ölümüne ait klasik belirtileri tetikledi ve kısa maruziyetten sonra bile yeni koloni oluşturma yeteneğini yok etti. Sisplatine dirençli melanom tümörleri taşıyan farelerde salinomisin enjeksiyonları büyümeyi dramatik şekilde yavaşlattı, tümör hacmini ve ağırlığını belirgin şekilde azalttı; belirgin toksisite gözlenmedi. Birlikte ele alındığında, bu sonuçlar salinomisinin standart kemoterapiye yanıt vermeyen melanom hücrelerini hedefleyebileceğini düşündürüyor. 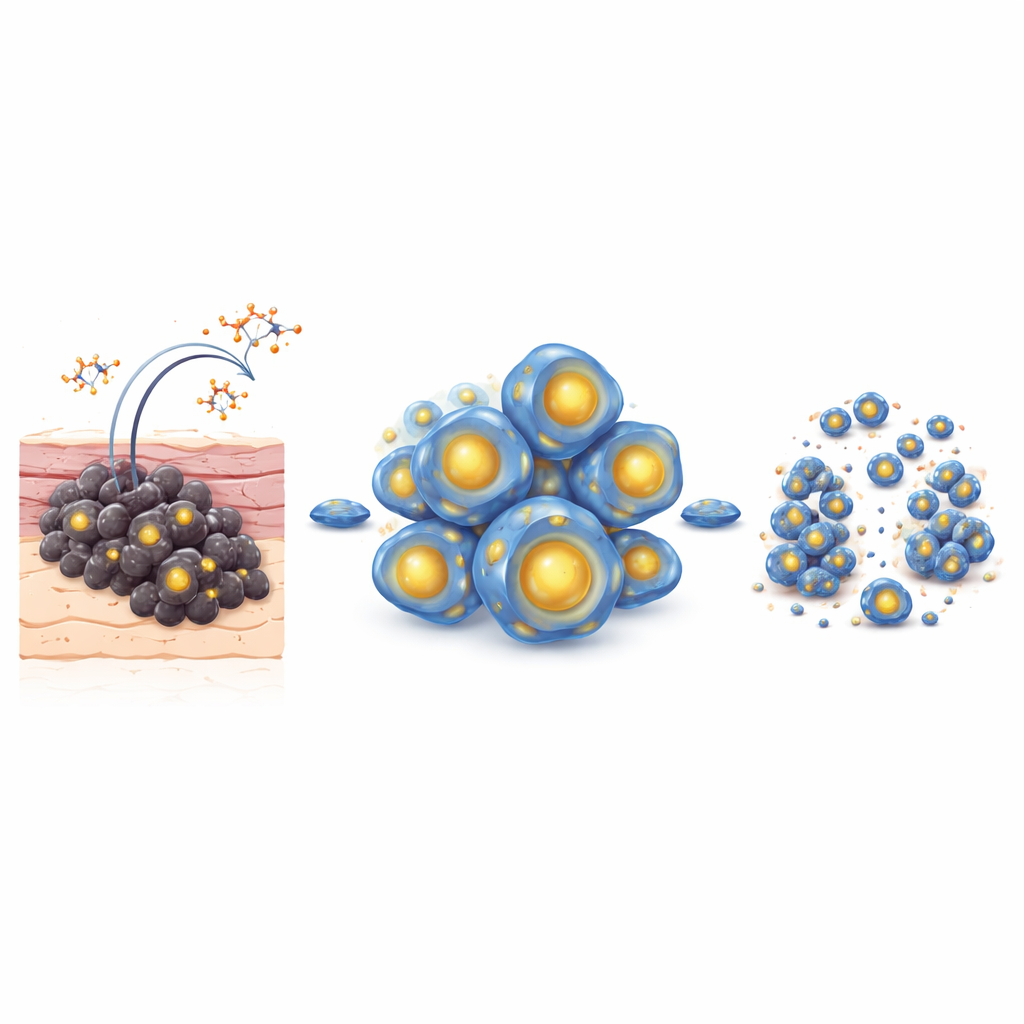
Hücre stresi, kalsiyum dalgaları ve zorlanan bir geri dönüşüm sistemi
Salinomisinin hücre içinde ne yaptığını öğrenmek için ekip endoplazmik retikulum üzerine odaklandı; bu organel yeni proteinlerin katlanmasına ve işlenmesine yardımcı olan bir membran labirentidir. Salinomisin iyon taşıyıcısı gibi davranır ve membranlar arasındaki yüklü parçacık akışını bozar; bu da bu organelin işlevinin aksamasına yol açabilir. Araştırmacılar, hücrenin protein katlama makinesinin zorlandığını gösteren protein belirteçlerinde güçlü bir aktivasyon gözledi. Aynı zamanda endoplazmik retikulumdan hücre dış sıvısına ve mitokondrilere doğru sızan bir kalsiyum dalgası tespit ettiler. Mitokondrilerin bu kalsiyumu almasını engellediklerinde hücreler daha kolay öldü; bu, mitokondrilerin normalde salinomisin stresine karşı ölümü geciktiren bir tampon görevi gördüğünü düşündürüyor.
Öztemizlik ölümcül bir trafik sıkışmasına dönüşüyor
Hücreler zorlu koşullarda hayatta kalmak için sıkça “öz‑yeme” olarak tanımlanan bir sürece güvenirler: hasarlı materyali küçük keseciklere sarar ve bunları asidik bölmelere göndererek parçalar ve geri dönüştürürler. Salinomisin, bu yolun erken adımlarını güçlü şekilde artırdı ve bu keseciklerin oluşumunu yönlendiren protein seviyelerini yükseltti. Ancak önemli bir nokta, ekip tarafından bulunan son temizleme adımının bozulmuş olmasıydı. Parçalanması gereken belirteçler birikmiş, mikroskopik görüntüler lizozomlarla düzgün şekilde füzyona girmeyen büyük vakuol benzeri yapılar gösteriyordu. İleri testler lizozomal membranların sızdırdığını ve bazı sindirim enzimlerinin yanlış yerde aktive olduğunu ortaya koydu. Sonuç, hücresel bir trafik sıkışması: geri dönüşüm paketleri oluşmaya devam ediyor ama verimli şekilde temizlenmiyor; bu da normalde koruyucu olan bir süreci hücre ölümünü tetikleyen bir mekanizmaya çevirebiliyor.
Tümöre karşı çevrilebilecek bir stres sinyal anahtarı
Bulmacanın bir diğer parçası, topluca MAP kinazlar olarak bilinen stres algılayıcı enzim ailesidir. Salinomisin bu sistemin üç kolunu da aktive etti, ancak özellikle p38 adı verilen bir kol öne çıktı. Araştırmacılar p38’i engellediklerinde, salinomisin çok daha fazla melanom hücresi öldürdü ve sitoplazmik vakuollerin sayısında ve büyüklüğünde çarpıcı bir artışa yol açtı. Kalsiyuma bağımlı bir enzim olan kalpain’i engellemek benzer etkiyi gösterdi; hem vakuol birikimi hem de uzun vadeli hayatta kalma üzerinde. Buna karşılık, daha verimli bir öz‑temizliği teşvik eden bir ilaç (rapamisin) geri dönüşüm keseciklerinin zararlı birikimini azalttı ve hücreleri salinomisinden korudu. Bu deneyler, salinomisin stresi altında p38 ve kalpain’in melanom hücrelerinin yavaşlatılmış, kusurlu bir geri dönüşüm yanıtını hayatta kalma taktiği olarak kullanmasına yardımcı olduğunu ve bu yedeği devre dışı bırakmanın ilacı daha öldürücü kıldığını öne sürüyor. 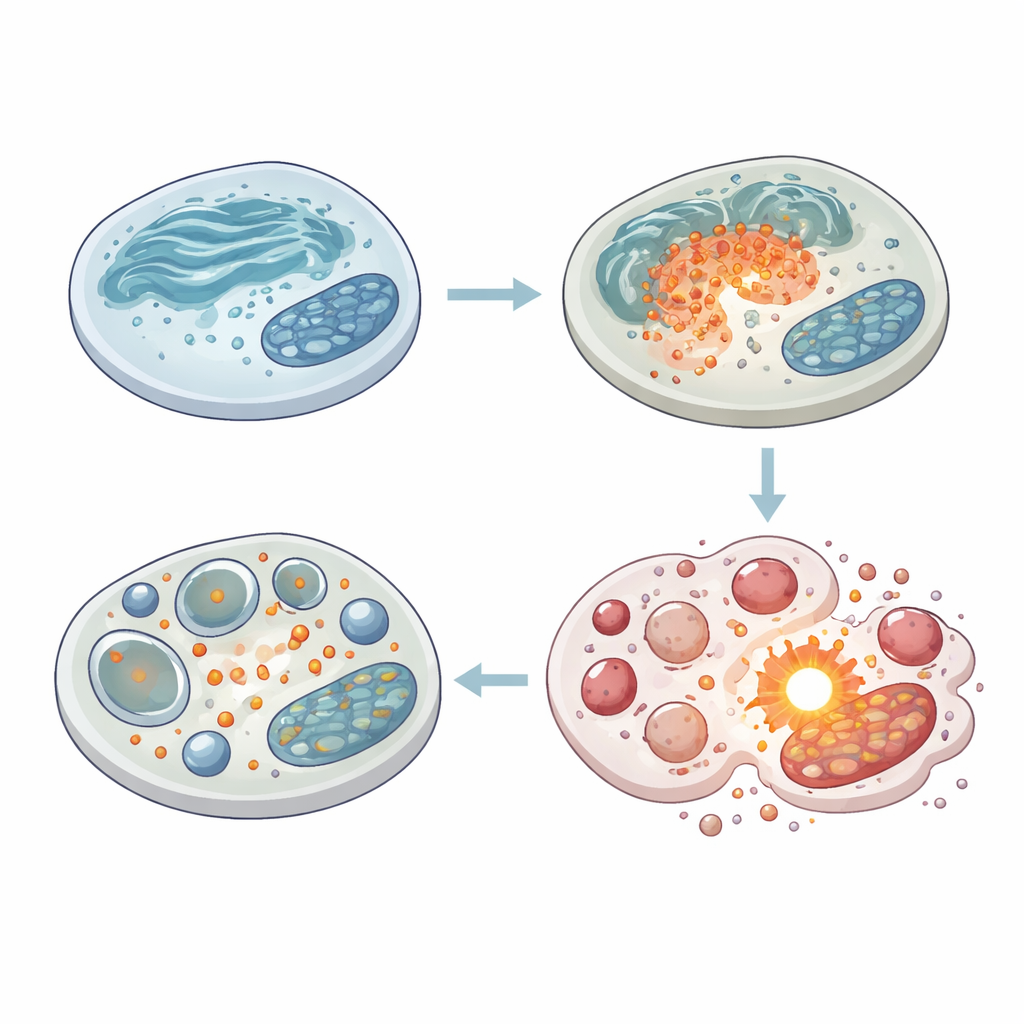
Gelecekteki kanser bakımına ne ifade edebilir
Genel olarak çalışma, salinomisini çift taraflı bir ajan olarak betimliyor: sisplatin‑dirençli melanom hücrelerini şiddetli iç stres altına sokuyor, onları kalsiyumla dolduruyor, atık işleme sistemlerini tıkıyor ve nihayetinde programlı hücre ölümüne yönlendiriyor. Aynı zamanda hücreler p38 yönlendirmeli bir geri dönüşüm yanıtı ve diğer hayatta kalma yollarını kullanarak kendilerini savunmaya çalışıyor. Hastalar için pratik mesaj, salinomisin veya ona benzer geliştirilmiş bileşenlerin bir gün bu hayatta kalma yollarını bloke eden ilaçlarla —örneğin p38 inhibitörleri veya otofaji bloke edicilerle— eşleştirilerek inatçı melanom hücrelerini seçici olarak ortadan kaldırmak için her bir ilacın daha düşük dozlarının kullanılmasını sağlayabileceğidir. Bu strateji kliniğe ulaşmadan önce hâlâ çok çalışma gerekse de, çalışma kombinasyon terapilerinin hedefleyebileceği açıklıkları ayrıntılı bir şekilde ortaya koyan bir yol haritası sunuyor.
Atıf: Tyagi, M., Patro, B.S. Interplay between autophagy and p38 MAPK during salinomycin-induced cell death in cisplatin-resistant melanoma. Sci Rep 16, 9640 (2026). https://doi.org/10.1038/s41598-025-34796-5
Anahtar kelimeler: melanom, ilaç direnci, salinomisin, otofaji, kombinasyon tedavisi