Clear Sky Science · tr
İnek kumulus-oosit komplekslerinin in vitro olgunlaşması sırasında hedeflenmiş hipoksi-indüklenebilir faktör 1-alfa (HIF1A) stabilizasyonu blastosist oranlarını artırır
Yumurtalarda oksijen algısını ayarlamanın önemi
Modern sığır yetiştiriciliği laboratuvarda üretilen embriyolara büyük ölçüde dayanır, ancak başarı garanti değildir: oositlerin yalnızca yaklaşık üçte biri transfer için hazır oldukları kritik blastosist aşamasına ulaşır. Bu çalışma, hayvancılık ve yardımcı üreme teknikleri açısından geniş öneme sahip, aldatıcı derecede basit bir soruyu irdeliyor: yumurtaların ovaryum içinde doğal olarak deneyimlediği düşük oksijen koşullarını—ana oksijen algılayıcı proteini nazikçe güçlendirerek—daha yakından taklit edersek, daha fazla embriyonun başarılı şekilde gelişmesine yardımcı olabilir miyiz?
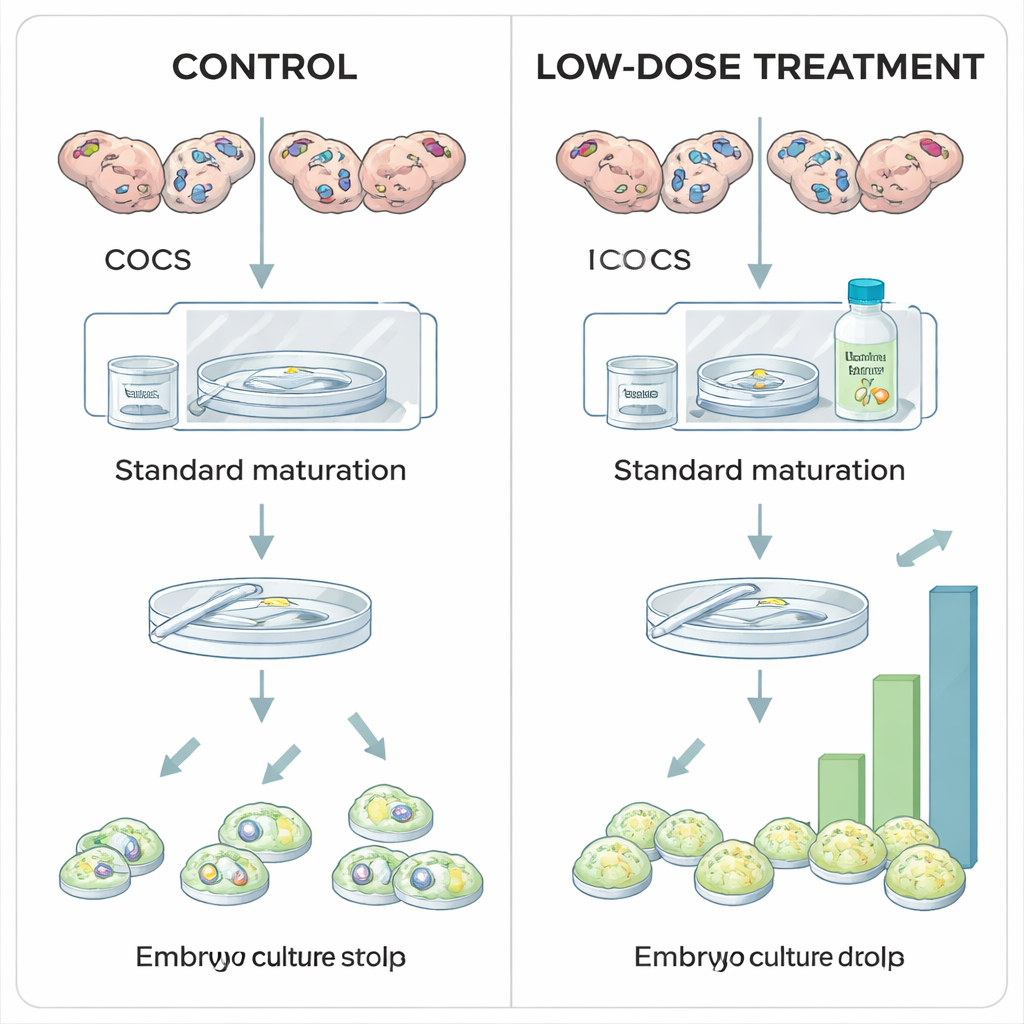
Hayat düşük oksijenli bir nişte başlar
Over içinde, her gelişen oosit etrafında kumulus adı verilen destekleyici hücre kümesi ile çevrilidir ve birlikte kumulus–oosit kompleksini oluştururlar. Foliküller büyüdükçe over daha fazla kanla beslenir hale gelse de, kan damarları oositin hemen çevresine ulaşmaz. Oksijenin difüze olması gerekir ve bu da olgunlaşan oositin etrafında hafifçe düşük oksijenli, yani hipoksik bir cep oluşturur. Bu niş içinde HIF1A adı verilen hücresel bir sensör, hücrelerin metabolizmayı ve hormon üretimini ayarlayarak uyum sağlamasına yardımcı olur. Önceki çalışmalar HIF1A’yı engellemenin oosit olgunlaşmasına zarar verdiğini ve embriyo oluşumunu büyük ölçüde azalttığını gösterdi; bu da bu proteini döllenme ve sağlıklı embriyo gelişimi için oosit yeterliliğinin (kompetansı) merkezi düzenleyicilerinden biri olarak öne çıkarır.
Yumurtanın oksijen sensörünü bir ilaçla ince ayarlamak
Araştırmacılar, boğanın oositlerinin laboratuvarda olgunlaştırılması sırasında HIF1A’yı ılımlı şekilde stabilize etmenin embriyo verimini artırıp artırmayacağını inceledi. Standart in vitro protokollerde kumulus–oosit kompleksleri büyük ölçüde pratik nedenlerle normal hava oksijen seviyelerinde olgunlaştırılır. Burada, kesimhane overlerinden toplanan oositler gruplara ayrıldı ve 24 saatlik olgunlaşma süresince farklı dozlarda Roxadustat adlı bir ilaca maruz bırakıldı; Roxadustat insan tıbbında anemi tedavisinde kullanılan bir ilaçtır. Roxadustat, HIF1A’yı oksijen bolken normalde yok edilmesi için etiketleyen prolin hidroksilazlar (PHD'ler) ailesini bloke ederek çalışır. PHD’leri inhibe ederek Roxadustat, HIF1A proteinine yüksek oksijen seviyelerinde bile birikme olanağı tanır ve böylece oositin in vivo algılayacağı hipoksik sinyali kısmen yeniden oluşturur.
Doğru dozda daha fazla blastosist, yüksek dozlarda zarar
Takım tedavi sonrası oositlerin ve embriyoların gidişatını incelediğinde belirgin bir desen ortaya çıktı. Düşük doz Roxadustat (25 mikromolar) oositlerin kaç tanesinin olgunlaştığını veya kaç tanesinin döllenip bölünmeye başladığını değiştirmedi, ancak blastosist aşamasına ulaşan oranı anlamlı şekilde artırdı. Başka bir deyişle, erken adımlar etkilenmemişti, fakat daha fazla embriyo başararak blastosist olma yolculuğunu tamamladı—bu da mütevazı HIF1A stabilizasyonunun oositin öznel kalitesini iyileştirdiğini düşündürüyor. Buna karşılık, en yüksek doz (100 mikromolar) olgunlaşan oosit yüzdesini azalttı ve aynı inhibitör sekiz günlük embriyo kültürü döneminde uygulandığında yüksek dozlar erken hücre bölünmesini değiştirmeden blastosist oluşumunu keskin şekilde düşürdü. Bu bulgular, olgunlaşma sırasında "yeterince" HIF1A aktivitesinin faydalı olduğunu, aşırı ya da çok uzun süreli aktivasyonun ise zararlı olduğunu gösteriyor.
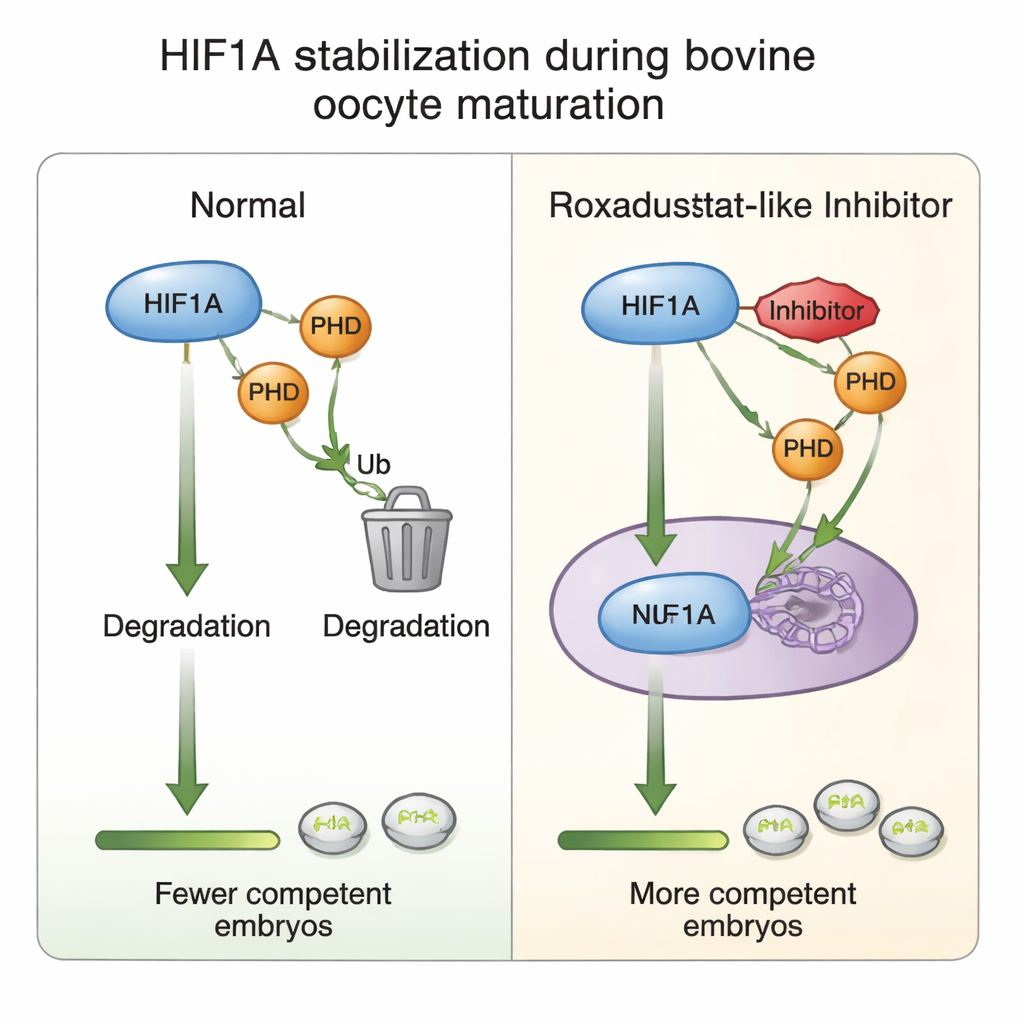
Oositin destek hücrelerinde neler oluyor
Bu kimyasal ayarın nasıl işlediğini anlamak için yazarlar her oositi çevreleyen kumulus hücrelerini inceledi. Olgunlaşmanın genel olarak HIF1A gen aktivitesini artırdığını buldular, ancak Roxadustat eklenmesi paradoksal olarak HIF1A mesajcı RNA’sını düşürürken HIF1A protein düzeylerini sabit bıraktı—bu, protein yeterince stabilize olduğunda hücrelerin gen çıktılarını kısmaya başlayabileceğine, bir tür dahili aşırı aktivasyon frenine işaret ediyor. En oksijene duyarlı PHD enzimlerinden biri olan PHD2 düzeyleri ilaca yanıt olarak arttı ve bunun oksijen algılama döngüsünün bir parçası olduğuna işaret etti. Daha yüksek ilaç dozlarında, çoğalma belirteçleri ve kumulus hücrelerinin oosit etrafında genişlemesine yardımcı olan yapışkan matriks işaretçileri azaldı; bu da gözlemlenen olgunlaşma ve embriyo oluşumundaki düşüşle tutarlı. Tüm bunlar, dikkatle dengelenmiş HIF1A aktivitesinin daha sonraki gelişim başarısının temelini oluşturan oosit ile kumulus hücreleri arasındaki diyaloğu ince ayarladığı fikrini destekliyor.
Hayvancılık ve ötesi için çıkarımlar
Bu çalışma, in vitro olgunlaşmanın kısa penceresi boyunca oositin oksijen sensörünü nazikçe stabilize etmenin sığırda blastosist verimini anlamlı şekilde artırıp dengeleyebileceğini gösteriyor; bu etki döllenme veya erken bölünmeyi değiştirmiyor. Pratik açıdan bu, oksijen seviyelerinde kaba değişiklikler veya daha toksik kimyasallar yerine hedeflenmiş bir ilaç kullanılarak yetiştirme programları için daha güvenilir embriyo üretimine dönüşebilir. Çalışma ayrıca insan fertilite tedavileriyle ilgili daha geniş bir ders veriyor: overin nüanslı, düşük oksijenli ortamını taklit etmek sadece oksijeni açıp kapamak değil, HIF1A gibi sinyal moleküllerinin hassas dengesine saygı göstermek demek. Bu dengeyi ince ayarlamak, uçlara itmek yerine, daha sağlıklı embriyolara giden kilit bir yol olabilir.
Atıf: Gübeli, M., Bleul, U. & Kowalewski, M.P. Targeted hypoxia-inducible factor 1-alpha (HIF1A) stabilization during in vitro maturation of bovine cumulus-oocyte complexes increases blastocyst rates. Sci Rep 16, 7554 (2026). https://doi.org/10.1038/s41598-025-33894-8
Anahtar kelimeler: in vitro embriyo üretimi, oosit olgunlaşması, hipoksi sinyallemesi, HIF1A stabilizasyonu, sığır üremesi