Clear Sky Science · tr
Zebrafish kalp yetmezliği modellerinde canlıda kardiyak ekstrasellüler adenosin dinamiklerinin görselleştirilmesi ve farmakolojik modülasyonu
Bu balık kalp hikâyesi neden önemli
Kalp yetmezliği dünya genelinde önde gelen ölüm nedenlerinden biri olmaya devam ediyor ve günümüzün en iyi ilaçlarına rağmen birçok hasta kötüleşiyor. Bilim insanları, stres altındaki kalp hücrelerinin çevrelerine kimyasal "kaygı sinyalleri" saldığını biliyor, ancak bu sinyalleri atan bir atan kalp içinde gerçek zamanlı izlemek zor oldu. Bu çalışma, insan kalplerinin temel özelliklerini yakından taklit eden şeffaf zebrafishleri kullanarak bu tehlike sinyallerini gerçek zamanlı izliyor ve onları susturmanın yeni bir yolunu test ediyor.
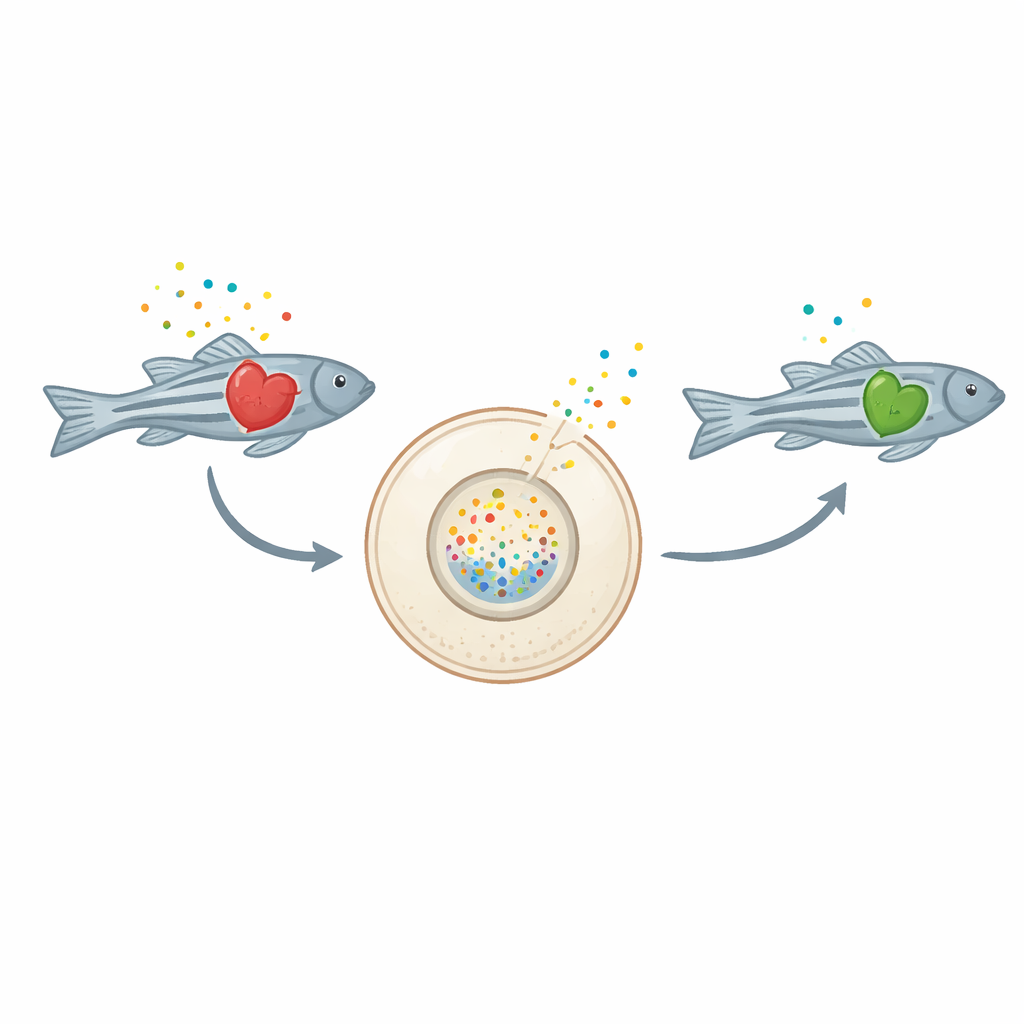
Mücadele eden bir kalpten gelen sinyaller
Kalp hücreleri yaralandığında, ATP gibi enerji taşıyan moleküller ve onun yıkım ürünü adenosin hücre dışı alana salınır. Hücre dışında bu aynı moleküller yakıt olarak değil, inflamasyonu körükleyebilecek acil mesajlar gibi davranırlar. Kronik kalp yetmezliğinde bu iltihaplanma yanıtı aşırı aktif hale gelerek kalbe daha fazla zarar verebilir. Ancak şimdiye kadar araştırmacıların, bu moleküllerin yetmezlik halindeki bir kalpte zaman içinde nasıl davrandığına dair doğrudan, canlıda kanıtı yoktu.
Zebrafishleri yaşayan kimyasal kameralara dönüştürmek
Araştırma ekibi, kalp hücrelerinin yüzeyinde GRABAdo adlı özel bir floresan sensör proteini üreten zebrafishler geliştirdi. Adenosin hücre dışına biriktiğinde, bu sensör daha parlak yeşil parlar ve her küçük kalbi kendi canlı kimyasal kamerasına çevirir. Araştırmacılar daha sonra terfenadin kullanarak zebrafishlerde kalp yetmezliğini tetiklediler; bu ilaç kalp ritmini bozması ve pompalamayı zayıflatmasıyla bilinir. Balıklarda daha yavaş kalp atışı, genişlemiş ve zayıflamış ventriküller, kalp çevresinde şişlik ve düşmüş yüzme performansı gibi belirgin kalp yetmezliği belirtileri gelişirken, kalp sensörleri parladı ve hücre dışı adenosinde belirgin bir artış ortaya çıktı. Tüm larvaların kimyasal ölçümleri, yetmezlikte toplam adenosin düzeylerinin daha yüksek olduğunu doğruladı.
Salınım vanasını kapamak
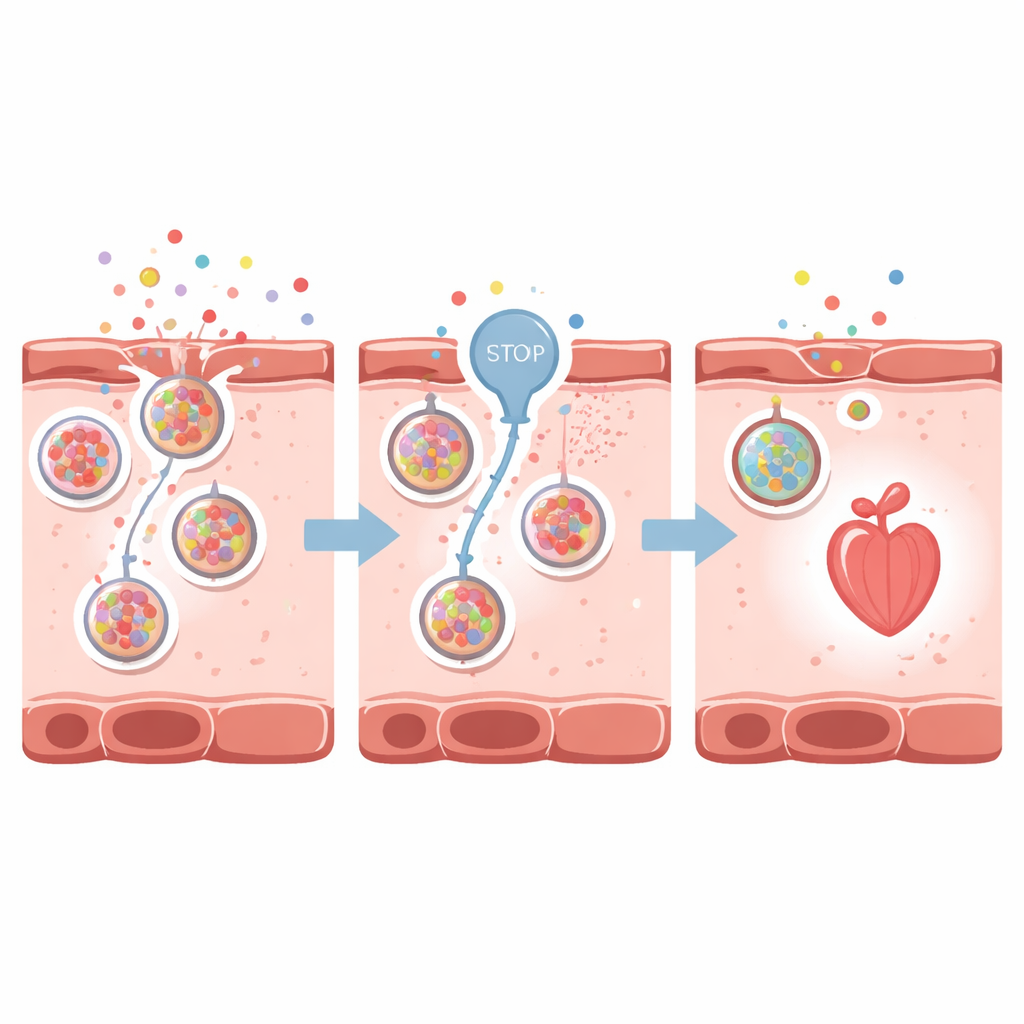
Bilim insanları bir sonraki adımda bu tehlike sinyallerini azaltmanın kalbi koruyup koruyamayacağını sordular. ATP’yi hücre içindeki küçük paketlere (veziküllere) yükleyen ve dışarı salınmasını sağlayan taşıyıcı VNUT’a odaklandılar. VNUT’u engelleyen klodronat adlı ilacı kullanarak ATP salınımını ve dolayısıyla kalp hücreleri çevresinde adenosin birikimini azalttılar. İlaçla indüklenen kalp yetmezliği olan zebrafishlerde VNUT inhibisyonu kalp şeklini korudu, odacık genişlemesini azalttı, kalp hızı ve pompalama gücünü iyileştirdi ve daha iyi kan akışını sürdürdü. Parlayan adenosin sensörü söndü; bu, hücrelerin dışında daha az kaygı sinyali olduğunu gösteriyordu. Benzer koruyucu etkiler, hızlı gelişen akut kalp yetmezliği görülen erişkin zebrafishlerde de ortaya çıktı.
Birlikte çalışan çoklu koruyucu kollar
Kalp yetmezliği birden fazla yol içerdiğinden, araştırmacılar VNUT blokajının diğer bilinen oyuncularla nasıl etkileştiğini test ettiler. Belirli adenosin reseptörlerini ve ATP reseptörlerini engelleyen ilaçlar ile zar kanalları aracılığıyla pasif ATP sızıntısını sınırlayan bir bileşik, zebrafish kalplerine yardımcı oldu. VNUT inhibisyonu ile birleştirildiğinde, bu tedavilerin çoğu ek yararlar sağladı; bu da pürin sinyallemesini birkaç noktada azaltmanın özellikle güçlü olabileceğini öne sürüyor. VNUT inhibisyonu ayrıca kalp hücrelerinde normal atım için gerekli olan kalsiyum dengesinin yeniden sağlanmasına yardımcı oldu ve hem hücre ölümü hem de inflamasyonla ilişkili gen aktivitesini azalttı. Birlikte, bu sonuçlar VNUT’u ATP salınımı, inflamasyon, bozulmuş kalsiyum düzeni ve ilerleyici kalp hasarını birbirine bağlayan merkezi bir anahtar olarak resmediyor.
Akvaryumlardan geleceğin terapilerine
Uzman olmayanlar için ana mesaj, çalışmanın yetmezlikteki kalplerde yükselen kimyasal bir stres sinyalini doğrudan görselleştirdiği ve bu sinyalin salınımını engellemenin yaşayan bir hayvanda kalp fonksiyonunu koruyabileceğini gösterdiğidir. Zebrafish kalpleri insan kalplerinden daha basit olsa da, yeni fikirler için güçlü bir test zemini sunacak kadar ortak biyolojiye sahiptirler. VNUT’u inflamasyon ve elektriksel dengesizlik kavşağında umut verici bir hedef olarak ortaya koyarak, bu çalışma gelecekteki kalp yetmezliği terapilerinin sadece kan akışını desteklemekle kalmayıp, kalbi yetmezliğe iten zararlı hücresel iletişimleri sakinleştirebileceğini düşündürüyor.
Atıf: Phurpa, P., Apolinario, M.E.C., Umeda, R. et al. In vivo visualization of cardiac extracellular adenosine dynamics and its pharmacological modulation in zebrafish heart failure models. Sci Rep 16, 8220 (2026). https://doi.org/10.1038/s41598-025-30303-y
Anahtar kelimeler: kalp yetmezliği, adenosin sinyalleşmesi, zebrafish modeli, inflamasyon, kardiyak koruma