Clear Sky Science · tr
Dizi, Yapı ve Bağlanma Afinitesi Verilerini İçeren Antikor ve Nanobody Tasarımı İçin Birleşik Bir Veri Kümesi
Neden küçük bağışıklık araçları ve büyük veri önemli
Antikorlar ve daha küçük akrabaları olan nanobody'ler, vücutta enfeksiyonlara ve kansere karşı kullanılan hassas, hedefe yönelik roketler gibidir. İlaç geliştiriciler artık bu molekülleri bilgisayar ortamında, mühendislerin uçak tasarlaması gibi tasarlamaya çalışıyor. Ancak yakın zamana dek yapay zeka ile tasarım için gereken hammadde—antikor bileşenleri, şekilleri ve hedeflerine ne kadar güçlü bağlandıklarıyla ilgili güvenilir veriler—birçok uyumsuz veritabanına dağılmış durumdaydı. Bu makale, araştırmacılara bir sonraki nesil hedefe yönelik tedavileri geliştirmek için gerekli temiz, kapsamlı veriyi sunmak amacıyla oluşturulmuş, birleşik ve herkese açık bir kaynak olan Antibody and Nanobody Design Dataset (ANDD)’i tanıtıyor.
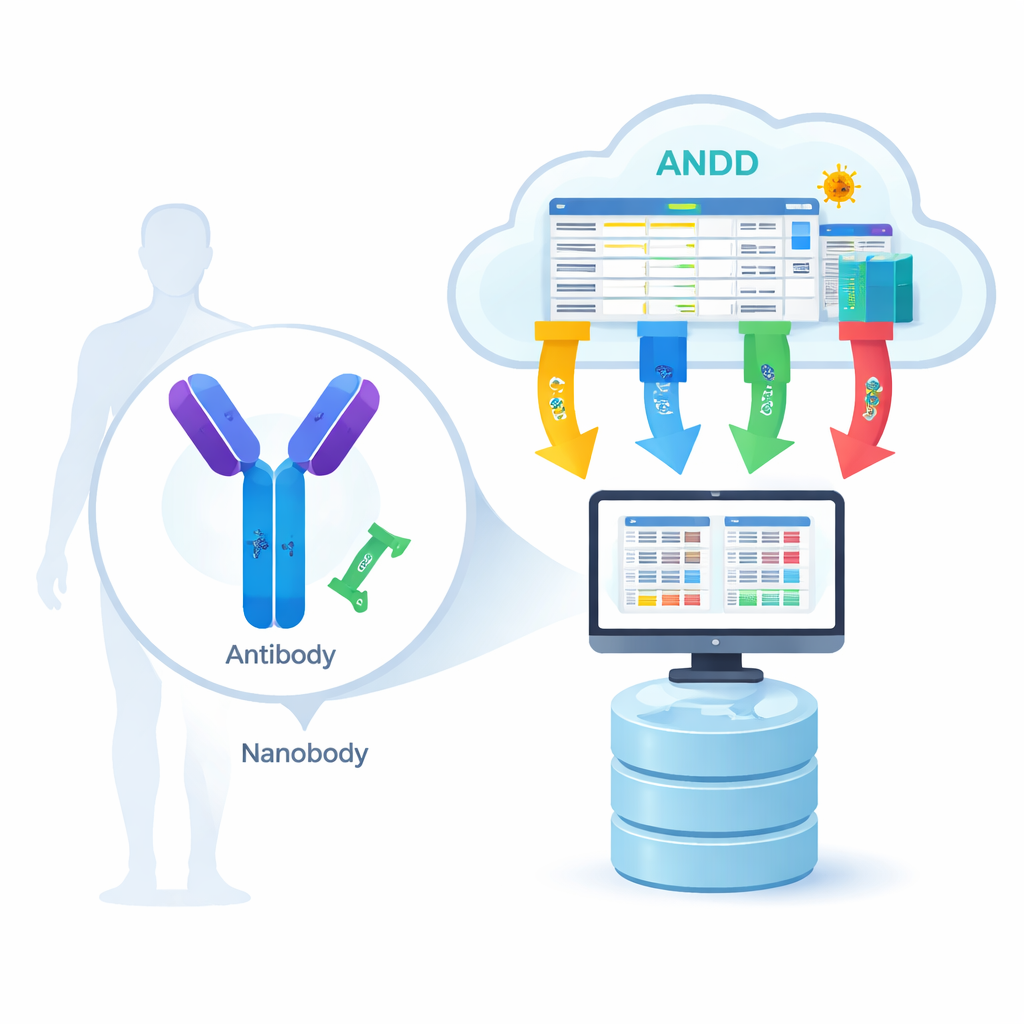
Biyolojik kilit-ve-anahtardan dijital plana
Antikorlar büyük Y biçimli proteinlerdir; nanobody'ler ise lama ve alpaka gibi hayvanlarda bulunan çok daha küçük, tek parçalı versiyonlardır. Her ikisi de virüsler, kanser hücreleri veya diğer hastalıkla ilişkili proteinler üzerindeki belirli “kilitleri” tanır. Bilgisayar modellerinin bu tanımayı nasıl yaptığını öğrenebilmesi için birçok farklı örnekte dört tür bilgiye ihtiyaç vardır: amino asit dizisi (parça listesi), 3B yapı (şekil), antijen (hedef) ve bağlanma gücü (iki parçanın ne kadar sıkı yapıştığı). Şimdiye dek çoğu kaynak bu parçaların yalnızca bir ya da ikisini aynı anda yakalıyordu; bu da bilim insanlarını veritabanları arasında atlamak ve elle veriyi birleştirmek zorunda bırakıyor, ilerlemeyi yavaşlatıyor ve hatalara yol açıyordu.
Dağınık parçaları tek, düzenli bir kütüphanede toplamak
ANDD ekibi, özel antikor ve nanobody veritabanları, genel protein depoları ve hatta patent belgeleri dahil olmak üzere 15 büyük kaynaktan veri topladı. Ardından bu ham girdileri dikkatle yazılmış bir işleme hattından geçirdiler: indirme, ortak bir şemaya yeniden biçimlendirme, tanımlayıcıları çapraz kontrol etme, çoğaltmaları çıkarma ve adlandırma kurallarını uyumlaştırma. Farklı veritabanları çeliştiğinde, küratörlü kaynaklar ve doğrudan deneyler önceliklendirildi. Sonuç, dizi, yapı, hedef ve bağlanma bilgisini tutarlı bir şekilde birleştiren tek bir tablo ve bir dizi yapı dosyasıdır; her kayıt, kullanıcıların kaynağını ve nasıl işlendiğini tam olarak izleyebilmesi için etiketlenmiştir.
Farklı araştırma ihtiyaçlarına göre katmanlı ayrıntı
ANDD’deki her kayıt aynı derecede ayrıntılı değildir; bu nedenle yazarlar koleksiyonu artan ayrıntı katmanlarına göre düzenlediler. En geniş düzeyde, dizin bilgisine sahip 48.683 antikor ve nanobody girdisi vardır. Bunların büyük bir alt kümesi 3B yapılar ekler ve daha küçük bir alt küme hedef proteinlerin dizilerini de içerir. En ayrıntılı katman—binlerce kayıt—ölçülmüş veya tahmin edilmiş bağlanma gücünü ekler. Örneğin antikorlar için 18.464 kayıt dizilere sahiptir, aynı sayı dizi ile yapıyı birleştirir, 8.000’den fazlası ayrıca antijen dizilerini içerir ve 7.737 kayıt tam dizi, yapı, antijen ve afinité verisine sahiptir. Nanobody’ler için paralel bir hiyerarşi mevcuttur; bu da deneycilere ve model geliştiricilere büyük, basit veri kümeleri veya daha küçük, daha bilgi zengini alt kümeler arasında esneklik sağlar.
Bağlanma gücündeki boşlukları doldurmak
Bağlanma gücü ilaç tasarımı için kritik önemdedir, ancak deneysel değerler nadir ve düzensiz raporlanır. Bu boşluğu veri ile tahmin arasındaki sınırı belirsizleştirmeden gidermek için yazarlar, yapı mevcut olup ölçüm eksikliği olan girdiler için yalnızca tahmin yapmak üzere ANTIPASTI adlı özel bir derin öğrenme aracını kullandılar. Bu 2.271 tahmin edilmiş değer açıkça etiketlenmiş ve yaklaşık 7.000 civarındaki deneysel olarak ölçülmüş değerlerden ayrı tutulmuştur. Ekip daha sonra genel tutarlılığı başka bir model olan AlphaBind ve bağlanmayla matematiksel olarak ilişkili ölçülerin karşılaştırılması yoluyla kontrol etti. Güçlü korelasyonlar ve düşük hata, küratörlü deneysel değerlerin güvenilir olduğunu ve tahmin edilen değerlerin yerleşik eğilimlere uygun davrandığını, ancak gerçek veri olarak kabul edilmemeleri gerektiğini gösterdi.
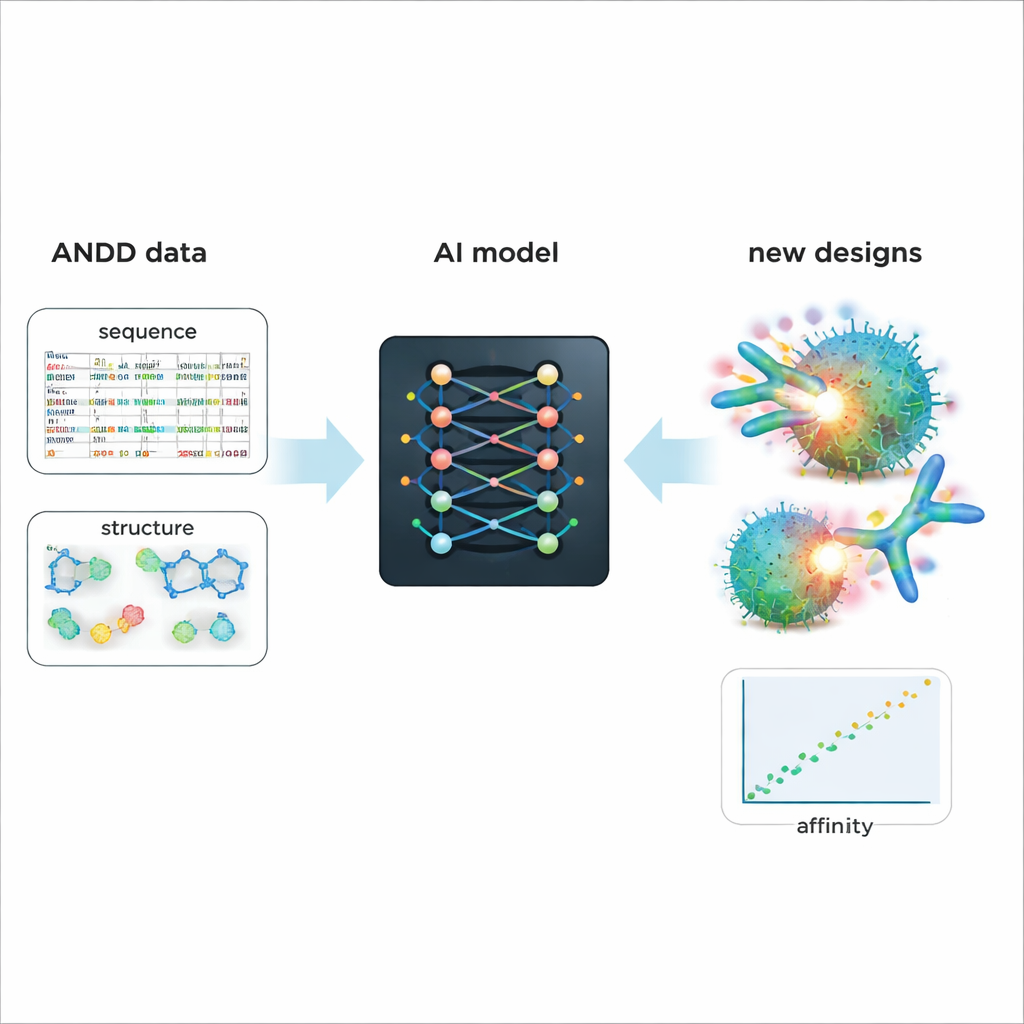
Geleceğin ilaçlarını daha akıllıca tasarlamayı mümkün kılmak
ANDD’nin pratik değerini göstermek için yazarlar antikor ve nanobody tasarlayan mevcut bir üretken yapay zeka modelini ince ayarladılar. ANDD’nin birleştirilmiş dizi, yapı, hedef ve afinité bilgileri üzerinde eğitim, daha eski ve daha basit verilerle eğitilmiş bir temel modele kıyasla daha iyi tahmin edilen bağlanma ve daha gerçekçi şekillere sahip üretilmiş moleküller verdi. Bu vaka çalışmasının ötesinde, ANDD hoşgörülü bir lisansla açıkça erişilebilirdir, tam belgeler ve tekrarlanabilir bir yapım hattı ile gelir ve düzenli olarak güncellenmek üzere tasarlanmıştır. Uzman olmayanlar için ana mesaj şudur: ANDD, antikor verilerinin dağınık yamalamasını tutarlı ve güvenilir bir kütüphaneye dönüştürerek, yapay zeka araçlarına daha hassas, daha etkili biyolojik ilaçlar tasarlamak için çok daha iyi bir başlangıç noktası sağlar.
Atıf: Wu, Y., Liu, X., Hrovatin, K. et al. A Unified Dataset for Antibody and Nanobody Design Including Sequence, Structure, and Binding Affinity Data. Sci Data 13, 295 (2026). https://doi.org/10.1038/s41597-026-06878-0
Anahtar kelimeler: antikor tasarımı, nanobody'ler, bağlanma afinitesi, biyolojik tedaviler, yapay zeka ile ilaç keşfi