Clear Sky Science · tr
Büyük Ölçekli Kolorektal Kanser Mikroçevresi İçin Meta Verili Histolojik Görüntü Veritabanı
Kanserin gizli komşuluğunu haritalamanın önemi
Doktorlar kolon tümörünü mikroskop altında incelediklerinde yalnızca kanser hücrelerini görmezler; yağ dokusu, bağışıklık hücreleri, bağ dokusu ve daha fazlasının yer aldığı yoğun bir komşuluk görürler. Bu hücre karışımı, tümör mikroçevresi olarak adlandırılır ve bir hastanın tedaviye yanıtını ve yaşam süresini güçlü biçimde etkiler. Ancak bu karmaşık sahneleri doktorların yorumlamasına yardımcı olabilecek bilgisayarlar, basit bir sorun yüzünden geri kaldı: öğrenebilmeleri için yeterince iyi etiketlenmiş görüntü yoktu. Bu çalışma, modern yapay zeka sistemlerini eğitmek ve test etmek üzere özel olarak tasarlanmış, şimdiye kadar toplanmış en büyük ve en dikkatle açıklanmış kolorektal kanser doku görsel koleksiyonlarından birini sunuyor.
Kolon tümörlerinin devasa bir görsel kütüphanesini oluşturmak
Araştırmacılar, HMU-CRC-Hist550K adını verdikleri bir kaynak oluşturdular; bu kaynak Çin’deki büyük bir kanser hastanesinde kolorektal kanser tedavisi gören 500 hastanın doku örneklerinden derlendi. Her hastanın tümörü korunmuş, patoloji laboratuvarlarında standart şekilde boyanmış ve yüksek çözünürlüklü dijital bir slayta taranmış. Bu slaytlardan ekip, patoloğun mikroskopta aynı anda görebileceği büyüklüğe yakın, küçük kare görüntü karolarını otomatik olarak çıkardı. Toplamda yaklaşık 550.000 böyle karo üretilerek yapay zeka modellerine farklı doku türlerinin nasıl göründüğünü öğrenmeleri için geniş ve çeşitli bir örnek seti sağlandı.
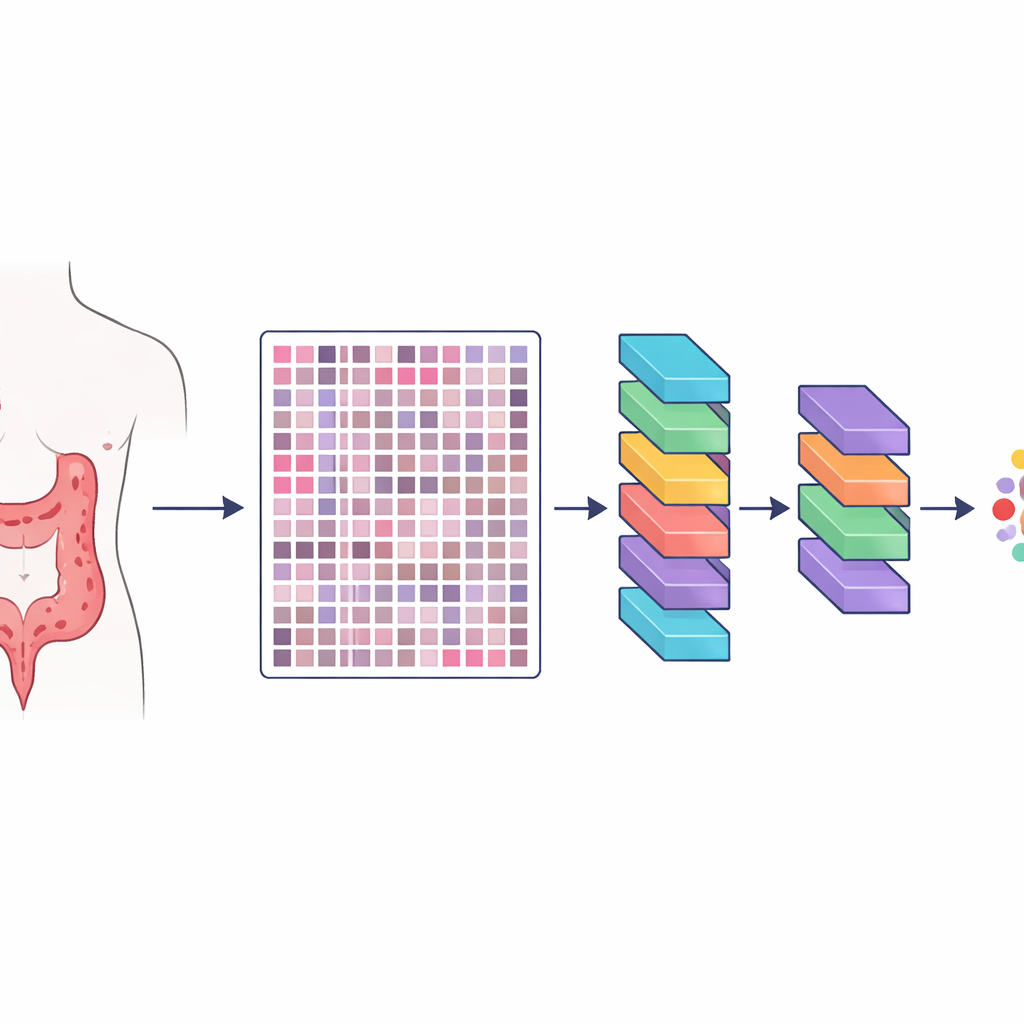
Kanser manzarasının titiz insan etiketlemesi
Büyük bir görsel kütüphanesi oluşturmak tek başına yeterli değildir; görüntülerin aynı zamanda doğru şekilde etiketlenmesi gerekir. Üç deneyimli patolog, tümör çevresinin sekiz ana bileşenini işaretlemek için üç aşamalı bir süreçte birlikte çalıştı: yağ dokusu, hücresel kalıntı, lenfosit adı verilen bağışıklık hücreleri, mukus, düz kas, normal kolon örtüsü, tümörü destekleyen bağ dokusu ve kanser hücreleri. İki patolog önce büyük slaytlar üzerinde bağımsız olarak bölgeler çizdi ve ardından birbirlerinin çalışmalarını kontrol etti. Bir kıdemli uzman son bir inceleme yaptı, anlaşmazlıkları çözdü ve belirsiz alanları hariç tuttu. Bu çapraz kontrol kişisel önyargıyı büyük ölçüde azalttı ve her karonun tümör komşuluğunda belirli bir doku türüne bağlandığı yüksek tutarlılıktaki ayrıntılı etiketler üretti.
Mikroskop görünümlerini hasta öyküleriyle birleştirmek
Bu veri setini özellikle güçlü kılan şey, görüntülerin her hasta için zengin klinik bilgilerle eşleştirilmiş olmasıdır. Her vaka için ekip yaş ve cinsiyet gibi temel bilgilerin yanı sıra tümör evresi, tümörün kolon ve rektum üzerindeki konumu, kanser hücrelerinin ne kadar anormal olduğu, sinir veya lenf düğümlerine invazyon olup olmadığı ve tedavi sonrası hastanın ne kadar süre yaşadığı gibi bilgileri topladı. Ayrıca tümörün genetik ve protein yapısını yansıtan yaygın laboratuvar test sonuçları da kaydedildi. Tüm kişisel tanımlayıcılar çıkarıldı, böylece hastalar tanınamaz hale getirildi. Doku örüntülerini bu klinik özelliklerle birleştirerek araştırmacılar, belirli mikroçevre düzenlerinin gerçek dünya sonuçlarıyla —örneğin hangi hastaların daha iyi veya daha kötü durumda olduğuyla— nasıl ilişkili olduğunu keşfedebilirler.
Yeni veri setinde YZ’yi sınamak
Veri setinin gerçekten işe yaradığını göstermek için bilim insanları, karolardaki sekiz doku türünü tanımlamak üzere üç farklı derin öğrenme modelini —görüntü görevlerinde üstün başarı gösteren modern desen tanıma sistemlerini— eğitti. Modellerin daha önce görmedikleri hastalar üzerinde değerlendirilmeleri için hastaları eğitim ve test grupları arasında ayırmada sıkı kurallar uyguladılar. Klasik görüntü ağları ve daha yeni bir “görsel dönüştürücü” (vision transformer) tasarımını içeren modellerin tümü çok yüksek doğruluk elde etti; birkaç test setinde performans skorları neredeyse mükemmele yakındı. Ekip ayrıca sonuçları diğer gelişmiş görüntü segmentasyon yöntemleriyle karşılaştırdı ve benzer şekilde güçlü performans buldu. Modellerin hangi doku bölgelerine dayandığını vurgulamak için görsel araçlar kullanıldı; bunlar modellerin rastgele desenler yerine tıbbi olarak anlamlı bölgelere odaklandığını doğruladı.
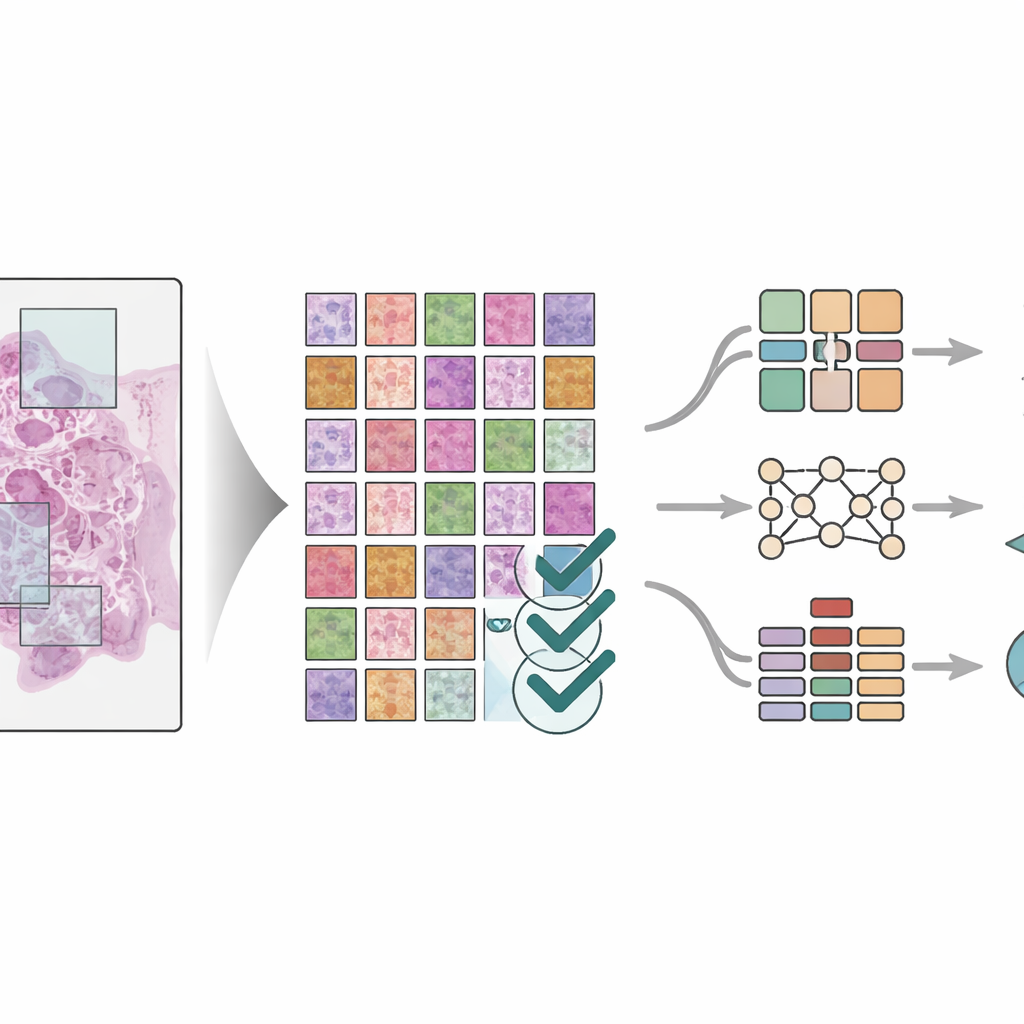
Gelecekteki kanser bakımına etkileri
Uzman olmayanlar için temel mesaj şudur: bu çalışma yeni bir tedavi sunmuyor, ancak daha akıllı tanı ve prognostik süreçler için güçlü bir temel oluşturuyor. Geniş, iyi düzenlenmiş ve ayrıntılı hasta kayıtlarına bağlı olarak açıkça erişilebilir bir görsel kütüphane paylaşarak, yazarlar dünya çapındaki araştırmacıların aynı sağlam zeminde yapay zeka araçları geliştirmesine ve karşılaştırmasına olanak tanıyor. Bu tür araçlar zamanla patologların tümör komşuluğunu daha hızlı ve tutarlı şekilde haritalamasına, hangi hastaların daha yüksek risk taşıdığını tahmin etmesine ve daha kişiselleştirilmiş tedavi stratejileri önermesine yardımcı olabilir. Mevcut veriler aylar veya yıllar içindeki değişimleri değil tek zaman noktalarını yakalasa da, bu kaynak dijital patoloji ve YZ’yi kullanarak kolorektal kanseri daha iyi anlamak ve nihayetinde daha iyi tedavi etmek yönünde önemli bir adımdır.
Atıf: Wang, H., Li, H., Xue, J. et al. Large-Scale Histological Image Dataset with Metadata for Colorectal Cancer Microenvironment. Sci Data 13, 431 (2026). https://doi.org/10.1038/s41597-026-06675-9
Anahtar kelimeler: kolorektal kanser, tümör mikroçevresi, dijital patoloji, derin öğrenme, tıbbi görüntü veritabanı