Clear Sky Science · tr
Vitamin B2 metabolizması, ferroptozisi önlemek için FSP1 stabilitesini destekler
Yaygın Bir Vitaminin Hücrelerin Yaşam ve Ölüm Arasındaki Kararını Nasıl Etkilediği
Hücresel düzeyde, hücreler sürekli olarak yaşamla kendini yok etme arasında ince bir çizgide yürürler. Ferroptozis adı verilen dramatik bir hücre ölümü biçimi, diğer tedavilere dirençli kanser hücrelerini seçici olarak öldürebildiği için ilgi çekmiştir. Bu çalışma, günlük besinlerden biri olan vitamin B2 (riboflavin)’nin, koruyucu bir ana proteini stabilize ederek dengeleri sessizce değiştirdiğini ortaya koyuyor. Diyet, hücre metabolizması ve kanser hücresi ölümü arasındaki bu gizli bağlantının anlaşılması, araştırıcıların daha akıllı tedaviler tasarlamasına ve gelecekteki beslenme önerilerini iyileştirmesine yardımcı olabilir.
Hücre İçindeki Özel Bir Paslanma Türü
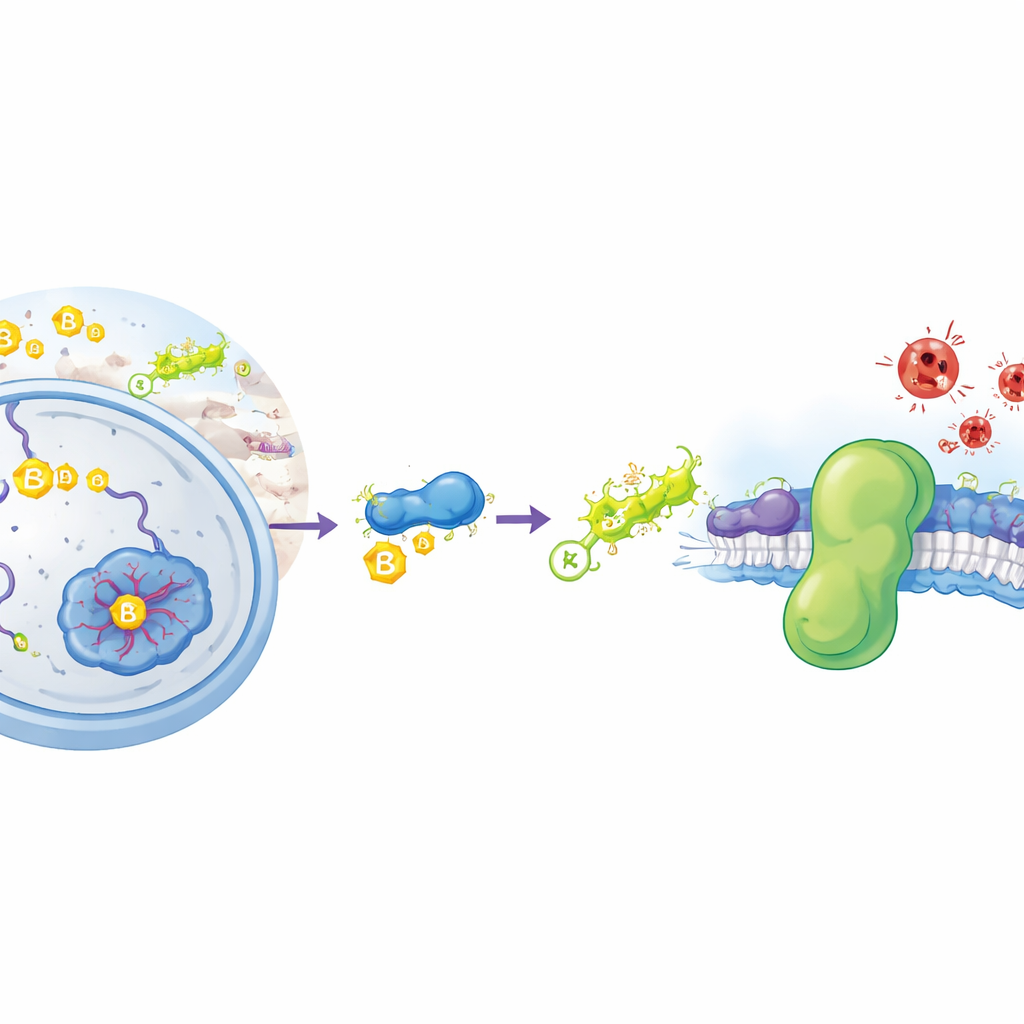
Ferroptozis, hücre membranlarındaki yağların kontrolsüz oksidasyonu gibi metalin paslanmasına benzeyen kimyasal bir süreç tarafından tetiklenen bir hücre ölümü türüdür. Bu yağlar parçalandığında, membranlar bütünlüğünü yitirir ve hücreler patlar. Hücrelerimiz normalde bunun olmasını engellemek için birkaç savunma mekanizması kullanır. Birincil kalkan, zararlı lipid peroksitleri detoksifiye etmek için küçük bir molekül olan glutathione’u kullanan GPX4 adlı bir enzimdir. Paralel ikinci bir kalkan ise hücresel membranlarda bulunan ve yıkıcı radikalleri yayılmadan önce yakalamak için yağ benzeri küçük moleküller kullanan FSP1 adlı bir proteindir. Kanser hücreleri sıklıkla ferroptozisten kaçınmak için FSP1’i artırır; bu da bu proteini yeni anti-kanser ilaçları için başlıca bir hedef haline getirir. Ancak şimdiye kadar, hücrelerin ne kadar FSP1 ürettiğini ve proteinin ne kadar süre yaşadığını nasıl kontrol ettikleri bilinmiyordu.
Bir Ölüm Engelleyici İçin Hücresel “Yakıt Göstergesi” İnşası
FSP1’in gizli yöneticilerini ortaya çıkarmak için araştırmacılar önce insan kemik kanseri hücrelerini floresan raporlayıcı taşıyacak şekilde dizayn ettiler. Doğal FSP1 proteinini yeşil bir ışık sinyaliyle işaretlediler ve hücrenin ne kadar FSP1 mesajı ürettiğini bildiren mavi sinyalle eşleştirdiler. Bu zekice tasarım, gen aktivitesindeki değişiklikleri (mavi) protein stabilitesindeki değişikliklerden (yeşil) ayırmalarını sağladı. Bu çift renkli sistem kurulduktan sonra, CRISPR–Cas9 kullanarak genomdaki neredeyse her geni sistematik olarak bozdular ve ardından yüksek veya düşük FSP1 seviyelerine sahip hücreleri ayırdılar. Hangi kılavuz RNA’ların hangi grupta zenginleştiğini karşılaştırarak, gen kontrolü veya protein dönüşümü düzeyinde FSP1’i artıran veya azaltan yüzlerce geni haritaladılar.
Vitamin B2’nin Gizli Görevi: Stabilize Edici Bir Sap Oluşturmak
En çarpıcı bulgulardan ikisi, vitamin B2’yi FAD adlı bir kofaktöre dönüştüren riboflavin kinaz (RFK) ve FAD sentaz (FLAD1) adlı iki enzimdi. FSP1, kimyasal reaksiyonlarını gerçekleştirmek için normalde FAD’a sıkı sıkıya bağlanan bir flavoproteindir. RFK veya FLAD1 çıkarıldığında ya da hücreler vitamin B2’den yoksun ortamda büyütüldüğünde, FSP1 protein seviyeleri gen aktivitesi benzer kalmasına rağmen keskin şekilde düştü. Ekip, bu kaybın GPX4 bloke edildiğinde hücreleri ferroptozise karşı çok daha savunmasız hale getirdiğini gösterdi. Önemli olarak, vitamin B2 kendisi klasik bir antioksidan gibi davranmıyordu: hassas bir test tüpü testinde, vitamin E’nin aksine lipid oksidasyonunu durduramadı. Bunun yerine, eksik hücrelere FAD (ve kısmen onun öncüsü FMN) eklemek hem FSP1 seviyelerini hem de ferroptotik ölüme karşı direnci geri getirdi; oysa işleme enzimleri eksikse ekstra vitamin B2 tek başına yardımcı olmadı.
Kofaktör Eksik Olunca Ne Olur
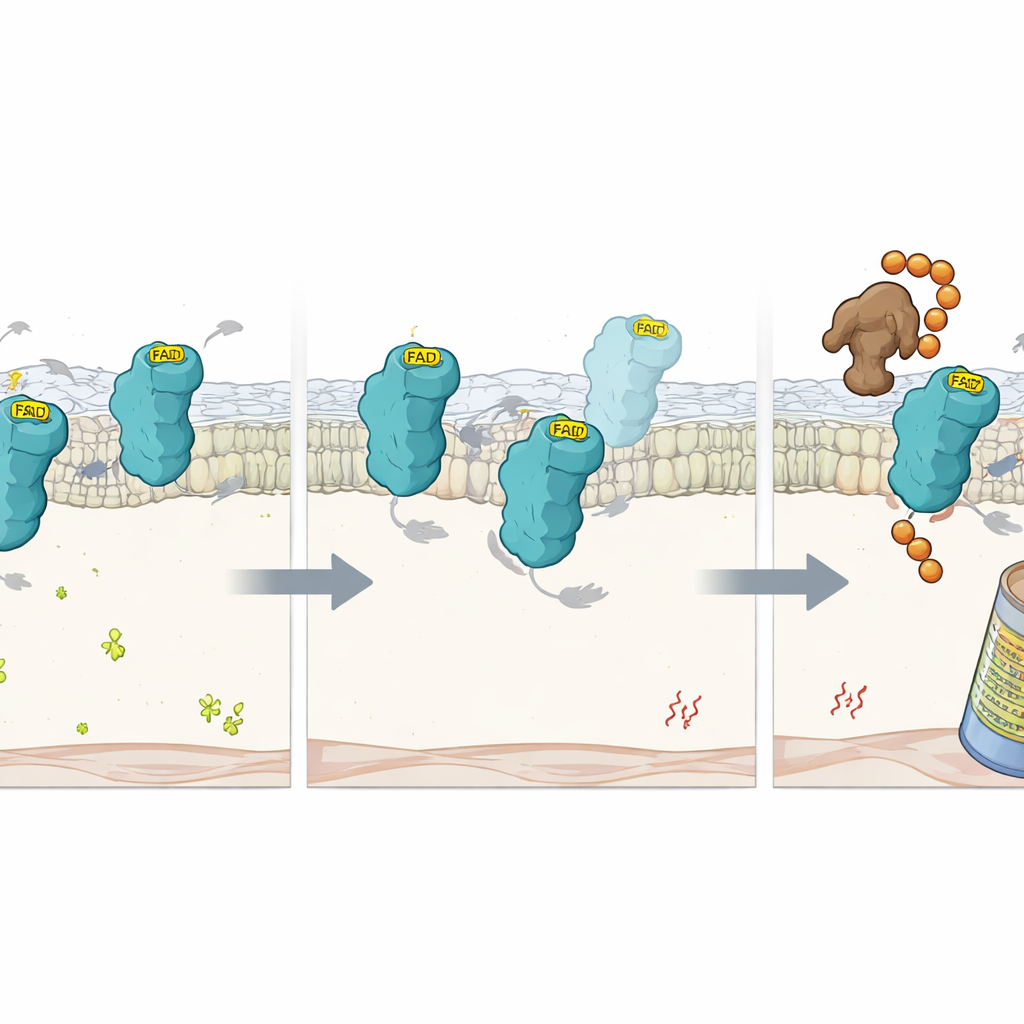
Daha da yakından bakmak için bilim insanları, FAD tutma yeteneğini bozan hassas FSP1 mutasyonlarını incelediler. Bu mutant proteinler büyük ölçüde normal şekillerde katlanmaya devam etmiş ancak FAD’larını ve katalitik aktivitelerini kaybetmişti. Hücre içinde, proteazom—hücrenin protein parçalayıcı makinesi—engellenmedikçe normal FSP1’e kıyasla çok daha hızlı bozuluyorlardı. Bu, FAD bağlanmasının kendisinin FSP1’i kusurlu olarak işaretlenmekten koruyan stabilize edici bir sap gibi davrandığını düşündürdü. Düşük FAD koşullarında yapılan başka odaklanmış bir CRISPR taramasıyla ekip, FAD’sız FSP1’i tanıyan RNF8 adlı bir E3 ligazını kilit bir faktör olarak belirledi. RFK silindiğinde, RNF8 boş proteine ubiquitin etiket zincirleri ekleyerek onu proteazom tarafından yok edilmeye hedefliyordu. RNF8’in uzaklaştırılması, FAD fakiri hücrelerde FSP1 dönüşümünü yavaşlattı, ancak kofaktör olmadan kaybolan koruyucu işlevini geri getiremedi.
Moleküler Devrelerden Kanser Terapisi Fikirlerine
Bu parçaları bir araya getiren yazarlar basit ama güçlü bir model öneriyorlar. Vitamin B2, RFK ve FLAD1 tarafından FAD’e dönüştürüldükten sonra FSP1’e bağlanır ve hem onun biyokimyasal aktivitesi hem de ömrü için esastır. Vitamin B2 arzı veya onun işlenmesi aksadığında, yeni sentezlenen FSP1 FAD’ı güvence altına alamaz, RNF8 tarafından işaretlenir ve proteazom tarafından hızla parçalanır; bu durum hücreleri ferroptotik hasara karşı daha açık hale getirir. Kanser verileri, RFK ekspresyonu daha yüksek olan tümörlerin ferroptozis indükleyen ilaçlara daha dirençli olduğunu göstererek bu yolun gerçek dünya alaka düzeyini vurguluyor. Uzman olmayanlar için ana mesaj, tanıdık bir vitaminin basit bir antioksidandan çok daha fazlasını yaptığıdır: güçlü bir anti-ölüm proteininin bekçi olarak kalıp kalmayacağına veya süpürülüp atılacağına karar vermesine yardımcı olur. Vitamin B2 metabolizması veya FSP1 stabilitesini ayarlayarak, gelecekteki tedaviler sağlıklı dokuları korurken kanser hücrelerini ortadan kaldırmak için ferroptozisi daha iyi kullanabilir.
Atıf: Deol, K.K., Harris, C.A., Tomlinson, S.J. et al. Vitamin B2 metabolism promotes FSP1 stability to prevent ferroptosis. Nat Struct Mol Biol 33, 525–536 (2026). https://doi.org/10.1038/s41594-026-01759-x
Anahtar kelimeler: ferroptozis, vitamin B2, FSP1, kanser hücresi ölümü, hücre metabolizması