Clear Sky Science · tr
Mayaya amino asit algılayıcı SEAC–EGOC süperkopleksinin yapı ve işlevi
Hücreler Büyümeye Ne Zaman Karar Verir?
Her hücre sürekli olarak büyüyüp büyümemeye veya kaynakları korumaya karar vermek zorundadır. Bu karar büyük ölçüde proteinlerin yapı taşları ve önemli bir azot kaynağı olan amino asitlere bağlıdır. Bu makale, maya hücrelerinin amino asit varlığını devasa bir moleküler düzen aracılığıyla nasıl algıladığını ve bu bilgiyi ana büyüme düzenleyicisi TORC1’i açıp kapatmak için nasıl kullandığını olağanüstü yapısal ayrıntıyla ortaya koyuyor. Aynı devre insan hücrelerinde korunmuş olduğundan ve kanser ile metabolizma ile ilişkilendirildiğinden, mayadan elde edilen bulgular bizim hücrelerimizin de ne zaman büyüme için uygun koşullar olduğunu nasıl değerlendirdiğine dair pencere açıyor.
Hücrenin Geri Dönüşüm Merkezinde Karmaşık Bir Merkez
Mayada, SEAC adı verilen merkezi bir karar verme kompleksi vakuol membranında yer alır; vakuol hücrenin geri dönüşüm merkezi gibi davranan bir organeldir. Orada amino asit düzeyleri hakkında bilgi ileten EGOC adlı başka bir kompleksle karşılaşır. Birlikte TORC1’e, ana büyüme anahtarına sinyal iletirler. SEAC iki işlevsel yarıya sahiptir: TORC1’i kapatabilen SEACIT ve uzun süre SEACIT’i kontrol altında tuttuğu düşünülen SEACAT. Yazarlar, tam SEAC’ın EGOC’a bağlı hâlini yüksek çözünürlüklü kriyo-elektron mikroskopisi ile görselleştirerek, sinyalleşmenin tam olarak gerçekleştiği vakuol yüzeyinde bu moleküler merkezinin anlık görüntüsünü yakaladılar. 
Moleküler Mimarinin Yakından Görülmesi
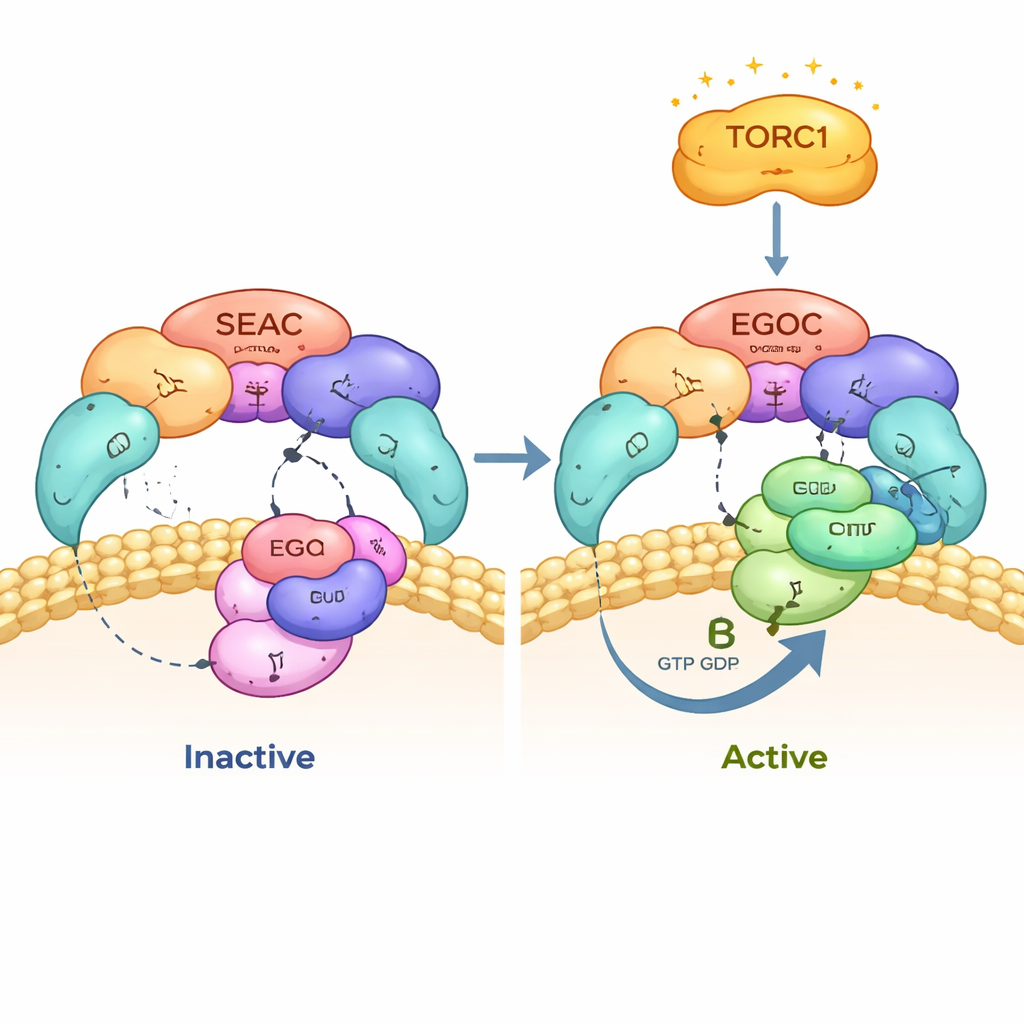
Yapı, SEAC’ı SEACAT alt birimlerinden oluşan büyük bir çekirdek olarak ortaya koyuyor; buradan iki esnek SEACIT "kanadı" uzanıyor. Her bir kanat bir EGOC kompleksine bağlanabilir; bu da tek bir SEAC’ın aynı anda iki sinyal girdisiyle etkileşime girebileceği anlamına geliyor. Dikkat çekici biçimde EGOC sadece kanatlara bağlanıyor, çekirdeğe değil ve EGOC varlığında SEAC’ın genel şekli neredeyse değişmiyor. Bu, SEACAT’ın SEACIT’in aktif bölgesini fiziksel olarak engellemediğini ve EGOC’un bağlanmasını engellemediğini gösteriyor. Kompleksin vakuol membranı üzerindeki yönlenmesi ayrıca SEAC çekirdeğini sitoplazmaya dönük konumlandırıyor; böylece ilave düzenleyicilerle etkileşime girebiliyor, kanatlar ise membrana yakın durarak EGOC ve diğer membran-bağlantılı ortaklarla temasa ideal şekilde uygun konumda bulunuyor.
SEAC Doğru Sinyali Nasıl Seçer?
Yazarlar SEAC ile EGOC arasındaki temaslara odaklandılar ve SEAC’ın yalnızca EGOC’un "aktif" sürümünü tanıdığını buldular; bu durumda EGOC’un küçük GTPaz proteini Gtr1 bir GTP-benzeri nükleotid taşırken eşlik eden Gtr2 GDP taşır. SEACIT, Gtr1’in nükleotid yuvasına uzanan katalitik bir "parmak" sağlar ve GTP’nin parçalanmasını hızlandırarak EGOC’u aktif durumdan inaktif duruma çevirir. Ayrıntılı kriyo-EM haritaları ve mutasyon deneyleri, bu katalitik parmak ile bitişik bir yardımcı kalıntının etkileşim ve nükleotid durumunun doğru okunması için elzem olduğunu gösteriyor. Yazarlar bu kritik kalıntıları değiştirdiklerinde, SEAC artık vakuole doğru şekilde lokalize olmuyor ve EGOC verimli şekilde bağlanamıyordu.
Büyüme Anahtarının Hızlı ve Yavaş Kontrolü
Canlı hücre için bunun ne anlama geldiğini anlamak üzere araştırmacılar, amino asitler kaldırıldığında ve sonra yeniden verildiğinde TORC1 aktivitesini zaman içinde izlediler. Normal hücrelerde, TORC1 azot kıtlığı sonrasında birkaç dakika içinde hızla kapanıyor ve amino asitler geri geldiğinde tekrar hızla açılıyor. SEACIT içindeki katalitik parmak devre dışı bırakıldığında ya da SEACIT alt birimleri çıkarıldığında, TORC1 bu erken zaman penceresinde neredeyse yanıt vermiyordu. Aynı durum hem Gtr1 hem Gtr2 çıkarıldığında da gözlendi; bu da SEAC–EGOC çiftinin TORC1’in amino asit kontrolü için baskın, hızlı yol olduğunu gösteriyor. Ancak daha geç zamanlarda —yaklaşık yarım saat civarında— bu mutantlarda bile TORC1 aktivitesi yavaşça ayarlandı; bu, GTPaz sisteminden bağımsız ayrı, daha yavaş bir TORC1 yolunun da hücrelerde işlediğini gösteriyor.
Uzak Bir Alt Birim İçin Sürpriz Bir Rol
Özellikle ilgi çekici bir bulgu Sea2 ile ilgili; Sea2, çekirdekten dışarı doğru çıkan esnek bir "pervane" bölgesine sahip SEACAT komponentidir. Sea2’nin veya yalnızca pervanesinin çıkarılması, SEAC’ın katalitik aktivitesinin kaybı görüldüğünde ortaya çıkan sinyal kusurlarına neredeyse tamamen aynı etkileri verdi: TORC1 amino asit çekilmesine ve yeniden beslemeye yavaş yanıt verdi. Oysa Sea2 katalitik bölgeden uzaktadır ve doğrudan SEACIT kanadına dokunmaz; bu nedenle basit bir engelleme mekanizması olası görünmüyor. Sea2 kaybını katalitik olarak ölü bir SEAC varyantıyla birleştiren genetik deneyler, GAP aktivitesinin tamamen açık veya tamamen kapalı kilitlenmesinin her ikisinin de hızlı yanıtı bozduğunu, oysa ara düzenlemenin gerektiğini öne sürdü. Yazarlar Sea2’nin pervanesinin, SEACIT’in aktivitesini ılımlı hale getiren bilinmeyen bir faktör için bir demirleme platformu görevi gördüğünü ve bunun hücrelerin TORC1’i tamamen kapatmak yerine hassaslaştırarak ayarlamasına izin verdiğini öneriyorlar.
Bu, Hücre Büyüme Kararları İçin Ne Anlama Geliyor?
Genel olarak çalışma, SEAC’ı karşıt iki düzenek olarak değil, amino asitleri algılayıp büyüme anahtarı TORC1’i hızlıca ayarlayan tek, bütünleşik bir makine olarak yeniden tanımlıyor: katalitik kanadı (SEACIT) ve yapısal çekirdeği (SEACAT) birlikte çalışıyor. SEACIT’in EGOC üzerindeki enzimatik etkisi hızlı ve hassas kontrol sağlarken Sea2’nin pervanesi muhtemelen bu aktiviteyi ayarlayan düzenleyicileri topluyor. Aynı zamanda daha yavaş paralel yollar, birincil sensör bozulsa bile TORC1’in nihayetinde besin durumunu yansıtmasını sağlıyor. Yakın ilişkili kompleksler insan hücrelerinde aynı işi yaptığından, mayadan elde edilen bu bulgular kendi hücrelerimizin büyümeyi besin arzıyla nasıl dengelediğini aydınlatıyor ve TORC1 sinyalleşmesinin bozulduğu hastalıkların anlaşılmasına ilişkin çıkarımlar sunuyor.
Atıf: Tafur, L., Bonadei, L., Zheng, Y. et al. Structure and function of the yeast amino acid-sensing SEAC–EGOC supercomplex. Nat Struct Mol Biol 33, 488–498 (2026). https://doi.org/10.1038/s41594-026-01746-2
Anahtar kelimeler: amino asit algılama, TORC1 sinyalleşmesi, SEAC GATOR kompleksi, hücre büyüme kontrolü, kriyokütle elektron mikroskobu