Clear Sky Science · tr
Cereblon, moleküler yüzey taklidi kullanarak G3BP2 neosübstratını parçalanmaya yönlendirir
Hücresel Temizliği Akıllı Bir Hedefleme Sistemine Çevirmek
Modern ilaçlar, sorunlu proteinleri sadece engellemekle kalmayıp onları tamamen ortadan kaldırmaya da giderek daha fazla odaklanıyor. Bu makale, hücrenin kendi "temizlik" makinelerinden birini yeniden kablolamanın zekice bir yolunu inceliyor; küçük bir molekülle eşleştirildiğinde kanser ve diğer bozukluklarla ilişkili bir proteini tanıyıp yok edebiliyor. Çalışma beklenmedik bir hile ortaya koyuyor: temizlik makinesi, proteinlerin doğal ortaklarından birini taklit etmek üzere yüzeyinin bir kısmını yeniden şekillendiriyor; bu sayede ona tutunup proteini hücresel çöpe gönderebiliyor.
Gizli Esnekliğe Sahip Bir Hücresel Çöp Toplayıcı
Hücrelerimiz sürekli olarak yıpranmış veya istenmeyen proteinleri ortadan kaldırmak için etiketler; bu kararları veren E3 ligazlar etrafında kurulu bir sistem kullanılır—atılması gerekenleri belirleyen büyük protein kompleksleri. Bu komplekslerden biri, diğer proteinlerdeki belirli özellikleri ("degronlar") tanıyan bir sensör gibi davranan cereblon adlı bir bileşene dayanır. Onaylanmış bazı ilaçlar zaten cereblon’u "moleküler yapıştırıcı" olarak kullanır: cereblon’a bağlanır ve hastalıkla ilişkili proteinleri çekip onların etiketlenerek parçalanmasına yol açan yeni bir bağlanma yüzeyi oluştururlar. Bugüne dek bilinen hedeflerin çoğu belirli bir yapısal deseni kullandığından, bu yolla kaldırılabilecek proteinlerin yelpazesi sınırlı görünüyordu.
Eski Kuralların Dışında Yeni Bir Hedef Keşfi
Yeni çalışmada yazarlar, insan hücrelerinde cereblon’a odaklı moleküler yapıştırıcı koleksiyonunu taradılar ve MRT-5702 adlı bir bileşiği tanımladılar. Bu küçük molekül, RNA’yı yöneten ve stres granüllerinin bir bileşeni olan G3BP2 adlı bir proteinin hızla kaybolmasına neden oldu—stres granülleri kanser, kalp sorunları ve nörodejeneratif hastalıklarla ilişkilidir. Önemli olarak, G3BP2 cereblon’un tanıdığı olağan degron desenini taşımıyordu. İzleyen hücre deneyleri, protein yakınlığını hassas ışık tabanlı okumalara kadar içeren testler, MRT-5702’nin cereblon ile G3BP2’yi G3BP2 parçalanmasına yol açan üçlü bir kompleks içinde bir araya getirdiğini doğruladı; bu esnada yakın akraba proteini G3BP1’i, kilit alanı değiştirilmedikçe, etkilemedi.
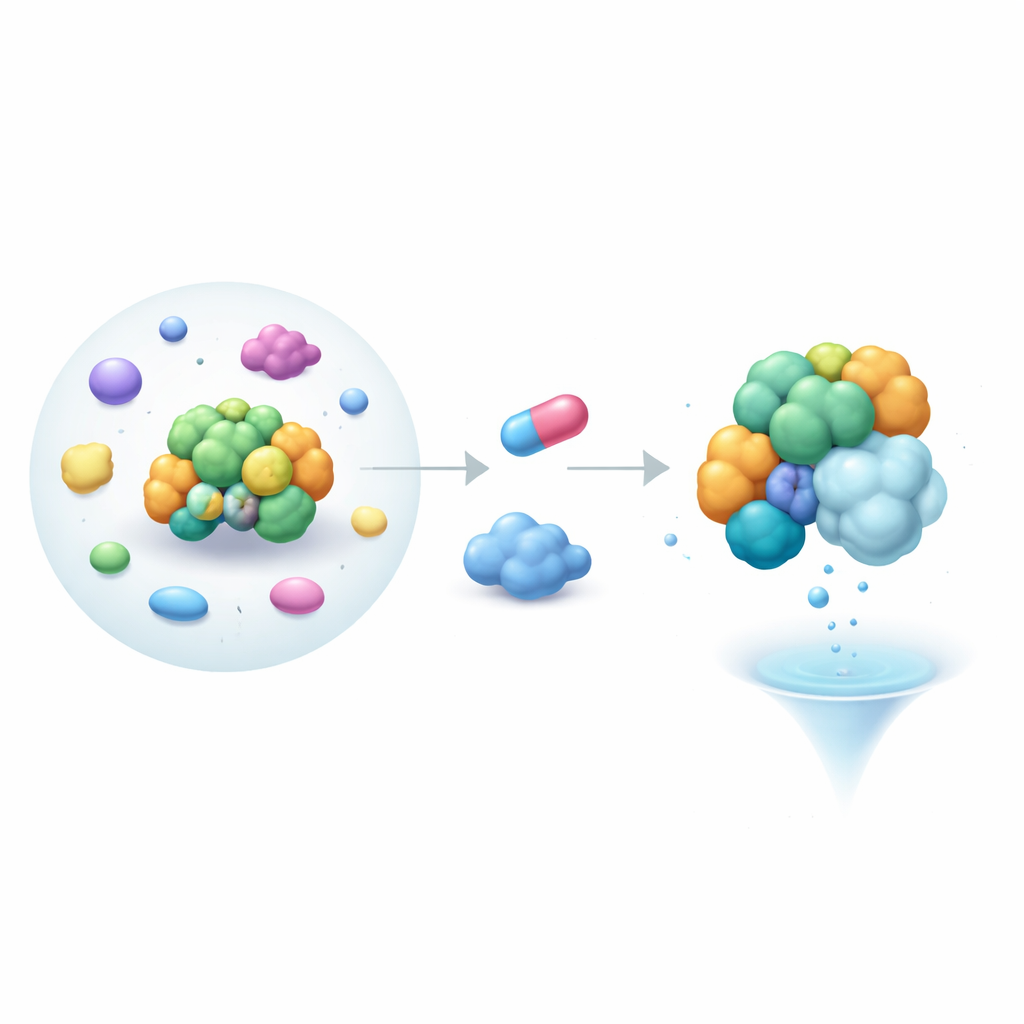
Bağlanma Stratejisi Olarak Taklit
Daha derine inen araştırmacılar, G3BP2’nin standart tanıma motifi olmadan cereblon’a nasıl bağlanabildiğini sordular. G3BP2 ile bilinen cereblon hedefleri arasındaki benzerlikleri aramak yerine soruyu tersine çevirdiler: cereblon, G3BP2’nin olağan bağlanma ortaklarından birine benzeyebilir miydi? G3BP proteinleri genellikle kısa dizi motiflerini tanıyan NTF2-benzeri bir bölgedeki bir sıcak nokta aracılığıyla diğer moleküllerle etkileşir. G3BP2’nin doğal ortağı USP10’un yapısal modellerini kullanarak, ekip cereblon yüzeyini hesaplamalı olarak taradı ve daha az anlaşılan bir bölge olan LON domenininde, USP10’un bağlanma motifinin şekil ve kimyasıyla yakından benzer bir yama buldu. Bu yamadaki sadece birkaç ana aminoasit veya G3BP2 sıcak noktasındaki değişiklikler üçlü kompleksi zayıflattı; bu da cereblon’un G3BP2’ye demir atmak için etkin bir şekilde USP10’u taklit ettiğini düşündürüyordu.
Yeni Arayüzü Atomik Ayrıntıda Yakalamak
Bu alışılmadık etkileşimi görselleştirmek için ekip, cereblon, başka bir temel ligaz bileşeni, MRT-5702 ve G3BP2’nin NTF2-benzeri domainini içeren bir kompleksin yapısını yüksek çözünürlüklü kriyo-elektron mikroskopisi ile çözdü. Görüntüler, cereblon’un LON domainindeki esnek bir döngünün bükülüp yeniden şekillenerek G3BP2 ile temas yüzeyinin neredeyse yarısını oluşturduğunu gösterdi. MRT-5702’nin aktif ayna görüntüsü cereblon’un olağan ilaç bağlanma cebinde oturuyordu, fakat döngüyle birlikte G3BP2 dimerinin bir yarısını kavrayan geniş bir iniş platformu yaratılmasına yardımcı oluyordu. Çarpıcı bir şekilde, bu düzenleme önceki yapıştırıcı hedefleri işleyen kanonik cereblon bölgesini neredeyse kullanmıyor, bu da cereblon’un yapıştırıcıya ve ilgili proteine bağlı olarak yüzeyinin çok farklı bölgelerine bağlanabileceğini gösteriyor. Aynı zamanda, G3BP2 dimerinin dokunulmamış yarısı diğer ortaklara bağlanmaya açık kalarak, bağlı olan proteinlerin “ikincil” parçalanması için makul bir yol sunuyor.
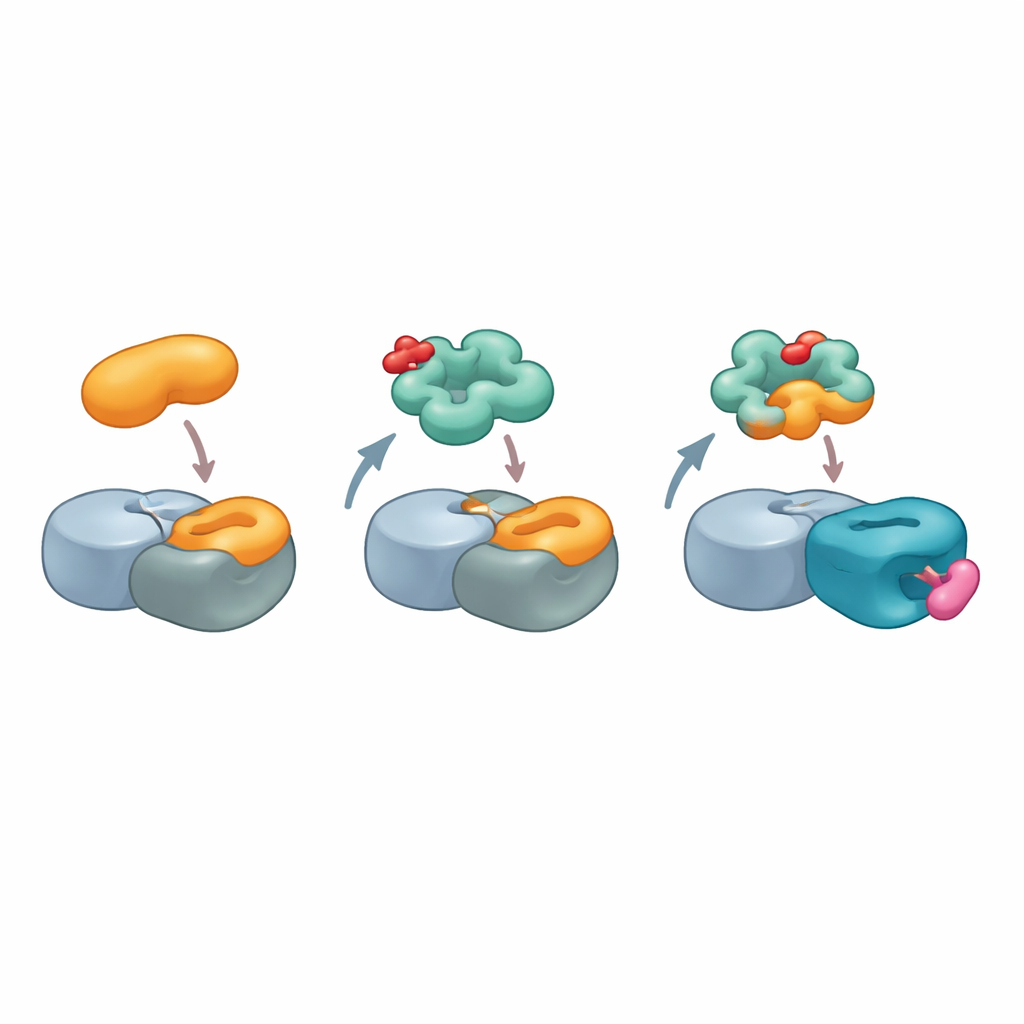
Gelecek İlaç Tasarımı için Yapıştırıcı Baskıları
Bir arada ele alındığında bulgular, cereblon’u önceki düşünülenden çok daha esnek bir arabulucu olarak resmediyor. Hedeflerin tek tip bir degron taşımasını şart koşmak yerine cereblon, uygun moleküler yapıştırıcı ile donatıldığında hücrenin başka yerlerindeki doğal protein–protein etkileşimlerini taklit eden bileşik bir yüzey oluşturabilir. Yazarlar, bunlara "glueprint" (yapıştırıcı baskısı) adını verdikleri bu birleşik protein-ve-yapıştırıcı yüzeylerin haritalanıp tasarlanarak birçok hastalıkla ilişkili proteindeki mevcut etkileşim sıcak noktalarını taklit edebileceğini öne sürüyor. Bir düz okuyucu için ana mesaj şu: ilaç geliştiricilerin sorunlu proteinlerde yepyeni bağlanma cepleri keşfetmelerine gerek olmayabilir; bunun yerine hücrenin kendi geri dönüşüm mekanizmasını, o proteinlerin olağan ortaklarının şekillerini kopyalayarak onları tanıyacak şekilde eğitebilirler; bu da güvenli ve seçici biçimde kaldırılabilecek hedeflerin listesini büyük ölçüde genişletir.
Atıf: Annunziato, S., Quan, C., Donckele, E.J. et al. Cereblon induces G3BP2 neosubstrate degradation using molecular surface mimicry. Nat Struct Mol Biol 33, 479–487 (2026). https://doi.org/10.1038/s41594-025-01738-8
Anahtar kelimeler: moleküler yapıştırıcı bozucular, cereblon, hedefe yönelik protein yok etme, G3BP2, protein–protein etkileşimleri