Clear Sky Science · tr
TGFβ sinyali, mekânsal ve zamansal olarak sınırlı miyelin dejenerasyonuna karşı mikroglial dayanıklılığı sağlar
Beynin Kablolamasının Neden Bakıcılara İhtiyacı Var
Yaşlandıkça sinir liflerimizin çevresindeki “yalıtım” olan miyelin doğal olarak aşınır. Bu yalıtım, beyin ile beden arasındaki hızlı ve güvenilir iletişim için hayati öneme sahiptir. Yeni çalışma, omuriliğin bir spesifik sinir lifi otoyolu olan dorsal kolonun neden bu aşınmaya karşı olağandışı derecede savunmasız olduğunu ve TGFβ adı verilen bir sinyal yolunun hasarın kontrolden çıkmasını nasıl engellediğini araştırıyor. Bu gizli güvenlik mekanizmasını anlamak önemlidir çünkü işlevinin bozulması bazı omurilik bozukluklarını açıklamaya yardımcı olabilir ve yaşlı yetişkinlerde beyin ile kanser hastalıklarının tedavisini etkileyebilir.
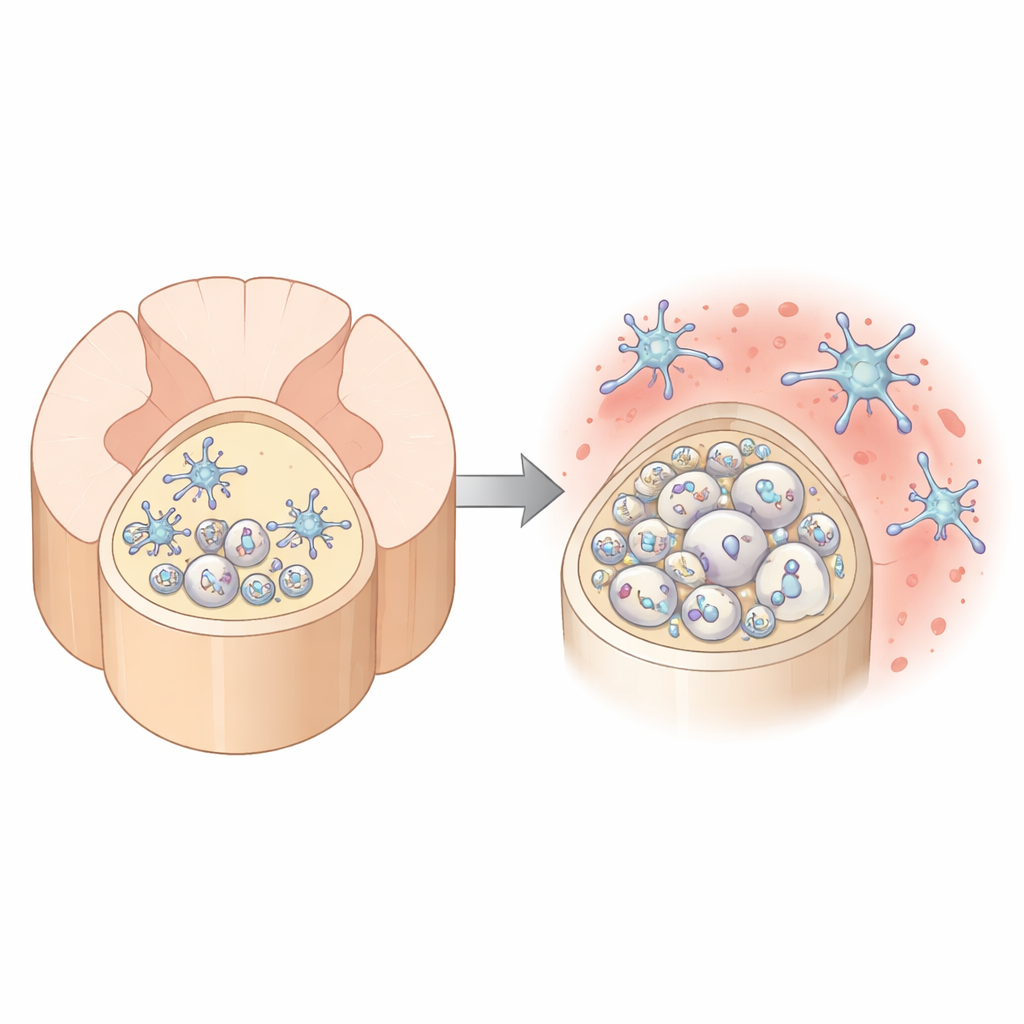
Yaşlanmanın Omuriliğin “Süper Otoyolu”na En Çok Zarar Verdiği Yer
Yazarlar önce fare omuriliğindeki iki ana beyaz madde yolunu karşılaştırdılar: arkadaki dorsal kolon ve öndeki ventral kolon. Yüksek çözünürlüklü elektron mikroskobu kullanarak, yaşla birlikte dorsal kolondaki miyelinin giderek daha fazla bozulduğunu buldular. Normalde sıkı sarılı olması gereken miyelin liflerin etrafında gevşiyor, dışa doğru kabarıyor veya ayrılıyor; sinir ile yalıtım arasında genişlemiş boşluklar ve açık miyelin parçalanmasında artış gözleniyor. Buna karşılık ventral kolon nispeten stabil kalıyor. Dorsal bölge ayrıca daha çok ama daha ince akson barındırıyor, bu da miyelini inşa eden ve bakımını yapan hücreler için özellikle zorlu bir ortam oluşturuyor.
Büyüyen Baskı Altındaki Bağışıklık Gözcüleri
Bu lifleri çevreleyen mikroglia, beyinin ve omuriliğin yerleşik bağışıklık hücreleri. Sürekli doku devriyesi yapar, artık maddeleri temizler ve bağlantıları ince ayarlarlar. Dorsal kolon miyelini yaşla birlikte bozuldukça, bu mikroglialar görünüm ve davranış olarak farklılaşmaya başlıyor: bağışıklık aktivasyonu ile ilişkili genleri yukarı yönlü düzenliyorlar, içinde yağlı damlacıklar biriktiriyorlar ve daha fazla hasarlı miyelini yuttuklarına dair işaretler gösteriyorlar. Aynı zamanda, dorsal kolon doku ortamı TGFβ1 açısından güçlü şekilde zenginleşiyor; bu molekül mikrogliayı kısıtlı, doku koruyucu bir durumda tutmasıyla biliniyor. Mikrogliaların kendileri bu TGFβ1’in başlıca kaynağı gibi görünüyor; bu da stres sinyalleri artarken kendi davranışlarını dizginlemeye çalıştıklarını düşündürüyor.
Güvenlik Freni Bozulduğunda Ne Oluyor
Bu frenin ne kadar önemli olduğunu araştırmak için, araştırmacılar erişkin farelerin mikroglialarında TGFβ sinyalini genetik olarak devre dışı bıraktılar; ya TGFβ’yi algılamak için kullandıkları reseptörü kaldırdılar ya da TGFβ1 üretmelerini engellediler. Her iki durumda da sonuç çarpıcı bir şekilde benzer ve yüksek derecede lokalize oldu: dorsal kolon mikrogliaları aşırı çoğaldı, yüksek oranda aktive oldu ve yutulmuş miyelinle dolu köpüksü bir görünüm aldı. Bu bölgedeki miyelin sıyrıldı, aksonlar dejenerasyon belirtileri gösterdi ve farelerde özellikle yaşlandıkça hareket ve koordinasyon bozuklukları kötüleşti. Diğer omurilik bölgeleri çok daha az etkilendi; bu da bu yola özgü bölge bağımlılığını ortaya koyuyor.
Özgün Bir Mikroglial Alt Tip ve Stres Altındaki Miyelin Üreticileri
Tek çekirdek RNA sekanslaması ekipçe hastalık ilerledikçe hücre türlerini kataloglamayı sağladı. TGFβ sinyali kaldırıldığında dramatik biçimde genişleyen belirgin bir mikroglia alt kümesi keşfettiler — bunlara TGFβ‑duyarlı mikroglia denildi. Bu hücreler, güçlü inflamatuar yanıtlar, yoğun miyelin yeme ve lipid işleme ile ilişkili genleri yüksek düzeyde ifade ediyordu ve dorsal kolonda yoğunlaşıyordu. Aynı zamanda, olgun miyelin üreten hücreler olan oligodendrositlerin popülasyonu değişti. Sağlıklı alt tipler azaldı, o esnada hasarlı dorsal kolonda genişleyen bir “hastalık‑ile ilişkili” oligodendrosit grubu belirdi ancak fonksiyonel miyelin yeniden inşa etmeyi başaramadı; görünürde bir onarım girişimi olmasına rağmen aksonlar açıkta kaldı.
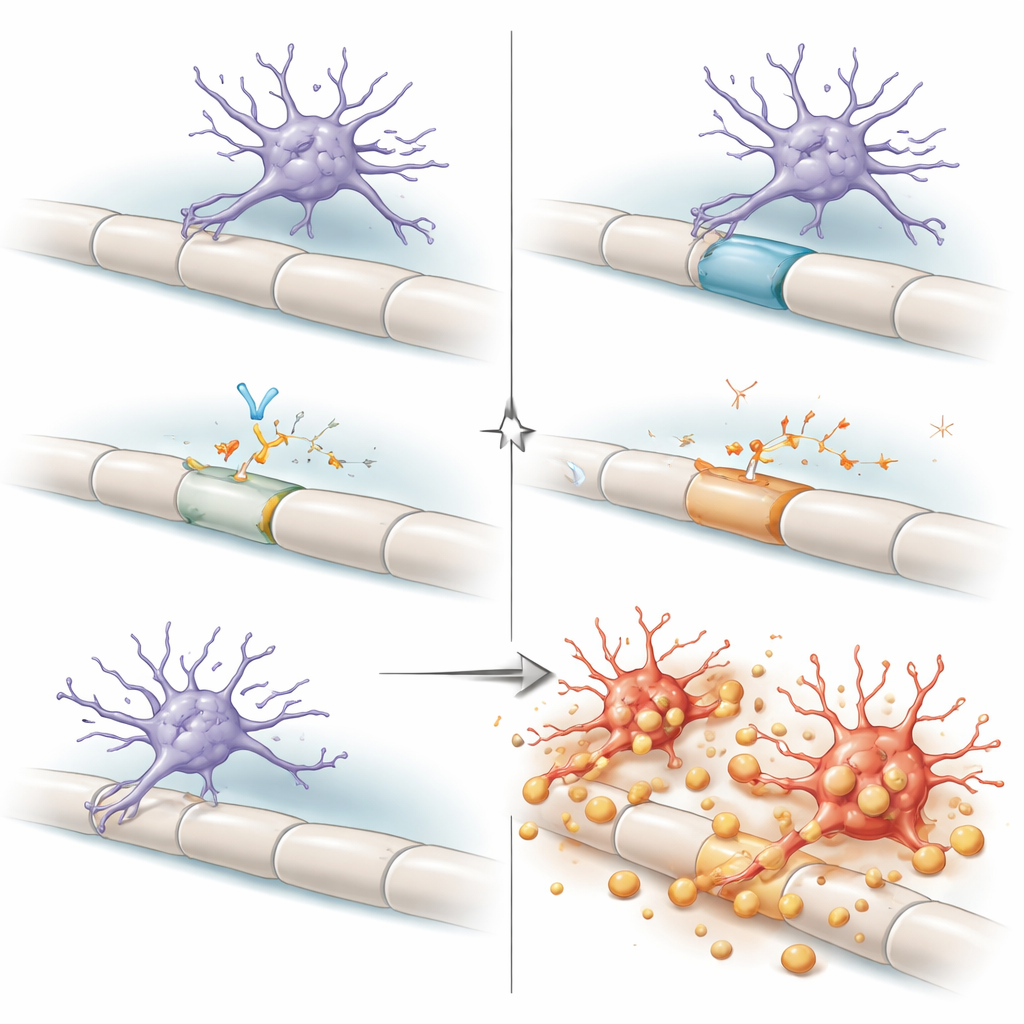
Yaşlanma ve Gelecek Tedaviler için Çıkarımlar
Bir arada değerlendirildiğinde bulgular, dorsal kolonu yaşlanan miyelin ve aşırı zorlanan destek hücrelerinin mikrogliayı bir eşik noktasına ittiği yüksek stresli bir mahalle olarak çiziyor. Normal koşullarda, mikrogliaların kendi TGFβ1’lerini ürettiği ve algıladığı otokrin bir döngü onları “hazır ama dayanıklı” bir durumda tutar; böylece devam eden artıklarla başa çıkabilirler ve nispeten sağlam miyeline saldırmazlar. Bu döngü bozulduğunda mikroglialar uyumsuz bir moda kayar, miyelini agresifçe sıyırır ve nörolojik gerilemeye yol açar. Halk için ana mesaj, beynin bağışıklık hücrelerinin basitçe iyi veya kötü olmadığıdır; davranışları büyük ölçüde yerel kablolama taleplerine ve TGFβ gibi moleküler frenlere bağlıdır. TGFβ engelleyici ilaçlar kanser ve bazı beyin hastalıkları için geliştirilirken, bu çalışma önemli bir uyarı getiriyor: özellikle yaşlılarda bu yolun bozulması, mikrogliaları sinirlerimizin işlevi için gereken yalıtıma saldırmak üzere serbest bırakarak savunmasız omurilik bölgelerine istemeden zarar verebilir.
Atıf: Zhu, K., Liu, Y., Min, JH. et al. TGFβ signaling mediates microglial resilience to spatiotemporally restricted myelin degeneration. Nat Neurosci 29, 617–631 (2026). https://doi.org/10.1038/s41593-025-02161-4
Anahtar kelimeler: mikroglia, miyelin yaşlanması, omurilik dorsal kolon, TGF beta sinyalleşmesi, nöroenflamasyon