Clear Sky Science · tr
DECODE: çeşitli omik veriler için derin öğrenmeye dayalı ortak dekonvolüsyon çerçevesi
Bu araştırma neden önemli
Modern biyomedikal alan, dokularımızın hangi genlerinin etkin olduğu, hangi proteinlerin bulunduğu ve hangi küçük moleküllerin hücrelerimizi beslediği gibi çok sayıda ölçümle dolu. Ancak bu ölçümlerin çoğu, birçok hücre tipinin karıştığı toplu örnekler üzerinde yapılıyor. DECODE çalışması, bu sinyalleri çözebilen güçlü bir yapay zeka çerçevesi sunuyor; farklı veri türleri arasında bile hangi hücrelerin ve hücre durumlarının bulunduğunu ortaya çıkarabiliyor. Bu yetenek, kanser, bağışıklık ve metabolik hastalık araştırmalarını hızlandırabilir ve mevcut biyobank örneklerinden daha verimli yararlanmayı sağlayabilir.
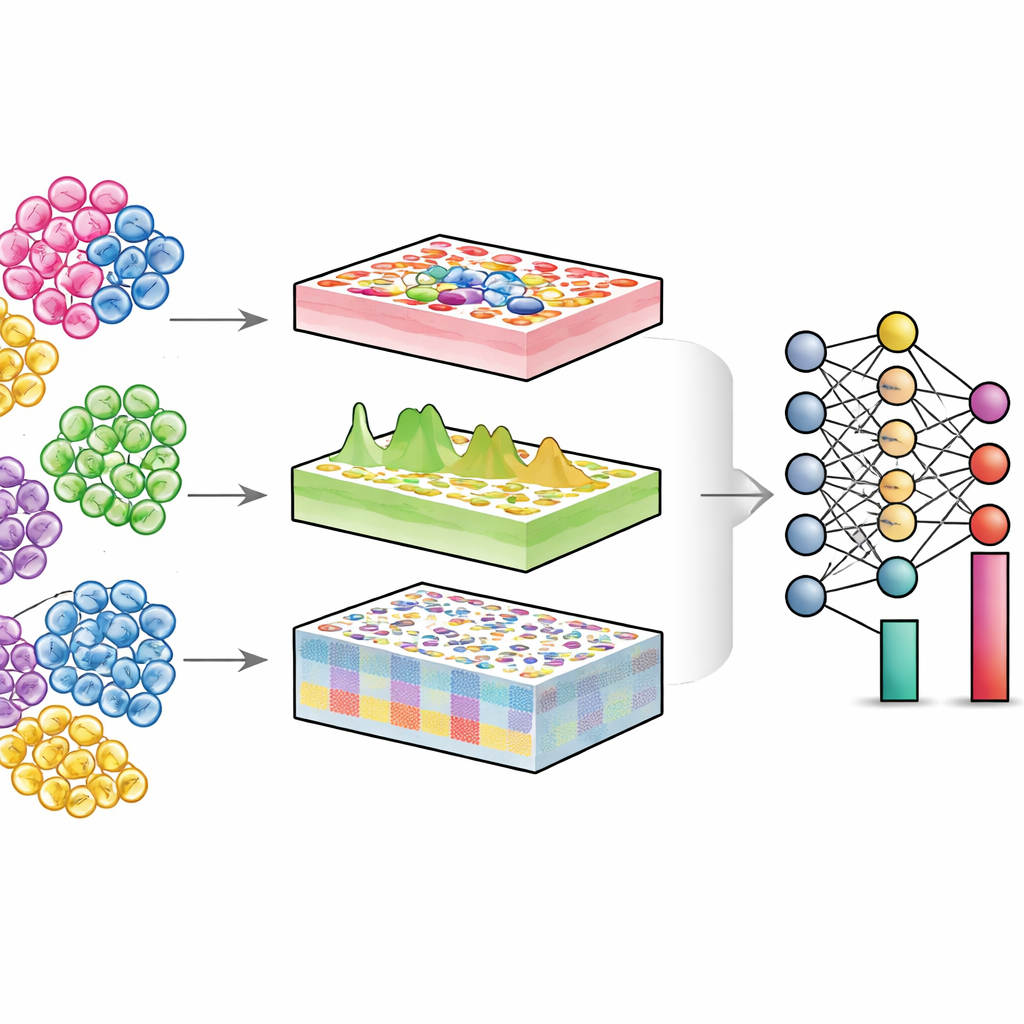
Karışık dokuların içine bakmak
Her organ, bağışıklık hücreleri, yapısal hücreler, kök hücreler ve daha fazlasını içeren farklı hücre tiplerinin bir topluluğudur. Sağlıkta ve hastalıkta değişen genellikle sadece her hücrenin yaptığı iş değil, aynı zamanda her hücre tipinin ne kadar bulunduğu ve hangi durumda olduğudur. Tek hücre teknolojileri bireysel hücreleri doğrudan ölçebilir, ancak büyük hasta kohortları veya uzun süre depolanmış örnekler için pahalı ve teknik olarak zordur. Buna karşılık geleneksel “toplu” deneyler binlerce veya milyonlarca hücreyi karıştırır ve ortalama bir sinyal okur. Dekonvolüsyon algoritmaları bu karışımı tersine çevirmeye çalışır: toplu veriler ve tek hücre referansı verildiğinde dokudaki her hücre tipinin oranını tahmin ederler.
Tek numaraya dayalı araçların sınırları
Mevcut dekonvolüsyon araçları çoğunlukla gen aktivitesi (transkriptomik) veya proteinler (proteomik) gibi tek bir ölçüm türüne göre özelleşmiştir. Genellikle diğer veri türleri için geçerli olmayan belirli istatistiksel varsayımlarda bulunurlar ve toplu dokuda referans veride eksik olan hücre tipleri olduğunda zorlanırlar. Donörler, cihazlar veya sağlık durumlarındaki farklılıklardan kaynaklanan güçlü batch etkileri biyolojik sinyalleri daha da bulanıklaştırabilir. Özellikle, klinik semptomlara en yakın olan küçük moleküllerin incelendiği metabolomik için pratik bir yöntem yoktu. Sonuç olarak, çokluomik kohortları analiz eden bilim insanları, her birinin kendine özgü özellikleri olan birkaç özel araçla uğraşmak zorunda kalıyordu; bu da çalışmalar ve veri türleri arasında karşılaştırmayı zorlaştırıyordu.
Evrensel bir ayırma motoru
DECODE, dekonvolüsyonu genleri, proteinleri ve metabolitleri birleşik bir şekilde işleyebilen esnek bir derin öğrenme problemi olarak ele alarak bu zorlukların üstesinden geliyor. Önce tek hücre profillerini rastgele oranlarda dijital olarak karıştırarak “sahte dokular” sentezliyor; böylece gerçek hücre kompozisyonunun bilindiği zengin bir eğitim seti oluşturuyor. Ardından bir düşmanca öğrenme aşaması, bir kodlayıcının gerçek dokuları ve sahte dokuları teknik farklılıkların minimize edildiği ama biyolojik açıdan anlamlı desenlerin korunduğu ortak bir temsile eşlemesini öğretiyor. Sonra kontrastif öğrenme ile yönlendirilen özel bir gürültü giderme modülü, gerçek doku sinyallerini yapay gürültüden ayırmayı öğreniyor. Bu adım, DECODE’u referans veride eksik hücre tiplerine ve ölçüm hatalarına karşı dayanıklı kılıyor. Son olarak, temizlenmiş özellikler, referansın ne kadar eksiksiz olduğuna bağlı olarak hücre tiplerinin ve hücre durumlarının mutlak veya göreli bolluklarını tahmin eden bir dekonvolüsyon modülüne aktarılıyor.
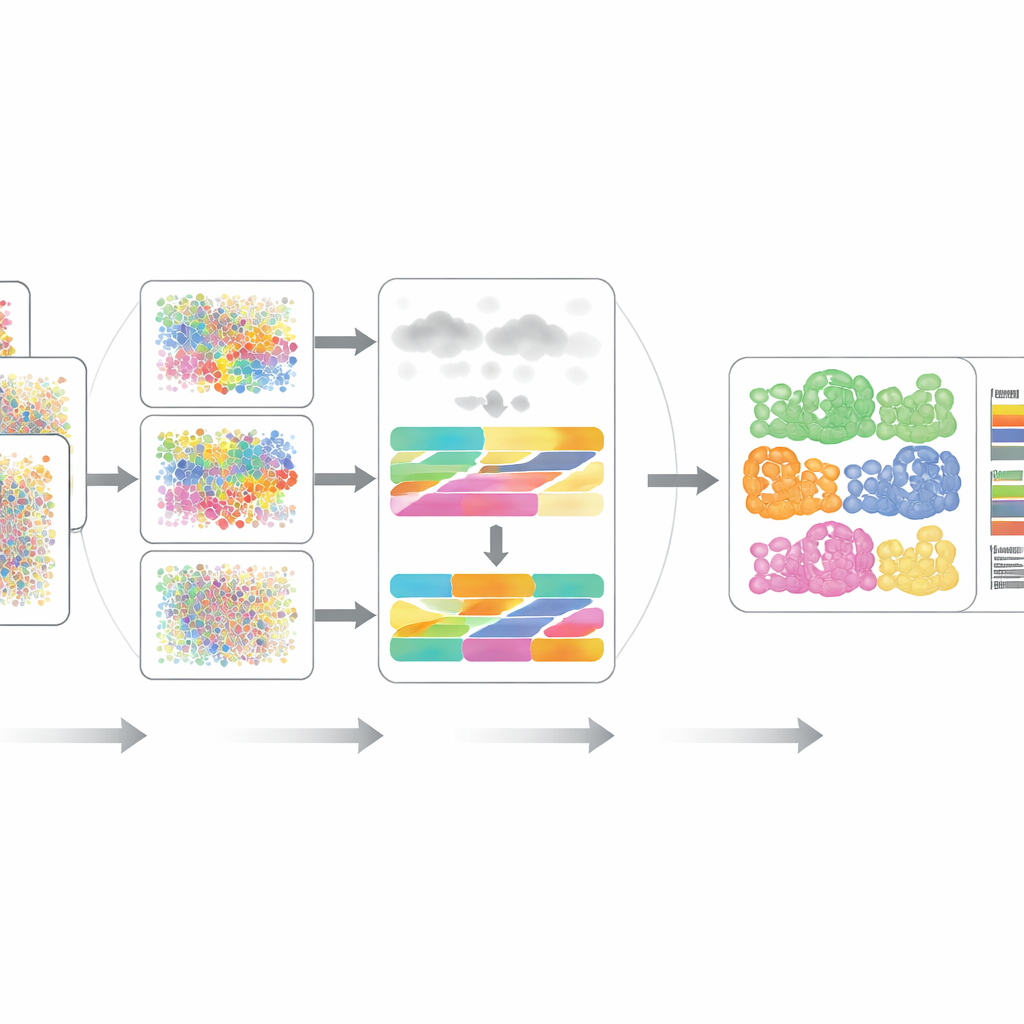
DECODE’u teste sokmak
Yazarlar, DECODE’u farklı donörler, hastalık durumları, sağlık koşulları, deneysel platformlar ve hatta mekansal olarak çözünür ölçümler dahil olmak üzere yedi gerçekçi senaryoyu kapsayan 15 veri kümesinde titizlikle değerlendirdiler. Transkriptomik ve proteomik boyunca DECODE, doğruluk açısından genelde en son teknoloji araçlara eşit veya onlardan üstün performans gösterirken makul hesaplama zamanı ve bellek kullanımı sağladı. Kritik olarak, DECODE metabolomik verilerde güvenilir sonuç veren tek yöntemdi; burada özellik sayısı daha az ve farklı hücre tipleri yanıltıcı şekilde benzer görünebiliyor. Çerçeve ayrıca yalnızca statik hücre tiplerini değil, gelişim yolculuğu boyunca ilerleme, hücre döngüsünün evreleri veya ilaç tedavisine verilen yanıtlar gibi hücre durumlarını izlemek konusunda da yetkin olduğunu gösterdi.
Gürültülü ve eksik gerçek dünya verilerinde dayanıklılık
Gerçek dokular genellikle laboratuvar tabanlı tek hücre referanslarında yakalanmayan hücre tipleri içerir ve deneysel gürültü birçok özelliği aynı anda bozabilir. Araştırmacılar bu sorunları bilinmeyen hücre tipleri ekleyerek ve transkriptomik, proteomik ve metabolomik boyunca çeşitli gürültü ve eksik veri türlerini tanıtarak simüle ettiler. Çoğu durumda DECODE en doğru yöntem olmayı sürdürdü ve metabolomikte çökmeyen tek yöntem oldu. Ayrıca, DECODE’un aynı kan hücresi örneklerinden alınan eşleştirilmiş gen ve protein ölçümlerine uygulandığında yüksek tutarlılık sağladığını gösterdiler; bu, büyük kohortlarda omik katmanlar arasında hücre tipi değişikliklerini karşılaştırmak için önemli bir gerekliliktir.
Çokluomik kohortlardan yeni biyolojik içgörüler
Bu birleşik araçla donanmış ekip, karmaşık hastalık veri setlerini yeniden inceledi. Meme kanserinde, immün hücrelerin ve destekleyici stromal hücrelerin metastaz yapmayan tümörler, metastaz yapan primer tümörler ve beyin metastazları arasında nasıl değiştiğini göstermek için transkriptomik ve proteomik kohortları birleştirdiler. Metastaz yapmayan lezyonlarda daha yüksek T hücresi ve perivasküler benzeri hücre bolluğu ile ileri hastalıkta artan B hücreleri gibi desenler önceki biyolojik çalışmaları destekliyor ve genişletiyor. Fare karaciğerinde DECODE, hepatositler, endotel hücreler ve yerleşik bağışıklık hücrelerinin farklı diyetler ve karaciğer hastalığı modelleri altında nasıl değiştiğini izlemek için transkriptomik, proteomik ve metabolomik kohortları entegre etti; inflamatuar durumlarda artan Kupffer hücresi oranları gibi bilinen eğilimleri yeniden yakaladı.
İleriye dönük ne anlama geliyor
Günlük okura yönelik ana mesaj şu: DECODE, biyomedikal veriler için akıllı bir prizma gibi işlev görüyor—dokulardan alınan karışık ölçümler verildiğinde birçok farklı hücre tipi ve durumu ayırabiliyor ve bunu çeşitli moleküler okumalarda güvenilir şekilde yapıyor. Bu, bilim insanlarının her proje için yeni tek hücre verisi toplamadan mevcut çokluomik kohortlardan ve biyobankalardan çok daha fazla bilgi çıkarmasını sağlıyor. Yöntem hâlâ mevcut tek hücre referanslarının kalite ve kapsamına bağlı olmakla birlikte ve metabolomik kaynaklar sınırlı kalmaya devam etse de, DECODE büyük ölçekli insan çalışmalarının rutin hücre düzeyinde yorumlanmasına doğru anlamlı bir adımı temsil ediyor; bu da hastalık mekanizmalarını anlamak ve hassas tıbbı yönlendirmek için potansiyel faydalar sunuyor.
Atıf: Zhao, T., Liu, R., Sun, Y. et al. DECODE: deep learning-based common deconvolution framework for various omics data. Nat Methods 23, 596–608 (2026). https://doi.org/10.1038/s41592-026-03007-y
Anahtar kelimeler: çokluomik dekonvolüsyon, tek hücre referansı, biyolojide derin öğrenme, metabolomik analizi, hücre tipi kompozisyonu