Clear Sky Science · tr
Multimodal antijenik kaçış: GPRC5D hedefli T hücre bağlayıcılarına karşı multipl miyelom
Kanser Hassas İmmünoterapiden Nasıl Üstün Gelir
Yeni, güçlü bağışıklık tabanlı ilaçlar multipl miyelom tedavisini dönüştürüyor; bu kanser çoğu hasta için hâlâ kür sağlamıyor. Bu tedaviler, vücudun kendi T hücrelerini tümör hücrelerini hedefleyen yüzey “işaretlerine” doğru yönlendirerek çalışır. GPRC5D adlı molekül, umut verici bir işaret olarak ortaya çıkmıştır. Ancak birçok hedefe yönelik tedavide olduğu gibi tümörler evrilip tedaviden kurtulabilir. Bu çalışma, miyelom hücrelerinin GPRC5D işaretini değiştirerek veya gizleyerek güçlü T hücreyi yönlendiren ilaçlardan nasıl kaçtığını olağanüstü ayrıntıyla ortaya koyuyor.
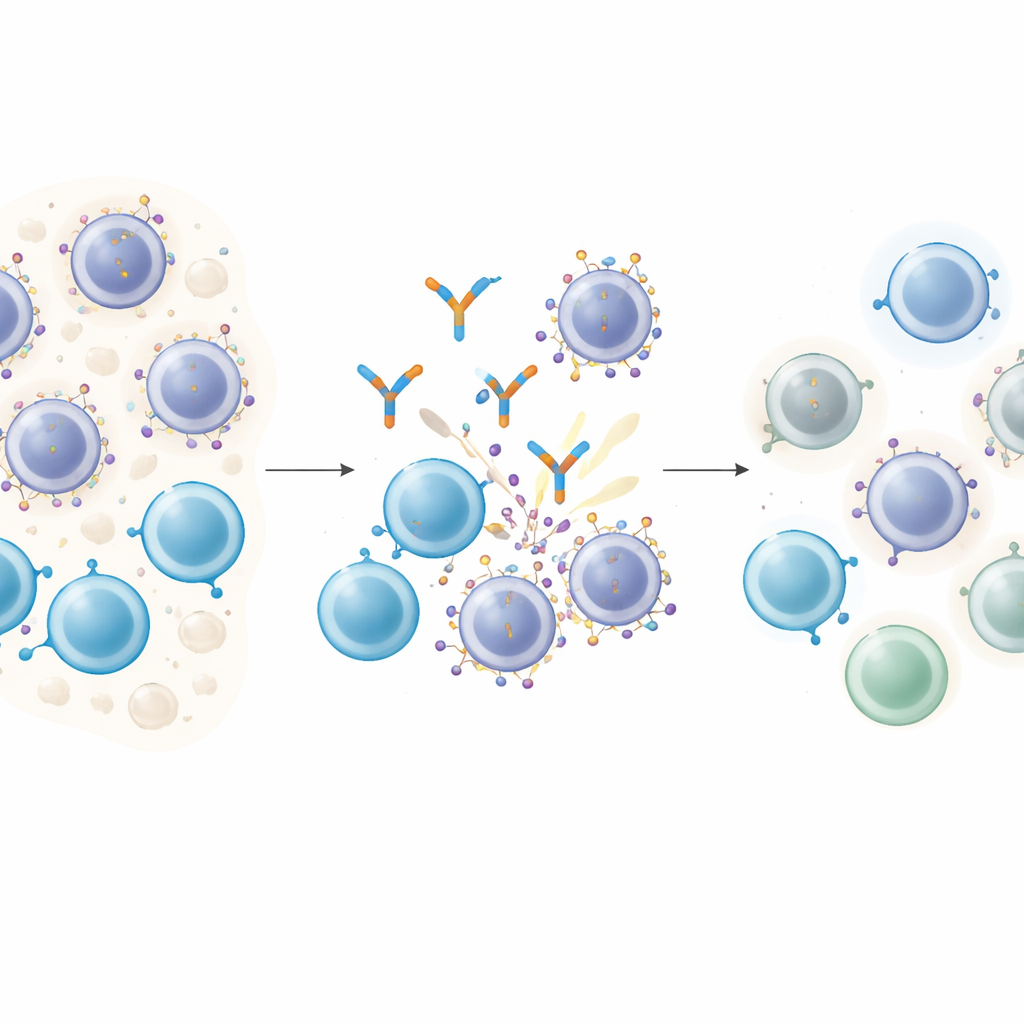
Akıllı İlaçlar Kanser Hücrelerine Nasıl Tutunur
T hücre bağlayıcı antikorlar moleküler çöpçatanlar gibidir: bir uç T hücresini yakalar, diğer uç kanser hücresindeki hedef moleküle tutunur ve böylece T hücresi ile hedef doğrudan temas eder, T hücresi avını öldürebilir. Multipl miyelomda GPRC5D, kötü huylu plazma hücrelerinde bol bulunup çoğu normal dokuda az olduğu için çekici bir hedeftir. Talquetamab adlı GPRC5D yönelimli ilaçla tedavi edilen hastalarda sıklıkla derin remisyonlar görülür. Ancak neredeyse hepsi sonunda nüks eder; bu da hayati bir soruyu gündeme getirir: Kanser hücreleri bu ilaçların dayandığı hedefi değiştiriyor mu?
Tümör Evrimini Gerçek Zamanlı İzlemek
Araştırmacılar, talquetamab alan ve tedavisi zor 21 miyelomlu hastayı izledi. Bazı hastalardan tedavi öncesi, bazılarından ise kanser geri döndüğünde kemik iliği örnekleri alındı ve tümör hücreleri DNA, RNA ve kromatin analizlerinin birden fazla katmanıyla incelendi. Bu ultra-ayrıntılı görünüm, nüks eden hastaların yaklaşık üçte ikisinde kanserin ilacın etkisini azaltacak veya engelleyecek şekilde GPRC5D’yi değiştirdiğini ortaya koydu. Çarpıcı biçimde, genetik olarak farklı birkaç direnç alt klonu sıklıkla aynı kişide bir arada bulundu; bu da kaçış yönüne doğru evrimin aynı anda birden çok yoldan ilerleyebildiğini gösteriyor.
Tümörlerin Hedefi Gizlemesinin Üç Ana Yolu
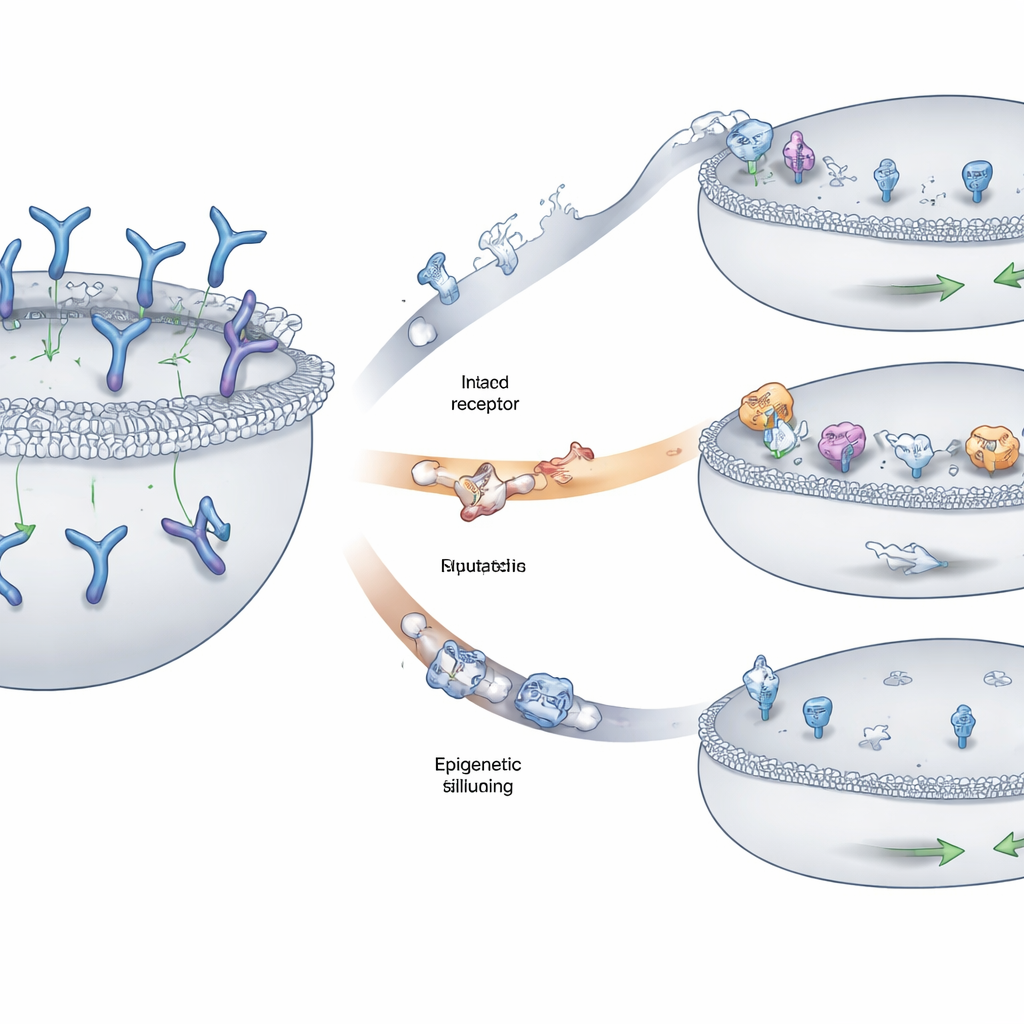
Ekip, miyelom hücrelerinin tanınmaktan kaçınmasına yol açan üç tekrar eden desen buldu. Bazı hastalarda GPRC5D genini taşıyan kromozom parçaları her iki kopyada da silinmiş, böylece hücre yüzeyindeki işaret tamamen yok olmuştu. Diğerlerinde, tek bazlı DNA değişimleri veya küçük ekleme/silinmeler gibi daha küçük değişiklikler GPRC5D proteininin kilit bölgelerini bozmuştu. Bu değişikliklerin birçoğu, proteinin hücre içinden dış zarına doğru doğru şekilde taşınması için gerekli parçaları bozarak GPRC5D’nin ilaç tarafından görülecek yerde değil hücre içindeki bir bölmede takılı kalmasına neden oldu. Üçüncü yol epigenetik susturmaydı: GPRC5D çevresindeki DNA sıkı paketlendi ve kimyasal işaretlendi, böylece genin okunması neredeyse durdu; altta yatan dizi ise büyük ölçüde sağlam kaldı. Bu stratejiyi kullanan tümör hücreleri çok az veya hiç GPRC5D üretmiyordu.
İşaret Varsa da Kilit Artık Uymuyorsa
Tüm kaçış yolları GPRC5D’yi hücre yüzeyinden kaldırmıyordu. Bazı vakalarda protein standart laboratuvar testlerine normal görünüyordu ama artık ilaca bir kilit-anahtar gibi uymuyordu. Ekip, hasta kaynaklı spesifik mutasyonları laboratuvar hücre dizilerinde yeniden yarattı ve farklı GPRC5D hedefli antikorların bu hücrelere ne kadar bağlanıp öldürebildiğini test etti. Bir mutasyon, talquetamab’ın reseptöre tuttuğu tam noktayı ince bir şekilde değiştirerek ilacın bağlanma ve hücre ölümünü tetikleme yeteneğini keskin biçimde azalttı; oysa reseptör rutin boyamalarla hâlâ görünüyordu. İlginç biçimde, reseptöre iki noktadan tutunan farklı bir GPRC5D yönelimli ilaç, bu mutantların birkaçına karşı etkisini korudu; bu da ilaç tasarımının —örneğin çokvalent veya çok-epitop bağlanma kullanmanın— dirençli klonların hayatta kalıp kalmayacağını etkileyebileceğini vurguluyor.
Hedefin Ötesinde: İmmün Saldırının Diğer Sınırları
Çoğu nüks vakası GPRC5D kaybı veya değişikliğinin bir formunu gösterse de, azınlık bir hasta grubu hedefin kendisinde belirgin değişiklik olmaksızın nüks etti. Bu durumlarda sorun T hücrelerinde görünüyordu: laboratuvar testlerinde daha az formdaydılar ve kanser hücrelerini öldürme kapasiteleri azalmıştı; bu, uzun süreli sürekli engager tedavisine maruz kalmanın immün sistemi tüketebileceğini düşündürüyor. Çalışma ayrıca belirli bir genetik miyelom alt tipinin (t(11;14) adlı kromozomal değişimi içeren) GPRC5D genini daha “kapalı” bir kromatin durumunda doğal olarak tuttuğunu ve başlangıçta daha düşük ifade düzeylerine yol açtığını ortaya koydu. Bu, bazı hastaların tümörleri hedef işaretin baştan zayıf düzeyde olması nedeniyle kötü yanıtlara yatkın olabileceği ihtimalini gündeme getiriyor.
Hastalar ve Gelecek Tedaviler İçin Anlamı
Hastalar ve klinisyenler için bu çalışma, neden son derece etkili GPRC5D hedefli terapilerin henüz kür sağlamadığını açıklıyor: miyelom hücreleri, bu ilaçların dayandığı işareti silebilir, yeniden düzenleyebilir, yanlış yönlendirebilir veya kapatabilir ve genellikle bunu birden çok yolla aynı anda yaparlar. Bulgular, standart laboratuvar testlerinin kaçırabileceği yeni kaçış mutasyonlarını tespit etmek için sadece protein seviyelerini ölçmek yerine tümör DNA’sını izlemenin önemli olacağını öne sürüyor. Ayrıca birden fazla bölgede daha güçlü bağlanan ilaçlar, aynı anda birden çok hedefi vuran kombinasyonlar veya susturulmuş genleri yeniden açan ajanlar gibi yeni nesil stratejilere işaret ediyor; bunlar tümör evrimine karşı önde kalmak için tasarlanabilir. Özetle, bu çalışma miyelomun kullandığı kaçış yollarını haritalandırıyor, böylece gelecekteki tedaviler bunları engelleyecek şekilde geliştirilebilsin ve T hücre tabanlı tedaviler daha uzun süre etkili kalsın.
Atıf: Lee, H., Ahn, S., Gonzales, G.A. et al. Multimodal antigenic escape to GPRC5D-targeted T cell engagers in multiple myeloma. Nat Med 32, 964–977 (2026). https://doi.org/10.1038/s41591-025-04175-8
Anahtar kelimeler: multipl miyelom, T hücre bağlayıcıları, GPRC5D, antijen kaçışı, kanser immünoterapisi