Clear Sky Science · tr
Flt3L aracılığıyla tümörde cDC1 genişlemesi, lenf düğümlerinde kök‑benzeri CD8+ T hücrelerini hazırlayarak immünoterapinin etkinliğini artırır
Bağışıklık Sisteminin Kanserle Nasıl Savaşacağını Hatırlamasına Yardım Etmek
Neden bazı insanların tümörleri modern immünoterapiyle kaybolurken bazılarında az veya hiç fayda görülmüyor? Bu çalışma, bu soruya yanıt aramak için bağışıklık sisteminin içini inceliyor. Araştırmacılar, tümörlerde belirli bir nöbetçi hücre grubunu güçlendirerek, yakın lenf düğümlerinde uzun ömürlü, “kök‑benzeri” katil T hücreleri rezervi oluşturabildiklerini gösteriyor. Bu hücreler de standart kontrol noktası ilaçlarının, özellikle anti‑CTLA‑4 tedavisinin, daha güçlü ve daha uzun süreli çalışmasını sağlıyor.
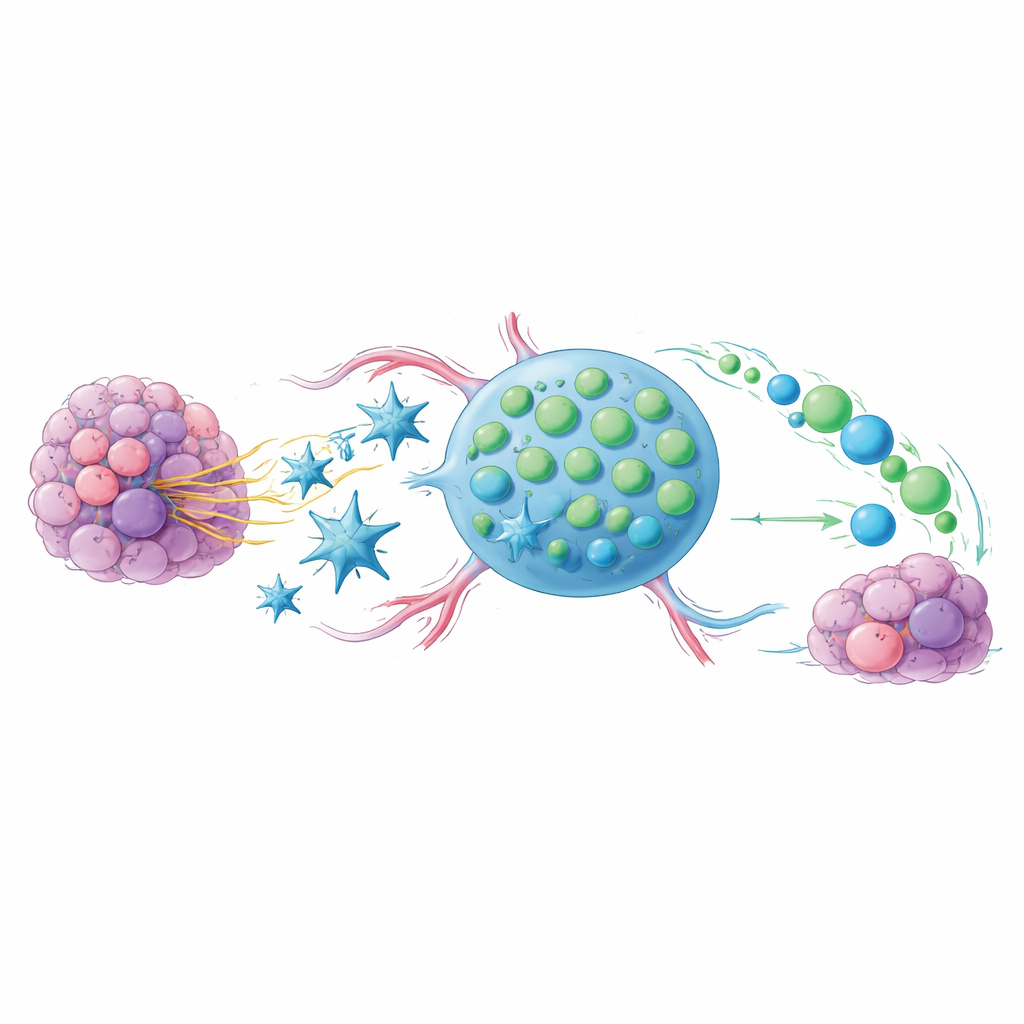
Yorgun Tümör‑Savaşçı Hücrelerin Sorunu
Anti‑PD‑1 ve anti‑CTLA‑4 gibi kontrol noktası ilaçları, bağışıklık hücrelerini kanserle savaşmaya serbest bırakır, ama yalnızca hastaların bir kısmında iyi sonuç verir. Bir ipucu, enfekte veya kanserli hücreleri yok eden ana hücreler olan CD8 T hücrelerinin durumunda yatıyor. Bu T hücreleri çok uzun süre çok fazla zorlandığında, tükenmiş, “exhausted” bir duruma girip etkin olarak çoğalamaz hale gelebilir. Ancak daha küçük bir alt grup, daha genç ve kök‑benzeri bir karakteri korur: kolay bölünür, yeni savaşçılar üretir ve kontrol noktası tedavisi gören kişilerde iyi yanıtlarla güçlü şekilde bağlantılıdır. Bu çalışmanın temel sorusu, tümörleri ve çevresini bu kök‑benzeri hücrelerin alevlenmiş hallerine tercih verecek şekilde nasıl yönlendireceğidir.
Tümörün Nöbetçi Hücrelerini Süper Şarj Etmek
Çalışma ekibi, tümör parçalarını T hücrelerine sunmada usta, nadir ama güçlü bir bağışıklık nöbetçi sınıfı olan konvansiyonel tip 1 dendritik hücrelere (cDC1) odaklandı. Bu hücreleri fare tümörleri içinde genişletmek için Flt3 ligandı (Flt3L) adlı bir büyüme sinyalini kullandılar; bunu ya kanser hücrelerini salgılayacak şekilde genetik olarak düzenleyerek ya da ilaç olarak vererek sağladılar. Tek hücre RNA dizilemesi, Flt3L‑çağırışlı tümörlerin çok daha fazla dendritik hücre ve lenfosit içerdiğini ve daha az tümör hücresi barındırdığını gösterdi. Dendritik hücre grubunun içinde, lenf düğümlerine göç etmeye hazır, yüksek derecede olgun bir grup da dahil olmak üzere üç farklı alt grup genişledi. Aynı zamanda, bu tümör içindeki CD8 T hücreleri terminal tükenmiş profilinden kök‑benzeri veya bellek‑benzeri bir duruma doğru kaydı.
Lenf Düğümünde Kök‑Benzeri T Hücre Rezervi Kurmak
Tümör‑özgü T hücrelerini izleyerek ve genetik araçlar kullanarak, araştırmacılar Flt3L tedavisinin yüzey belirteçleri kök‑benzeri potansiyel ve aktif bölünme ile ilişkili CD8 T hücre popülasyonunu artırdığını gösterdi. Bu hücreler XCR1‑pozitif dendritik hücrelere ve dendritik hücrelerin tümörden drenaj yapan lenf düğümüne CCR7 rehberliğinde hareketine bağlıydı. Dendritik hücreler yok edildiğinde veya göçleri engellendiğinde kök‑benzeri T hücre havuzu küçüldü. Lenf düğümlerinden lenfosit çıkışını engellemek benzer bir etki yarattı; yenilenmiş T hücre arzını tümöre kesti. Moleküler profilleme, bu sürecin Myb transkripsiyon faktörüne dayandığını ve tümör hedeflerini nispeten düşük‑güçte tanıyan T hücrelerini tercih ettiğini ortaya koydu; bu tür hücrelerin kalıcı kanser kontrolü için giderek daha önemli olduğu kabul ediliyor.
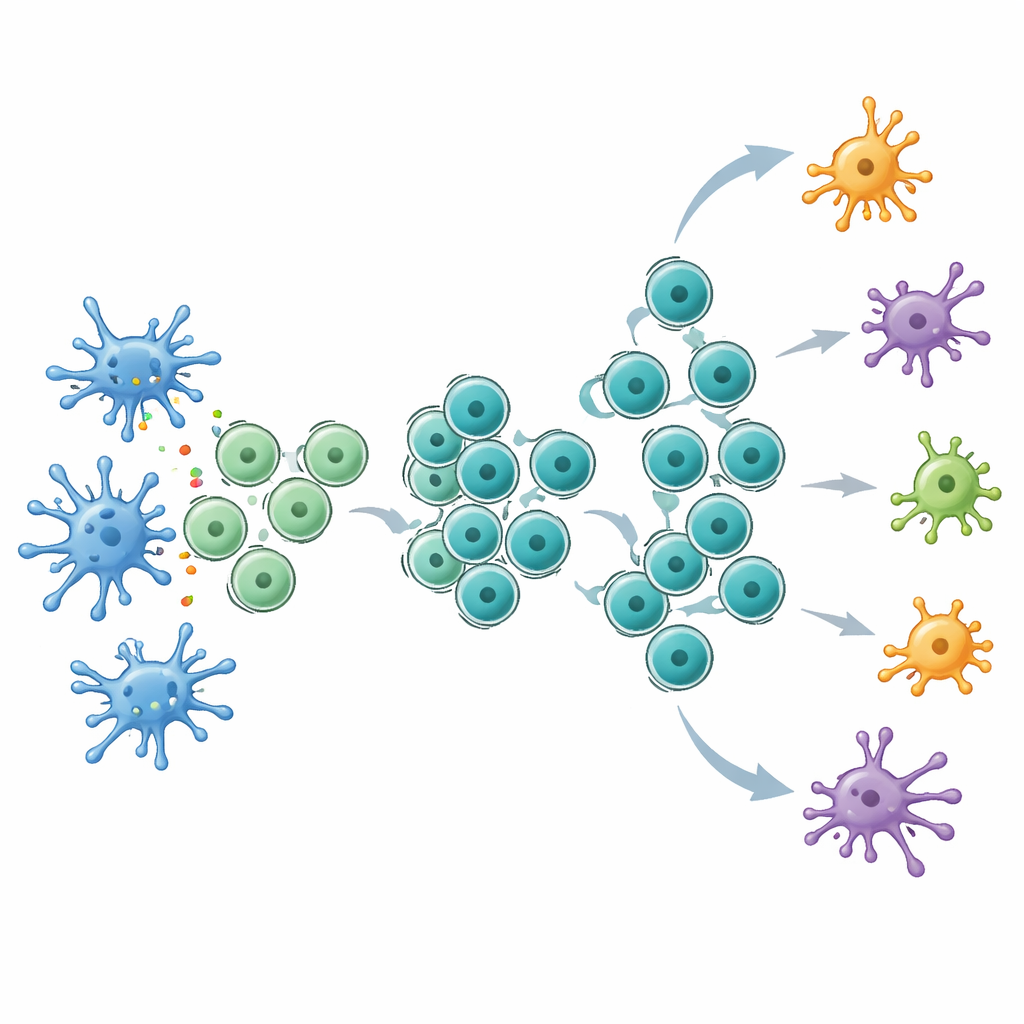
Kontrol Noktası Terapisini Daha Etkin Hale Getirmek
Bu genişletilmiş kök‑benzeri T hücre rezerviyle donanmış fareler, özellikle anti‑CTLA‑4 tedavisine karşı kontrol noktası blokajına çok daha iyi yanıt verdi. Flt3L ile tedavi edilen hayvanlardaki tümörler daha fazla küçüldü, sağkalım iyileşti ve kan ile lenf düğümlerinde daha fazla tümör‑özgü T hücre bulundu. Tümörlerde Flt3L, kök‑benzeri CD8 hücrelerini artırırken, ardından uygulanan CTLA‑4 blokajı bu hücreleri güçlü etkileyicilere olgunlaştırarak önemli anti‑tümör moleküllerinin yüksek düzeyde üretimine yol açtı. T hücresi reseptörlerinin dizilenmesi, kombine tedavinin genişleyen T hücresi klonlarının çeşitliliğini artırdığını, birçok alt‑dominant klonu da kapsadığını gösterdi; bu da kansere karşı daha çeşitli bir saldırı öneriyor. Ayrıntılı tek hücre analizi, IL‑21 bağışıklık habercisi reseptörünü ifade eden, kök‑benzeri ile tükenmiş durumlar arasında yer alan ve hem erken hem de geç popülasyonlarla T hücresi reseptörlerini paylaşan benzersiz bir CD8 T hücre kümesi ortaya çıkardı. IL‑21 sinyalinin blokajı, Flt3L ile anti‑CTLA‑4 kombinasyonunun yararlarını zayıflattı.
Geleceğin Kanser Tedavileri İçin Bunun Anlamı
Bir halk okuyucusu için çıkarım, başarılı immünoterapinin yalnızca bağışıklık sistemini daha sert zorlamaya bağlı olmadığı, aynı zamanda doğru tür hücrelere sahip olmak gerektiğidir. Bu çalışma, dendritik hücreleri Flt3L ile beslemenin ve yönlendirmenin, yakın lenf düğümlerini yenilenebilir bir kök‑benzeri katil T hücreleri havuzuyla doldurabileceğini gösteriyor. Ardından anti‑CTLA‑4 gibi kontrol noktası ilaçları uygulandığında, bu rezervden yararlanarak daha fazla, daha çeşitli ve tümörleri daha iyi kontrol edebilen yeni dalgalar halinde savaşçılar üretilebiliyor. İnsan kanseri veri setlerinin analizleri, bu yolla ilişkili gen imzalarının hastalarda daha iyi sonuçları öngördüğünü düşündürüyor. Birlikte ele alındığında, bu bulgular önce Flt3L gibi ajanlarla doğru bağışıklık hücresi “tohum stokunu” inşa edip sonra kontrol noktası ilaçlarıyla serbest bırakan kombinasyon tedavilerine işaret ediyor; bu da daha güçlü ve daha kalıcı kanser kontrolü vaat ediyor.
Atıf: Lai, J., Chan, C.W., Armitage, J.D. et al. Flt3L-mediated tumor cDC1 expansion enhances immunotherapy by priming stem-like CD8+ T cells in lymph nodes. Nat Immunol 27, 530–542 (2026). https://doi.org/10.1038/s41590-026-02419-4
Anahtar kelimeler: kanser immünoterapisi, dendritik hücreler, kök‑benzeri CD8 T hücreleri, kontrol noktası engelleme, Flt3 ligandı