Clear Sky Science · tr
Fibroblast TGFβ sinyalleşmesinin mekânsal düzeni romatoid artritte tedavi direncinin altında yatar
İnatçı eklem ağrısı neden önemli
Birçok romatoid artrit hastası bağışıklık sistemini yatıştıran modern ilaçlar kullanmasına karşın eklemleri hâlâ ağrılı ve sert kalır. Bu çalışma, eklemdeki iltihap azalmış gibi görünse bile neden bazı hastaların düzelmediğini sorguluyor. Eklemin destek hücrelerinin nerede ve nasıl yara izi oluşturma programlarını etkinleştirdiğini yakından inceleyerek, araştırmacılar devam eden ağrıyı açıklayabilecek gizli bir hasar biçimini ortaya çıkarıyor ve yeni tedavi stratejilerine işaret ediyor.
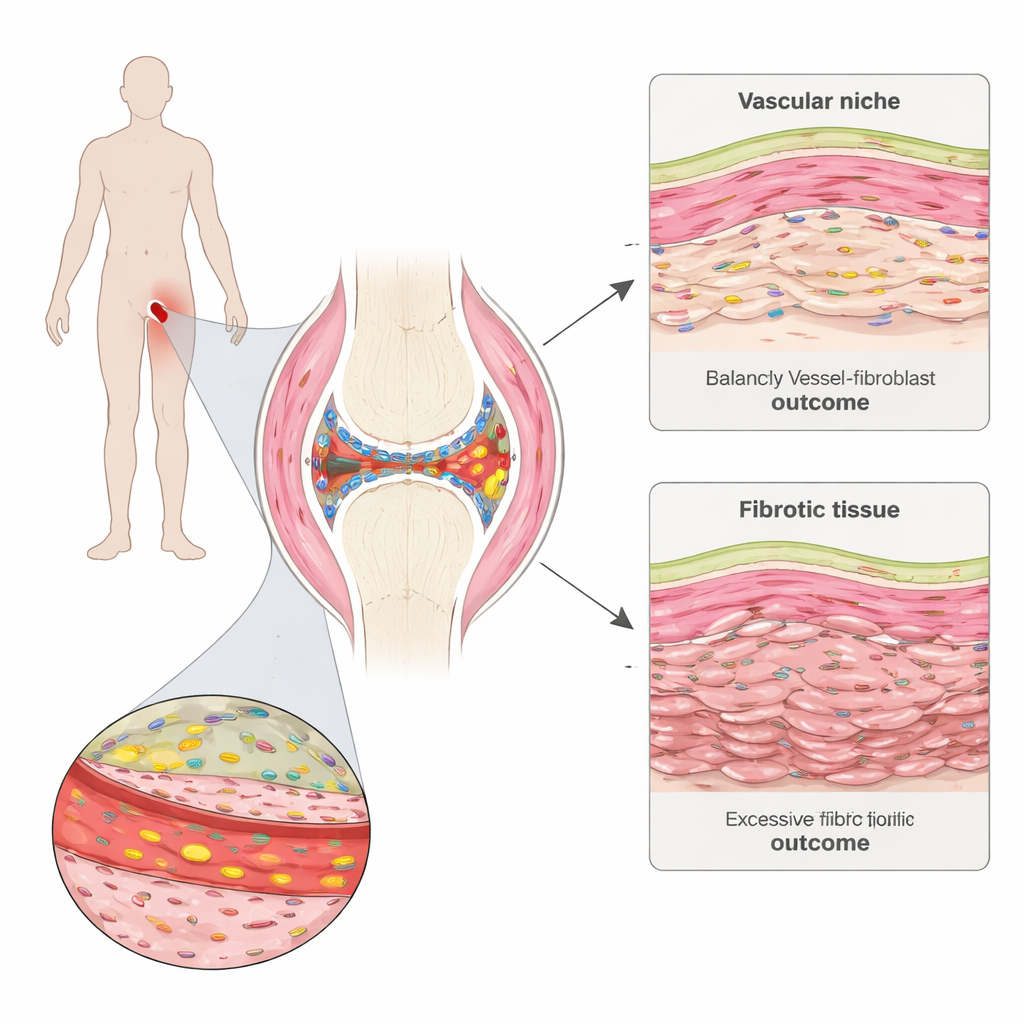
Ağrılı eklemin içini daha yakından görmek
Romatoid artrit, eklemleri çepeçevre saran ve yağlayan ince bir doku olan sinovyuma saldırır. Ekip, terapiye başlamadan önce ve altı ay sonra erken dönem hastalığı olan kişilerden küçük sinovyal biyopsiler aldı. Gelişmiş mekânsal gen haritalama kullanarak, bu hücrelerin dokuda hangi konumda kaldığını koruyarak binlerce tek tek hücrede hangi genlerin aktif olduğunu görebildiler. Bağışıklık hücresi kümeleri, yağ bakımından zengin alanlar, ince iç astar ve kan damarları ile yapısal hücreler olarak adlandırılan fibroblastlarla dolu bölgeler dahil olmak üzere sinovyumda farklı “mahalleler” tanımladılar.
Yara izi oluşturan hücreler ve tedavi direnci
Daha sonra remisyona giren hastalarla girmeyenleri karşılaştırdıklarında, araştırmacılar çarpıcı bir desen buldu: tedavi öncesinde remisyona girmeyen hastalarda çok daha güçlü doku skarlaşması ya da fibrozis işaretleri vardı. Özellikle COMP adlı bir ekstraselüler matriks proteininin yüksek üretimiyle işaretlenen belirli bir fibroblast programı bu hastalarda genişlemişti. Bu COMP bakımından zengin fibroblastlar, akciğer ve deri fibrozisinde görülen yara izi oluşturan hücrelerle benzer özellikler paylaşıyor ve kötü tedavi yanıtıyla en güçlü ilişkiyi gösteriyordu. Zamanla, bu hücrelerin hakim olduğu bölgeler hücresel olarak nispeten fakir ama bağlayıcı dokuyla yoğunlaşma eğilimindeydi; bu da iltihap geçse bile kalıcı olabilen sert bir matriks ürettiklerini düşündürüyor.
Gizli bir yönetici olarak kan damarları
Fibrojenez yapan fibroblastlar rastgele dağılmamıştı. Kan damarlarının etrafında kümelenmiş, katmanlı perivasküler zonlar oluşturuyorlardı. Damar duvarına en yakın iç katman dış katmandan farklı genler ifade ediyordu. Ekip, damarları kaplayan hücrelerin (endotelyal hücreler) yakınlardaki fibroblastlara Notch sinyalleri gönderdiğini ve bunun da bu fibroblastların TGF‑beta adı verilen yaraşı teşvik edici bir sinyal ailesine nasıl yanıt verdiğini şekillendirdiğini gösterdi. Damara yakın bölgede, Notch sinyalleşmesi fibroblastları TGF‑beta üretmeye itiyor ama aynı zamanda yüzeylerindeki TGF‑beta reseptörlerinin sayısını düşürerek duyarlılıklarını sınırlıyordu. Uzaklaştıkça, Notch etkisi zayıflayan fibroblastlar daha fazla reseptör taşıyor ve yüksek derecede yanıtlı hale gelerek fibrozisi tetikleyen COMP‑zengin hücrelere dönüşüyordu.
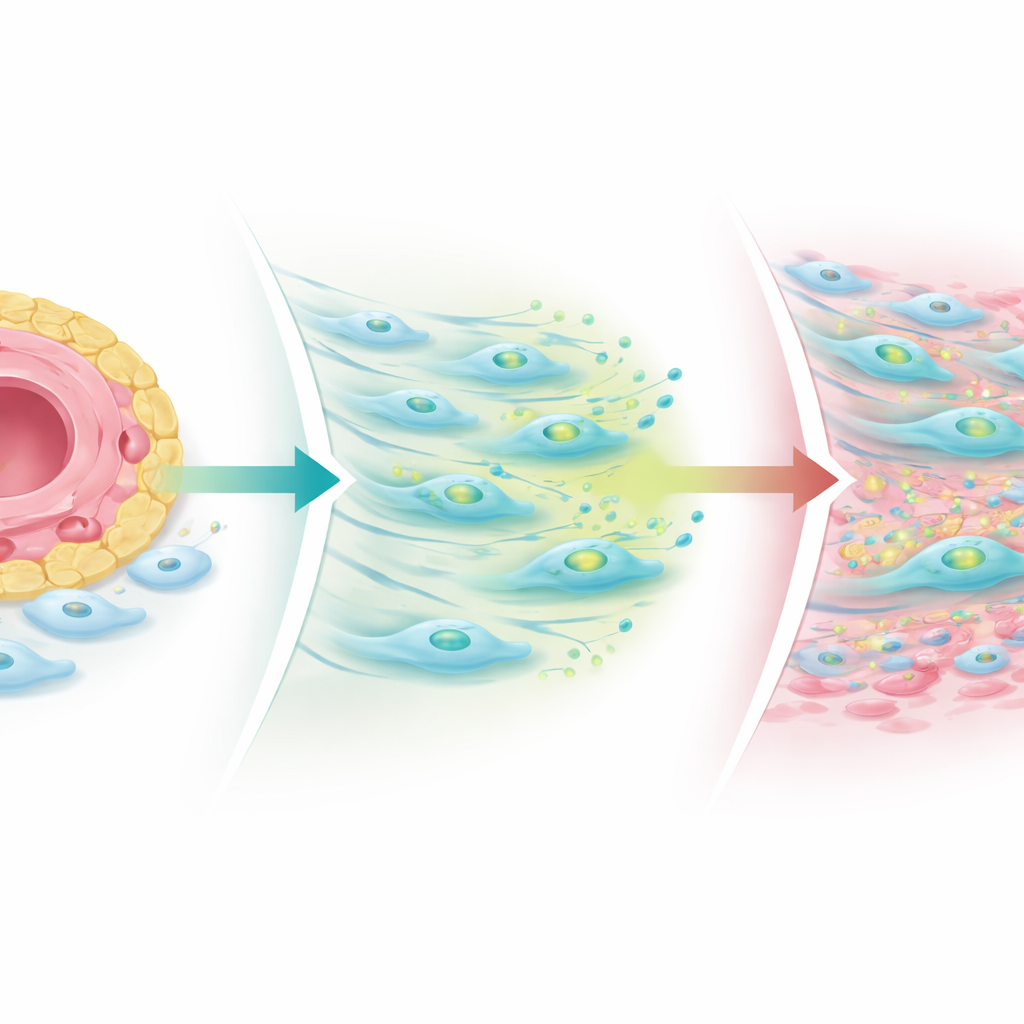
Denge bozulduğunda ne olur
Araştırmacılar bu mekanizmayı incelemek için laboratuvar kaplarında basitleştirilmiş eklem modelleri ve hasta dokusundan yapılmış üç boyutlu organoidler kurdular. Endotelyal hücrelerden gelen Notch sinyallerini güçlendirdiklerinde, fibroblastlar TGF‑beta üretimini artırdı ama reseptör düzeyleri azaldı, bu da skar oluşumunu sınırladı. Notch engellendiğinde veya düzenli deseni bozulduğunda, fibroblastlar özellikle TGF‑beta reseptörü III adlı bir yardımcı reseptör olmak üzere TGF‑beta reseptörlerini geri kazandı ve COMP‑pozitif fibrojenez hücreleri damarlardan uzaklaşarak genişledi. Tedavi sonrası alınan hasta biyopsilerinde, bağışıklık hücresi kümeleri neredeyse herkes için küçülmüşken, özellikle COMP‑zengin bölgeler olmak üzere fibrojenez bölgeleri sıklıkla büyümüştü; bu durum eklem ağrısı devam edenlerde daha belirgindi. Bu, standart anti‑inflamatuar ilaçların bağışıklık “ateşini” söndürebileceğini ama eklemde sertlik ve ağrıyı sürdürebilen ya da açığa çıkarabilen bir skarlaşma sürecini geride bırakabileceğini gösteriyor.
İnatçı eklemleri yatıştırmanın yeni yolları
Son olarak ekip, bu fibrojenez devrelerini bozmanın terapötik açıdan yararlı olup olmayacağını test etti. Hasta kaynaklı organoidlerde Notch’u inhibe eden veya TGF‑beta sinyalleşmesini engelleyen ilaçlar COMP ve diğer skar ilişkili proteinlerin ve önemli kollajenlerin üretimini azalttı ve perivasküler zonlardaki gen aktivitesini yeniden yönlendirdi. Bir gözlemci için çıkarım şudur: her romatoid artrit hasarı görünür iltihaptan gelmiyor; bir kısmı eklemin destek hücreleri ve kan damarlarına “donmuş” halde yerleşmiş durumda. Fibroblastların skar dokusu oluşturma biçimini kontrol eden Notch–TGF‑beta iletişimini hedefleyerek, gelecekteki tedaviler bugünün bağışıklık odaklı ilaçlarına direnç gösteren ısrarcı, fibrotik bir hastalık formunu önleyebilir veya tersine çevirebilir.
Atıf: Bhamidipati, K., McIntyre, A.B.R., Kazerounian, S. et al. Spatial patterning of fibroblast TGFβ signaling underlies treatment resistance in rheumatoid arthritis. Nat Immunol 27, 556–571 (2026). https://doi.org/10.1038/s41590-025-02386-2
Anahtar kelimeler: romatoid artrit, fibrozis, fibroblastlar, TGF-beta sinyalleşmesi, Notch yolu