Clear Sky Science · tr
Mammal hücrelerinde proteoglikanları manipüle etmek için ksilosiltransferaz mühendisliği
Hücre Dış Kapakları Neden Önemli
Vücudumuzdaki her hücre, komşularıyla iletişim kurmasına ve çevresini algılamasına yardımcı olan moleküler bir “kapak” taşır. Bu kapağın önemli bir bölümünü, büyüme faktörleri, bağışıklık sinyalleri ve yapısal ipuçları için küçük antenler gibi davranan uzun şeker zincirleriyle süslenmiş proteinler olan proteoglikanlar oluşturur. Bu şeker süslemesi bozulduğunda gelişim aksayabilir ve kemik ile kas gibi dokular ciddi şekilde etkilenebilir. Yine de bilim insanları bu zincirleri hangi proteinlerin taşıdığını ve kapaktaki bireysel bileşenlerin hücre davranışını nasıl etkilediğini tam olarak haritalamakta zorlandı. Bu çalışma, yaşayan memeli hücrelerinde bu şeker zincirlerini etiketleyip yeniden inşa etmek için kesin bir kimyasal strateji sunuyor; hücre yüzeylerinde şifrelenmiş bilgiyi okumaya ve yeniden yazmaya olanak veriyor. 
Şeker Bağlanmasının İlk Adımını Yeniden Yönlendirmek
Proteoglikanların inşası, özel bir enzim ailesi olan ksilosiltransferazlar XT1 ve XT2, bir proteine ilk şekeri takarak başlar; bu, uzun zincirin büyüyeceği yeri işaretler. Her iki enzim de aynı ilk adımı gerçekleştirebildiği için, hücre içinde hangisinin hangi protein üzerinde çalıştığını ayırt etmek zor oldu. Yazarlar bunu çözmek için modern kimyasal biyolojide sık kullanılan “takoz‑ve‑delik” tasarımını kullandılar. XT1’in aktif bölgesinin şeklini biraz değiştirip ekstra bir boşluk (“delik”) oluşturdular ve eşleşen, biraz daha hacimli bir şeker yapı taşı olan 6AzGlc’yi (“takoz”) tanıttılar. Mühendislik ürünü XT1 artık bu modifiye şekeri kullanabiliyor; doğal enzim ise kullanamıyor; böylece araştırmacılar yalnızca yeniden tasarlanmış enzimin dokunduğu proteinleri etiketleyebiliyor.
Hücrelere Tasarım Şekeri Kaçırmak
Bu yaklaşımın yaşayan hücrelerde çalışması için ekip, takozlu şekeri hücresel metabolizma tarafından tanınabilecek bir formda iletmek zorundaydı. Ksiloz analoglarını iyi işleyemeyen normal şeker alım yollarına güvenmek yerine, gizli bir fosfat grubu taşıyan kafeslenmiş bir 6AzGlc biçimi oluşturdular. Sitoplazmaya girdikten sonra hücresel enzimler bu grubu açığa çıkarıp molekülü, mühendislik ürünü ksilosiltransferazların gerektirdiği etkinleştirilmiş form olan UDP‑6AzGlc’ye dönüştürür. Titiz kromatografi, doğru yapılandırılmış kafeslenmiş bileşikle muamele edilen hücrelerin etkinleştirilmiş tasarım şekerinden önemli miktarda ürettiğini, ayna görüntülü kontrolün ise neredeyse hiç üretmediğini doğruladı. 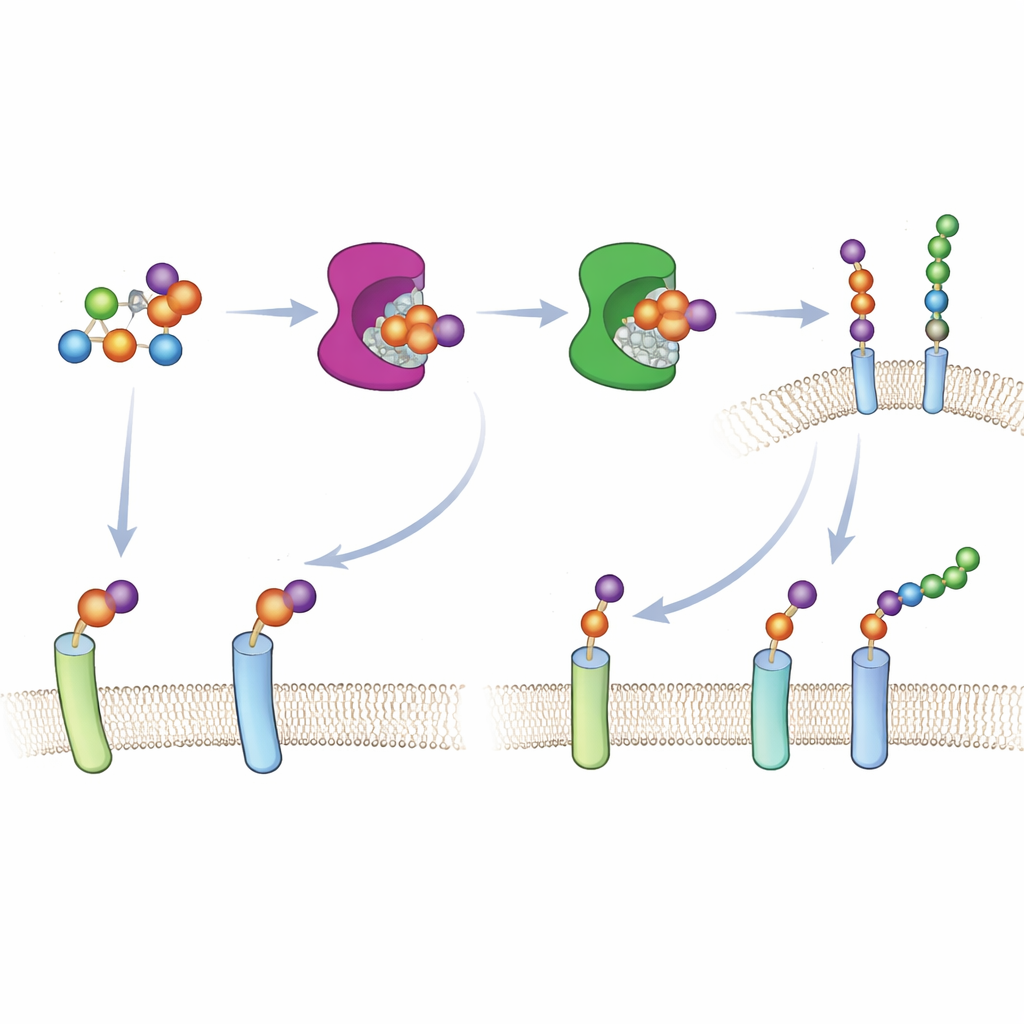
Gizli Oyuncuları Etiketleyip Tanımlamak
Modifiye enzim ve etkinleştirilmiş şeker bir araya gelince, araştırmacılar yalnızca mühendislik ürünü XT1 veya XT2 ifade eden hücrelerin yüzey proteoglikanlarına 6AzGlc etiketini dahil ettiğini gösterdiler. 6AzGlc üzerindeki azid grubu, floresan boyalara veya biotine “tıklandığında” bağlanabilen küçük bir kimyasal tutamak görevi görür; bu, etiketlenmiş proteinlerin görselleştirilmesini ve zenginleştirilmesini sağlar. Zenginleştirilmiş örneklerin kütle spektrometrisi, decorin, çeşitli glipikanlar, syndecan‑4, CD44 ve versican dahil olmak üzere bilinen proteoglikanlardan zengin bir koleksiyonu ortaya koydu; bu, sistemin gerçek şeker taşıyan proteinleri işaretlediğini doğruladı. Önemli olarak, mühendislik ürünü enzimler doğal muadillerinin aynı dizi tercihlerini korudu; yani kimyasal etiket yeni, yapay pozisyonlarda değil, özgün bağlanma noktalarında takılıyor.
Tasarım Proteoglikanlar İnşa Etmek
6AzGlc etiketinin beklenmedik bir avantajı, doğal başlatıcı şekerin aksine, aşağı akış enzimleri tarafından tam uzunlukta bir zincire uzatılamamasıdır. Bu, zinciri etkin bir şekilde sonlandırır ve kütle spektrometrisi ile analiz edilmesi gereken moleküler yapıyı basitleştirir. Yazarlar bu özelliği bir araca çevirdiler: XT1 6AzGlc’yi doğal bir bağlanma noktasına taktığında, click kimyası kullanarak sentetik heparin parçalarını ekleyip kesin tanımlı şeker zincirlerine sahip “tasarım proteoglikanlar” oluşturdular. Kendi syndecan‑1’leri olmayan meme kanseri hücrelerine böyle tasarım versiyonlar eklemek, protein kaplı bir yüzeyde normal yayılmayı geri kazandırdı; bu da kimyasal olarak yeniden inşa edilmiş proteoglikanın fonksiyonel olarak doğal olanın yerini alabileceğini gösterdi.
Biyoloji ve Tıp İçin Anlamı
Bu çalışma, hücrelerin iletişimini kontrol eden şeker zincirlerini seçici olarak etiketleyip manipüle etmeye yarayan güçlü bir araç seti sunuyor. XT1 ve XT2’nin rollerini ayırıp yalnızca doğrudan hedeflerini etiketleyerek araştırmacılar artık belirli dokularda ve hastalık durumlarında hangi proteoglikanların etkin olduğunu haritalayabilir. Doğal zincir büyümesini durdurup yerine özel‑yapılmış şekerler koyma yeteneği, bir proteoglikanın işlevinin ne kadarının protein iskeletiyle ne kadarının şeker kabuğuyla taşındığını ayrıştırmaya da olanak tanır. Uzun vadede bu tür hassas mühendislik, hücre yüzeyindeki karmaşık sinyalleşmeyi çözmeye yardımcı olabilir ve gelişim bozuklukları, kanser ve diğer hastalıklarda bozulmuş hücresel kapakları onaran veya yeniden programlayan terapilere ilham verebilir.
Atıf: Li, Z., Chawla, H., Di Vagno, L. et al. Xylosyltransferase engineering to manipulate proteoglycans in mammalian cells. Nat Chem Biol 22, 612–621 (2026). https://doi.org/10.1038/s41589-025-02113-w
Anahtar kelimeler: proteoglikanlar, glikozaminoglikanlar, ksilosiltransferaz, kimyasal biyoloji, hücre yüzeyi sinyalleşmesi