Clear Sky Science · tr
Tek bir allosterik bölge TRPM5’te aktivasyonu, modülasyonu ve inhibisyonu birleştiriyor
Tek Bir Minik Kapı Bekçisinin Tat ve Metabolizmayı Nasıl Şekillendirdiği
Zevk aldığımız yiyecekler ve vücudumuzun şekeri nasıl işlediği, hücrelerimizdeki mikroskobik “kapı bekçisi” proteinlere bağlıdır. Bu bekçilerden biri olan TRPM5 adlı kanal, tatlı, acı ve umami tatları almamıza yardımcı olur ve pankreasın insülin salgılamasını destekler. Bu çalışma, TRPM5 üzerindeki tek bir küçük cebin kanalın ana kontrol düğmesi gibi davranarak kanalı açabileceğini, duyarlılığını ayarlayabileceğini ve hatta kapatabileceğini gösteriyor — bu bulgu diyabet, obezite ve bağırsak hastalıkları için gelecekteki tedavilere rehberlik edebilir.
Tat ve Kan Şekeri Kavşağındaki Bir Kanal
TRPM5, dildeki tat hücrelerinin zarlarında, bağırsakta hormon üreten hücrelerde ve pankreasta insülin salgılayan hücrelerde bulunur. Bu hücrelerin içindeki kalsiyum seviyeleri yükseldiğinde TRPM5 açılır ve pozitif yüklü iyonların akmasına izin vererek hücrenin voltajını kısa süreliğine değiştirir. Tat tomurcuklarında bu elektriksel sinyal, beyine dilde tatlı, acı veya umami bir şey olduğunu bildirir. Pankreasta ise yemek sonrası insülin atımlarını ince ayar yapmaya yardımcı olur. TRPM5 fonksiyonu bozulmuş kişilerde ve hayvanlarda insülin salınımı ve kan şekeri kontrolünde sorunlar gözlemlendiğinden, TRPM5’i hedefleyen ilaçların bir gün metabolik hastalıkların tedavisinde faydalı olabileceği düşünülüyor. Ancak yakın zamana kadar araştırmacıların bu kanalı kesin olarak açıp kapatabilecek araçları yoktu.
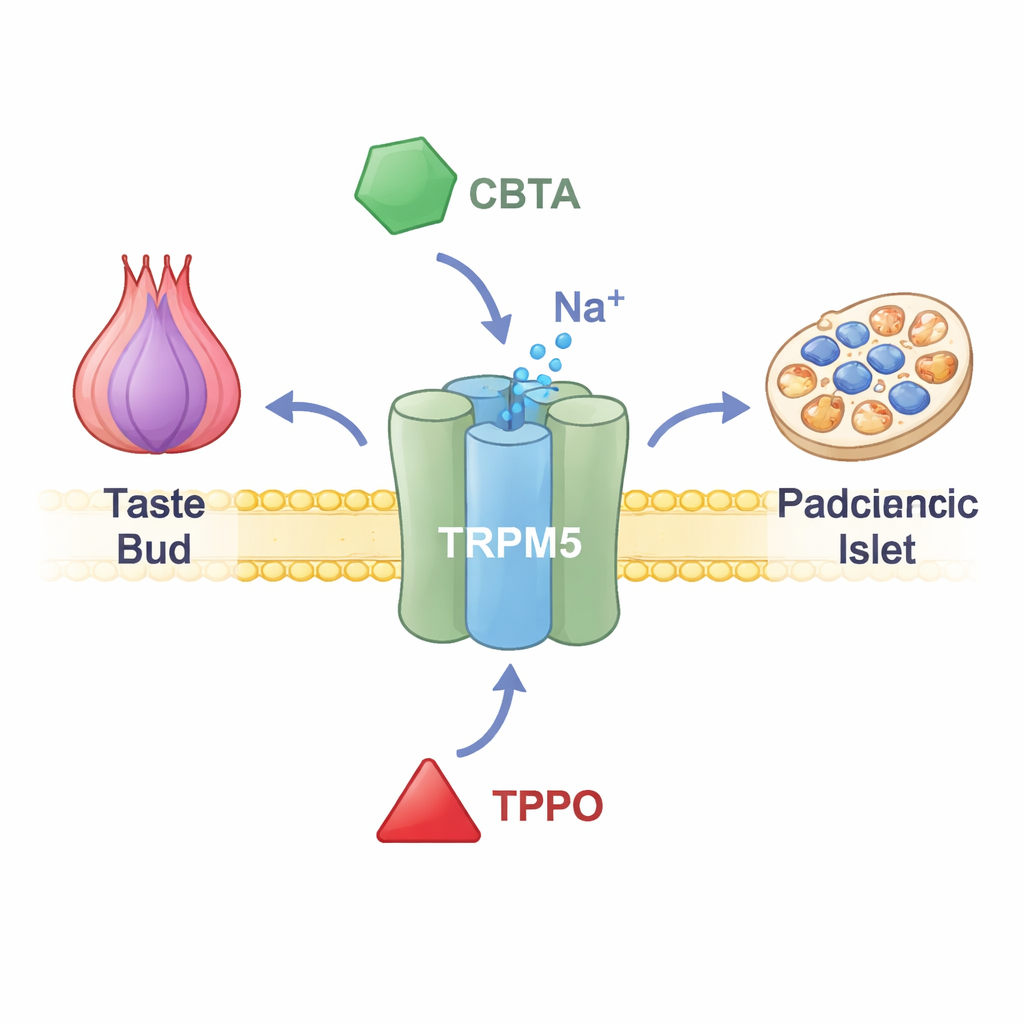
Kanala Süper Güç Kazandıran Yeni Bir Kimyasal Anahtar
Araştırmacılar daha önce TRPM5’i uyardığı bilinen ama iyi anlaşılmamış sentetik bir bileşik olan CBTA’ya odaklandılar. TRPM5 üreten hücrelerden yapılan elektriksel kayıtlarla, CBTA’nın kalsiyum neredeyse yokken bile kanalı açabildiğini gösterdiler; bu da CBTA’nın yalnızca kalsiyumun etkisini artırmakla kalmayıp gerçek bir aktivatör olarak işlediğini kanıtlıyor. Normalde TRPM5’i sessiz bırakan çok düşük kalsiyum miktarlarının var olduğu durumlarda—CBTA ve kalsiyum birlikte hareket ederek tek başlarına oluşturduklarından çok daha büyük akımlar üretiyorlar. Bu, CBTA’nın TRPM5’i son derece duyarlı hale getirdiği anlamına geliyor; dinlenim seviyesine yakın kalsiyum bile aniden kanalı tamamen açmaya yetecek kadar etkili oluyor.
Cryo-EM ile Ortaya Çıkan Gizli Bir Kontrol Cebi
Bunun atomik ayrıntıda nasıl çalıştığını görmek için ekip, farklı koşullar altında TRPM5’in üç boyutlu anlık görüntülerini yakalamak üzere kriyo-elektron mikroskopi kullandı. CBTA’nın, kalsiyumun genellikle bağlandığı yerin hemen üzerinde, kanalın voltaj algılama bölgesinin üst kısmında daha önce fark edilmemiş bir boşluğa yerleştiğini keşfettiler. Bir amino asit kümesi tarafından oluşturulan bu boşluk hassas bir kenetlenme noktası olarak görev yapıyor. Bilim insanları bu cebin çizgisini oluşturan önemli yapı taşlarını mutasyona uğrattıklarında, kalsiyum hâlâ çalışmasına rağmen CBTA TRPM5’i artık etkinleştiremedi; bu, bu küçük nişin ilacın etkisi için elzem olduğunu doğruluyor. Çarpıcı şekilde, CBTA bağlanması proteinin yakın kısımlarını kalsiyumun sıradan durumunu yakalamasını çok daha kolay hale getirecek biçimde ince bir şekilde yeniden düzenliyor; bu da elektriksel ölçümlerde görülen dramatik sinerjiyi açıklıyor.
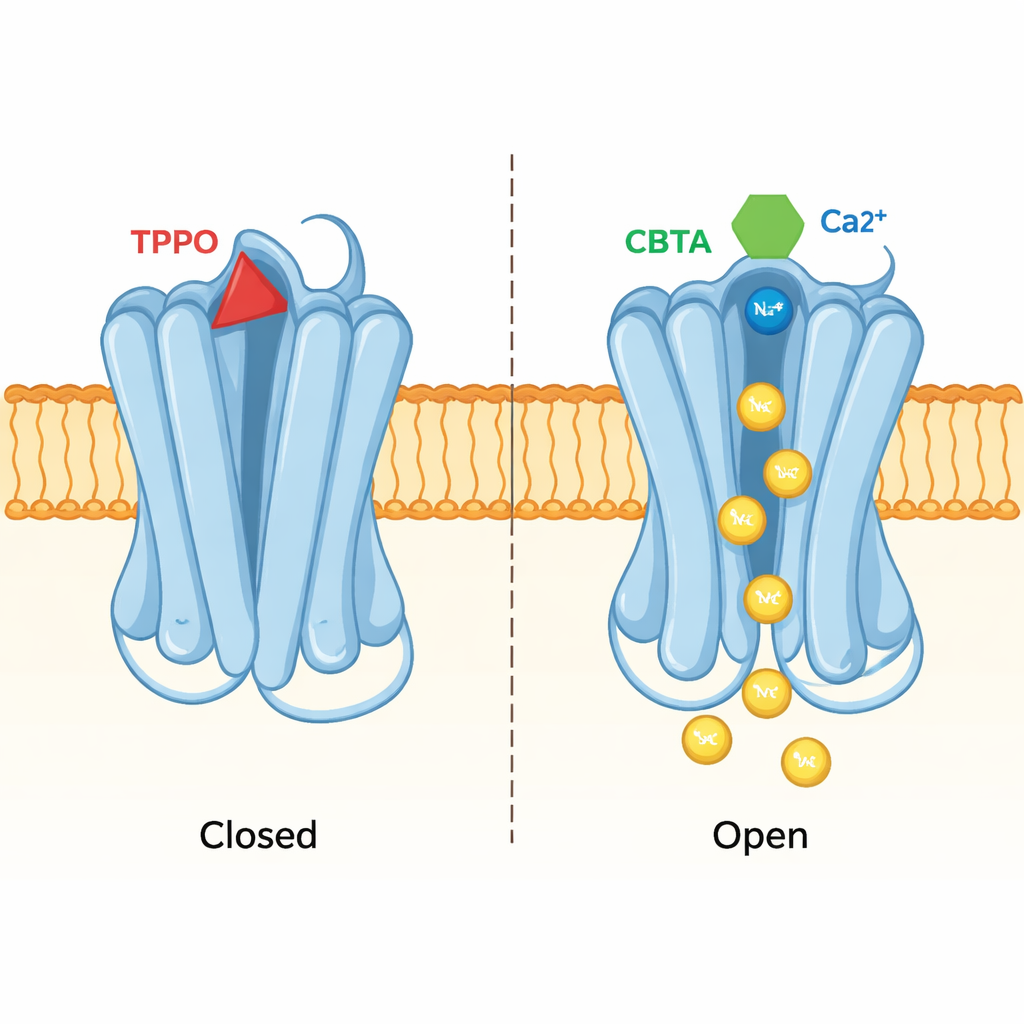
Tek Bir Cep, İki Zıt Sonuç
Aynı yapısal yaklaşım, TPPO adlı bir inhibitörün tam olarak aynı cebi kullanarak ters etkiyi nasıl ürettiğini de ortaya koydu. TPPO bağlandığında, TRPM5 üzerindeki her iki kalsiyum bölgesi dolu kalır, ancak kanalın merkezi gövdesi sıkışmış halde kalır ve iyon geçişine izin verilmez. TPPO bağlı ve CBTA bağlı yapılar karşılaştırıldığında, bu iki molekülün farklı şekillerinin yakın protein segmentlerini zıt yönlere ittiği görüldü. CBTA, gövdeye yayılan ve onu açan hareketleri teşvik ediyor; TPPO ise cebiyle gövde arasındaki iletişimi bozarak kapıyı kapalı tutuyor. Özetle, bu tek cep, hangi molekülün yerleştiğine bağlı olarak ya bir hızlandırıcı ya da bir fren görevi görebiliyor.
Kanalın İç Kablajını Yeniden Yönlendirmek
Araştırma ayrıca bu kontrol cebinin normalde hücre içindeki ayrı bir kalsiyum bağlama bölgesinin üstlendiği işleri devralabildiğini gösteriyor. İç kalsiyum bölgesi devre dışı bırakılmış mutant kanallarda kalsiyum tek başına TRPM5’i açamıyordu. Buna karşın CBTA bu mutantları hâlâ aktive edebiliyor ve kanalın iç ve dış kısımlarını bağlayan önemli bir yapısal öğeyi yeniden şekillendiriyordu. Kalsiyum bağlanması ile gövdenin açılması arasındaki bağlantıyı bozan başka mutantlarda ise CBTA eklenmesi normal davranışı geri getirdi. Bu sonuçlar, yeni tanımlanan bölgenin farklı kanal alanları arasındaki iletişimi yeniden yönlendirebileceğini veya onarabileceğini; protein içinde uzak mesafe sinyalleşmesi için esnek bir merkez görevi görebileceğini ortaya koyuyor.
Gelecekteki İlaçlar İçin Neden Önemli
Uzman olmayanlar için temel mesaj, araştırmacıların TRPM5 üzerinde aktivasyonu, ince ayarı ve kapamayı bütünleştirebilen tek, ilaç duyarlı bir cep bulmuş olmalarıdır. CBTA gibi küçük bir aktivatör hem kalsiyumu taklit edebilir hem de kanalın duyarlılığını büyük ölçüde artırabilirken, TPPO gibi başka bir bileşik aynı kanalı kapalı tutabilir; tümü aynı yerde kenetlenerek gerçekleşir. TRPM5’in nasıl kontrol edildiğine dair bu birleşik anlayış, belirli dokularda aktivitesini ya artıracak ya da azaltacak şekilde tasarlanmış moleküller geliştirme yolunu açıyor; bu da tat bazlı tedavilerin ve bağırsak motilitesi ilaçlarının iyileştirilmesinden kan şekeri ve metabolik hastalıkların yönetimine kadar çeşitli uygulamalara kapı aralayabilir.
Atıf: Ruan, Z., Lee, J., Li, Y. et al. A single allosteric site merges activation, modulation and inhibition in TRPM5. Nat Chem Biol 22, 402–410 (2026). https://doi.org/10.1038/s41589-025-02097-7
Anahtar kelimeler: TRPM5 kanalı, tat algısı, insülin salgılanması, iyon kanal kapama/açma, allosterik modülasyon