Clear Sky Science · tr
CDK4/6 inhibitasyonu, kemoterapi kaynaklı TP53-mutant klonal hematopoez genişlemesini azaltıyor
Kanı kanser tedavisinden korumanın önemi neden büyük
Kanser kemoterapisi hayat kurtarabilir, ancak yeni kan hücrelerinin üretildiği kemik iliğini de yıpratır. Bazı insanlarda bu hasar, nadir ve önceden var olan mutant kan kök hücrelerinin büyümesini istemeden teşvik ederek onların hakimiyet kurmasına yol açar; bu durum daha sonra agresif kan kanserlerine dönüşebilir. Bu çalışma umut verici bir soruyu gündeme getiriyor: kemoterapi sırasında kan kök hücrelerini korumak için geçici bir “duraklatma düğmesi” ilacı kullanabilir miyiz; böylece bu riskli mutant klonların yükselişini yavaşlatıp kanser tedavisinin etkinliğini zayıflatmadan koruma sağlayabilir miyiz?
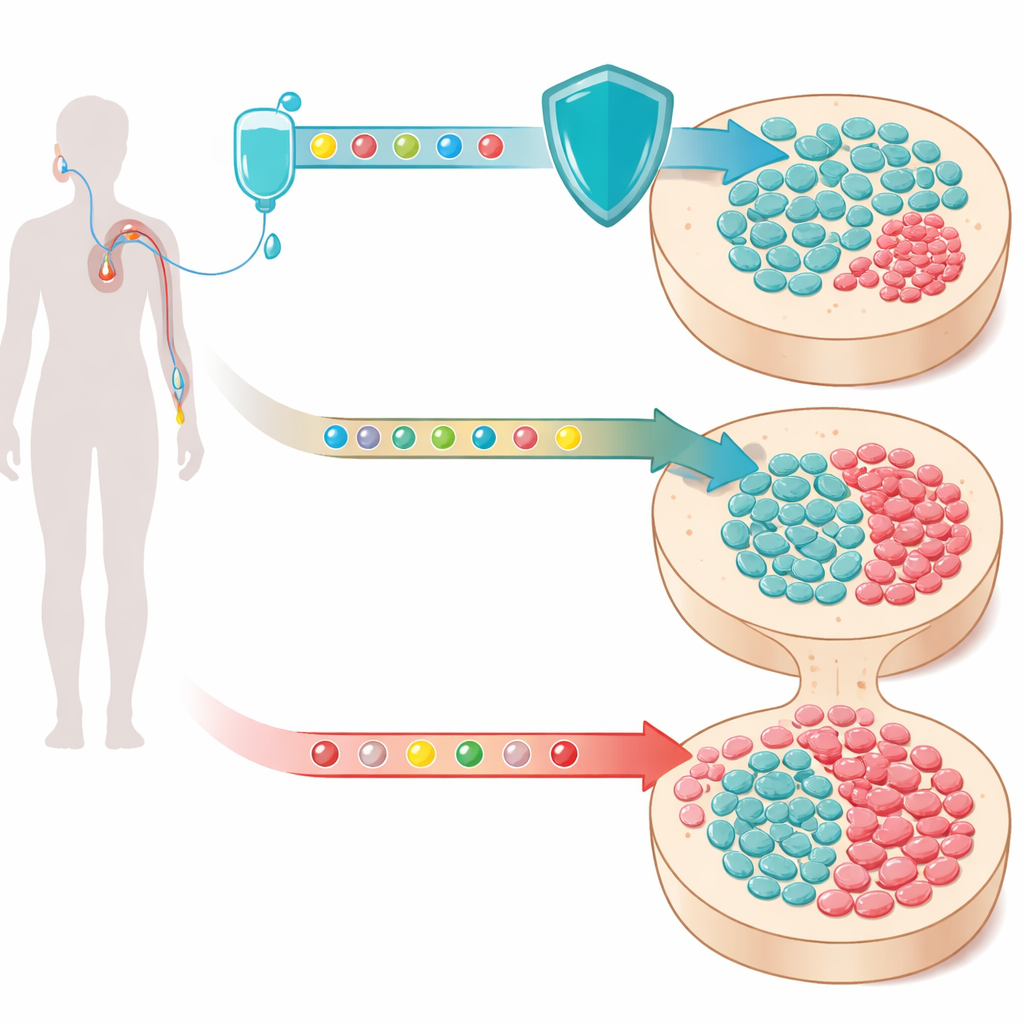
Kandaki gizli klonlar
İlerledikçe, kan oluşturan kök hücrelerimizde yavaş yavaş DNA değişiklikleri birikir. Bu değişime uğramış hücrelerin çoğu zararsız kalır, ancak bazıları büyüme avantajı kazanıp küçük klonlar—genetik olarak eşleşmiş hücre yığınları—oluşturmaya başlar ve dolaşıma girer. Klonal hematopoez adı verilen bu olgu, yaşlı erişkinlerde şaşırtıcı derecede yaygındır. Etkilenen gen TP53 veya diğer DNA hasarına yanıt genleri olduğunda, bu klonlar özellikle endişe vericidir: normal hücreleri öldüren strese direnç gösterirler ve yıllar sonra kemoterapinin tetikleyebileceği, sıklıkla ölümcüle varabilen tedavi ilişkili myeloid neoplazilerle yakından ilişkilidirler.
Kemoterapi sırasında kök hücreleri duraklatmak
Araştırmacılar, hücrelerin bölünmesini yönlendiren temel motorlar olan CDK4/6’yı engelleyen ilaçlara odaklandı. Bu ilaçlardan biri olan trilaciclib, belirli akciğer kanseri tedavisi görenlerde düşük kan sayımlarını azaltmak için zaten onaylıdır. Kemoterapiden kısa süre önce verildiğinde, kemik iliği kök ve progenitör hücrelerini dinlenme durumuna itiyor. Ekip, hem sağlıklı hem de TP53‑mutant kök hücreler kemoterapi vurduğunda daha az aktifse, mutantların alışılmış hayatta kalma avantajının büyük ölçüde kaybolacağı mantığıyla hareket etti; çünkü DNA’yı hasar veren ilaçların en toksik olduğu anda bölünme halinde bulunan daha az hücre—normal ya da mutant—yakalanmış olurdu.
Kanser denemeleri ve hayvan modellerinden kanıt
Bu fikri gerçek hastalarda test etmek için grup, küçük hücreli akciğer kanseri, metastatik kolorektal kanser ve triple‑negatif meme kanseri için kemoterapi alan kişilerde yürütülen dört randomize klinik çalışmadan alınan kan örneklerini analiz etti. Her bir çalışmada hastalar rastgele olarak trilaciclib veya plasebo eşliğinde standart kemoterapi almaya atandı. Tedavi başlangıcında ve birkaç döngü sonrasında kan hücrelerinin ultra‑derin DNA dizilemesi kullanılarak, bilim insanları bilinen mutant klonların zaman içindeki boyut değişimini izlediler. Tüm çalışmalarda, özellikle TP53 ve PPM1D taşıyan DNA hasarına yanıt mutasyonları kemoterapi sırasında genişledi; ancak trilaciclib alan kişilerde bu klonlar önemli ölçüde daha yavaş büyüdü. Ortalama olarak, bu riskli klonların büyüme hızı yaklaşık üçte bir oranında azaltıldı; diğer genlerdeki daha rutin, yaşa bağlı mutasyonlar ise büyük ölçüde etkilenmedi.
Korumaya hangi mekanizmalarla ulaşıldığına yakından bakmak
Hasta takip süresi hâlâ görece kısa olduğundan ekip, CDK4/6 blokajının tedavi sırasında kemik iliğini nasıl yeniden şekillendirdiğini ortaya çıkarmak için fare modellerine döndü. İnsan klonal hematopoezini taklit etmek üzere kan sistemlerinde Trp53‑mutant kök hücrelerin küçük bir fraksiyonunu içeren fareler oluşturuldu. Bu farelere sadece platin bazlı kemoterapi verildiğinde, mutant hücreler kan ve iliikte normal komşularını hızla geride bıraktı. Ancak trilaciclib—veya başka bir CDK4/6 inhibitörü olan palbociclib—her kemoterapi dozundan kısa süre önce verildiğinde, bu mutant hakimiyeti neredeyse tamamen engellendi. Ayrıntılı tek hücre RNA dizilemesi, CDK4/6 inhibitasyonunun kök ve progenitör hücreleri daha sessiz, daha az proliferatif bir duruma ittiğini, uzun ömürlü mutant hücreleri destekleyen “kök hücrelik” gen programını azalttığını, gelişimi miyeloid hatlardan lenfoid hatlara yönlendirdiğini ve Trp53‑mutant kök hücrelerde seçici olarak hücre ölümü yollarını tetiklerken normal hücreleri koruduğunu gösterdi.
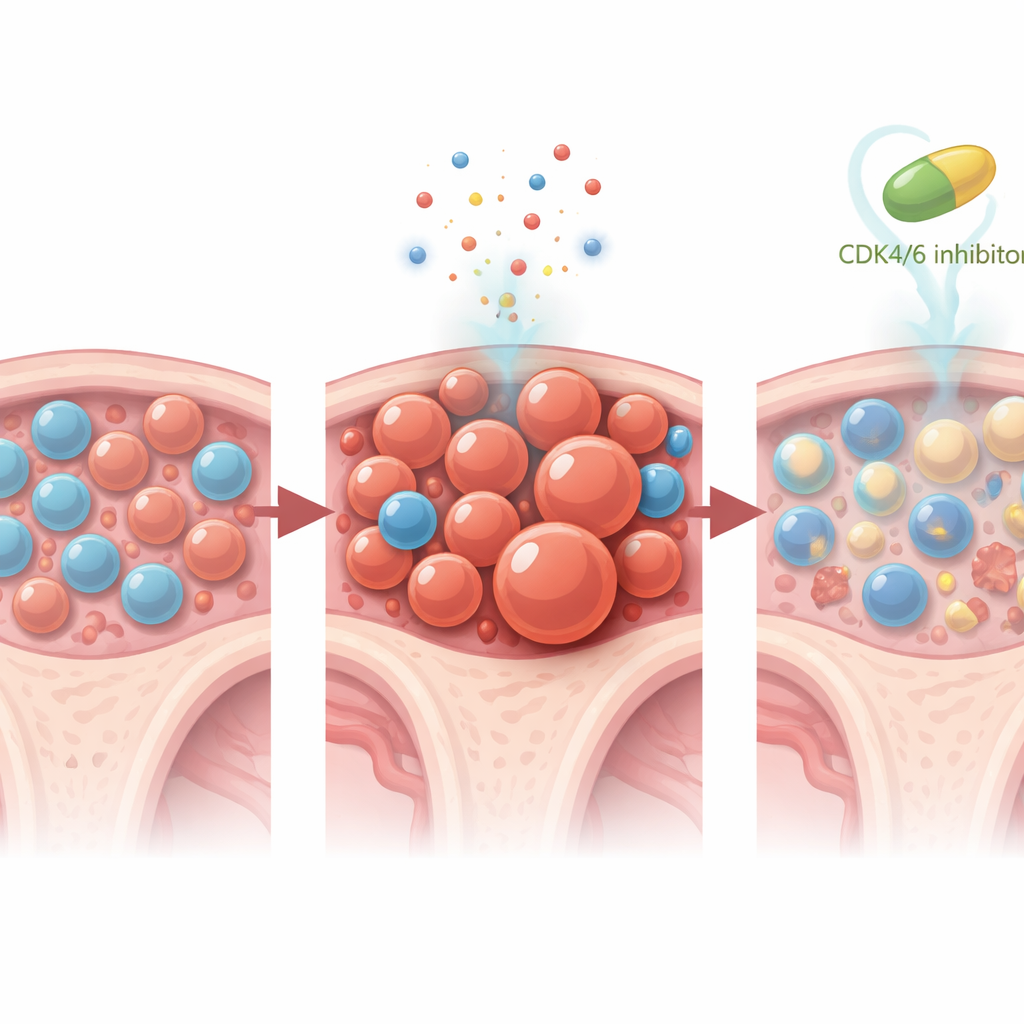
Sürdürülebilir etkiler ve gelecekteki yönelimler
Tek bir çarpıcı fare deneyi, kısa bir CDK4/6 inhibitörlüğü kürünün bile kalıcı etkiler yaratabileceğini gösterdi: kemoterapi çevresinde verilen iki haftalık trilaciclib, tüm tedavi durduktan sonra en az altı hafta boyunca Trp53‑mutant klonların genişlemesini engelledi. Önemli olarak, kan sayımları ve genel iliğin sağlığı kabul edilebilir düzeyde kaldı; bu da koruyucu stratejinin bir tür toksikliği başka bir tür toksiklikle değiştirmediğini gösteriyor. Çalışmalardaki hastaların sınırlı takip süresinde hiçbirinin kan kanseri geliştirmemiş olmasıyla birlikte, çok küçük TP53‑mutant klonların varlığı ve yavaşlayan büyümeleri, bunun tedavi ilişkili lösemiye giden yolda erken ve değiştirilebilir bir adım olduğu fikrini destekliyor.
Bu, kanserli insanlar için ne anlama gelebilir
Zaten yüksek riskli kan hücresi klonlarına sahip hastalar için en büyük korku, sağlam tümörü kontrol altına almak amacıyla verilen kemoterapinin gelecekte sıklıkla tedavi edilemeyen bir lösemi tohumunu da ekmesi oldu. Bu çalışma, dikkatle zamanlanmış CDK4/6 inhibitörlerinin kemoterapi sırasında kemik iliğini kısa süreliğine koruyarak bu tehlikeli klonların büyüme avantajını azaltabileceğine yönelik bir kavram kanıtı sunuyor. Bu stratejinin tedavi ilişkili kan kanserleri insidansını gerçekten düşürdüğünü kanıtlamak için daha uzun ve daha büyük klinik çalışmalara ihtiyaç olsa da, birincil kanseri agresif biçimde tedavi ederken aynı zamanda kan oluşturan sistemi uzun vadeli genetik zarardan koruyabileceğimiz bir geleceğe işaret ediyor.
Atıf: Chan, I.C.C., Zhang, P., Pan, X. et al. CDK4/6 inhibition mitigates chemotherapy-induced expansion of TP53-mutant clonal hematopoiesis. Nat Genet 58, 582–592 (2026). https://doi.org/10.1038/s41588-026-02526-w
Anahtar kelimeler: klonal hematopoez, TP53 mutasyonları, kemoterapi yan etkileri, CDK4/6 inhibitörleri, tedavi ilişkili lösemi