Clear Sky Science · tr
Otoimmün hipotiroidinin tüm genom ilişkili analizleri otoimmün ve tiroide özgü katkıları ve kanser riski ile ters ilişkisini ortaya koyuyor
Günlük sağlık için bunun önemi
Birçok insan yorgun, üşüyen veya zihnen bulanık hissederken tiroid bezinin suçlu olabileceğini fark etmiyor. Vücudun kendi savunma mekanizmalarının tiroide yavaşça saldırdığı otoimmün hipotiroidi yirmide birden fazla kişiyi etkiler. Bu çalışma, yüz binlerce gönüllüden elde edilen genetik verileri kullanarak iki büyük soruyu soruyor: DNA’mızdaki hangi kalıtsal değişiklikler bu durumu daha olası kılıyor ve aynı değişiklikler kanser gelişme riskiyle nasıl ilişkili? Yanıtlar, bazen tiroide zarar veren ancak tümörlere karşı ek koruma sağlayabilen bağışıklık sistemi arasında şaşırtıcı bir takas ortaya koyuyor.
Tüm genomu taramak
Araştırmacılar, Finlandiya’daki FinnGen ile Birleşik Krallık’taki UK Biobank olmak üzere iki büyük nüfus projesinin sağlık kayıtları ve genetik bilgilerini birleştirdi. Uzun süreli tiroid hormonu replasmanı ihtiyacı olan kişilere odaklandılar ve cerrahi, kanser veya diğer otoimmün olmayan nedenlere bağlı tiroid sorunlarını dikkatle dışladılar. Bu, şimdiye kadarki en büyük çalışmayı oluşturarak 81.000’den fazla otoimmün hipotiroidi vakası ve 700.000’den fazla kontrol üretti. Genom boyunca milyonlarca DNA belirteci taranırken, ana immün gen kümesinin dışındaki 280’den fazla bölgede yayılan 418 bağımsız genetik sinyal keşfedildi. Bu sinyallerin çoğu, protein yapısını değiştiren nadir veya düşük frekanslı DNA değişikliklerini içeriyordu ve altta yatan biyolojiye doğrudan ipuçları sağladı.
Genel bağışıklık etkilerini tiroide özgü olanlardan ayırmak
Otoimmün hipotiroidi, genel otoimmünite ile tiroid bezinin özgün biyolojisinin kesiştiği noktadadır. Bu bileşenleri ayırmak için ekip, bulgularını diğer otoimmün hastalıkların genetik çalışmaları ve az işleyen tiroidi saptamada kullanılan ana klinik belirteç olan tiroid stimüle edici hormonun (TSH) kan seviyeleri ile karşılaştırdı. Bayesçi sınıflandırma yöntemi kullanarak genetik sinyalleri geniş otoimmün hastalıklarla paylaşılanlar ve tiroid hormonu düzenlemesine daha özgü olanlar şeklinde grupladı. Yaklaşık olarak sinyallerin %38’inin birçok otoimmün durumu etkileyen genel immün yolaklar aracılığıyla etki gösterdiğini, yaklaşık %20’sinin ise esas olarak tiroid işlevi üzerinden etki ettiğini tahmin ettiler. Tiroide odaklı varyantlar genellikle hormon seviyelerini ve tiroid dokusunda aktif genleri etkilerken, genel immün varyantlar bağışıklık yanıtlarını yöneten T hücrelerinde daha aktiftir.
Anahtar bir immün anahtara yakından bakmak
Özellikle dikkat çekici bir bulgu, T hücreleri içindeki anahtar sinyal proteini olan ZAP70 genindeki nadir bir DNA değişikliğini içeriyordu. Bu proteindeki ciddi kusurların derin immün yetmezliğe yol açtığı biliniyor, ancak burada tanımlanan varyant yalnızca kısmi işlev kaybı üretiyordu. Mühendislikle değiştirilmiş T hücrelerinde yapılan laboratuvar deneyleri, bu değişmiş ZAP70’in hedefin tanınmasını takiben normalde oluşan sinyal kaskadını zayıflattığını, ancak tamamen engellemediğini gösterdi. Varyantı taşıyan hücreler aktivasyon belirteçlerini ve aşağı yöndeki sinyal adımlarını daha az etkin şekilde açabiliyordu. Bu yavaşlamış yanıt, normalde öz-reaktif T hücrelerini elenmesini sağlayan hassas dengeyi bozuyor gibi görünerek taşıyıcıları otoimmün hastalığa eğilimli hale getirirken bazı immün yetmezlik risklerini de hafifçe artırıyordu.
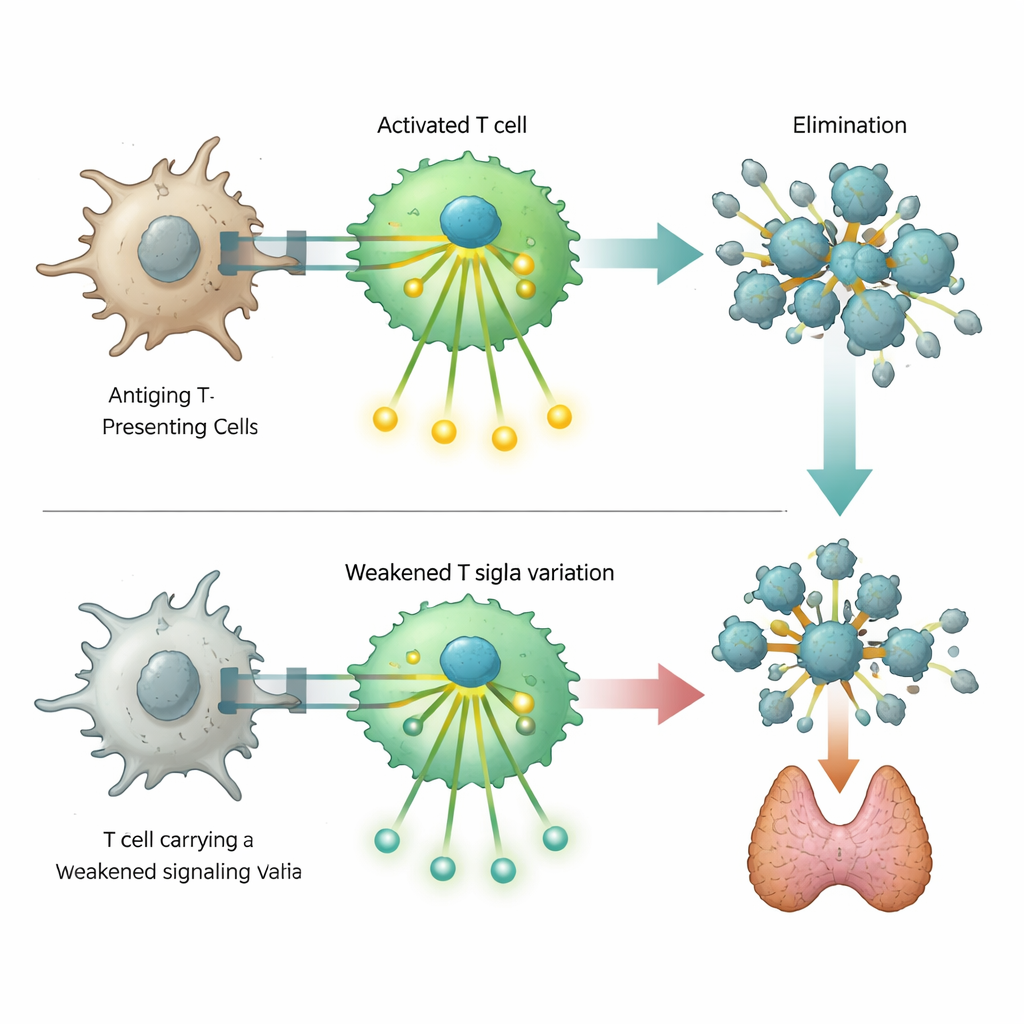
Kanser korumasına beklenmedik bir bağlantı
Otoimmüniteyi tetikleyen aynı immün yolakların tümörlere de saldırabileceği düşünüldüğünde, yazarlar bir sonraki adımda otoimmün hipotiroidi genetiğinin kanser riskiyle nasıl ilişkili olduğunu sordular. Her kişinin kalıtsal hipotiroidi eğilimini özetleyen bir poligenik risk skoru hesapladılar ve bunu Finlandiya verilerindeki birçok hastalıkla ilişkilendirdiler. Beklendiği gibi, daha yüksek skor çeşitli otoimmün durumlarla daha yüksek riskle ilişkiliydi. Daha şaşırtıcı olan ise bazal hücre karsinomu ve diğer deri kanserleri başta olmak üzere, ayrıca meme ve prostat kanseri ile genel “tüm kanser” grubunda tutarlı olarak daha düşük bir kanser riski deseniydi. Ekip kanser için yapılan genom çapı taramalara doğrudan baktığında, hipotiroidi ile ilişkili bölgelerin yaklaşık %10’unun deri kanserini de etkilediğini ve genellikle aynı genetik varyantın tiroid otoimmünitesini artırırken deri kanseri riskini azalttığını buldu. Bu paylaşılan varyantlar, immün kontrol noktası immünoterapisinde bilinen ilaç hedefleri dahil olmak üzere immünle ilişkili genlerde yoğunlaşmıştı.
Hastalar ve tıp için bunun anlamı
Halk diliyle bakıldığında, bu çalışma bazı insanların doğuştan biraz daha “aktif” ayarlı bağışıklık sistemleriyle doğduğunu; bunun tiroid bezine yavaş, çoğu zaman sessiz zarar vermeye daha yatkın kıldığını ancak aynı zamanda ortaya çıkan kanserleri daha iyi fark edip ortadan kaldırabilecek donanımı sağladığını gösteriyor. Çalışma hangi genetik değişikliklerin genel immün aşırı etkinlik yoluyla, hangilerinin ise özellikle tiroid hormonu üretimini etkileyerek etki ettiğini ayırıyor; bu da Hashimoto hastalığı ve Graves hastalığı gibi durumların bazı risk genlerini paylaşırken tiroid işlevini zıt yönlerde nasıl etkileyebileceğini açıklıyor. Ayrıca, immün güçlendirici kanser ilaçları alırken tiroid sorunları geliştiren hastaların neden bu tedavilere genellikle daha iyi yanıt verdiğini açıklamaya yardımcı oluyor. Genel olarak bulgular, immün kontrol noktası ve sinyal ileten genlerdeki yaygın, doğal varyasyonun hem otoimmün tiroid hastalığını hem de yaşam boyu kanser riskini şekillendirdiğini öne sürüyor ve önleme ile immünoterapilerin daha kişiselleştirilmiş kullanımına yönelik yeni yollar sunuyor.
Atıf: Reeve, M.P., Kanai, M., Graham, D.B. et al. Genome-wide association analyses of autoimmune hypothyroidism reveal autoimmune and thyroid-specific contributions and an inverse relationship with cancer risk. Nat Genet 58, 550–559 (2026). https://doi.org/10.1038/s41588-026-02521-1
Anahtar kelimeler: otoimmün hipotiroidi, tiroid hastalığı, genetik risk, bağışıklık sistemi, kanser koruması