Clear Sky Science · tr
Tümör–beyin iletişimi, duyu–sempatik ekseni aracılığıyla kanser bağışıklığını sınırlıyor
Sinirlerin Tümörlerin Saklanmasına Nasıl Yardımcı Olabildiği
Kanser genellikle asi hücrelerle bağışıklık sistemi arasındaki bir savaş olarak ele alınır, ancak bu çalışma şaşırtıcı bir üçüncü oyuncuyu ortaya koyuyor: sinir sistemi. Araştırmacılar, akciğer tümörlerinin akciğerler ve beyin arasında köprü kuran bir duyu–sempatik sinir devresine erişebildiğini ve bu devreyi vücudun doğal anti-kanser savunmalarını zayıflatmak için kullanabildiğini gösteriyor. Tümörler ile beyin arasındaki bu gizli “kabloyu” anlamak, sadece kanser hücrelerini değil, sinirleri ve sinyallerini hedef alan yeni akciğer kanseri tedavi yollarını açabilir. 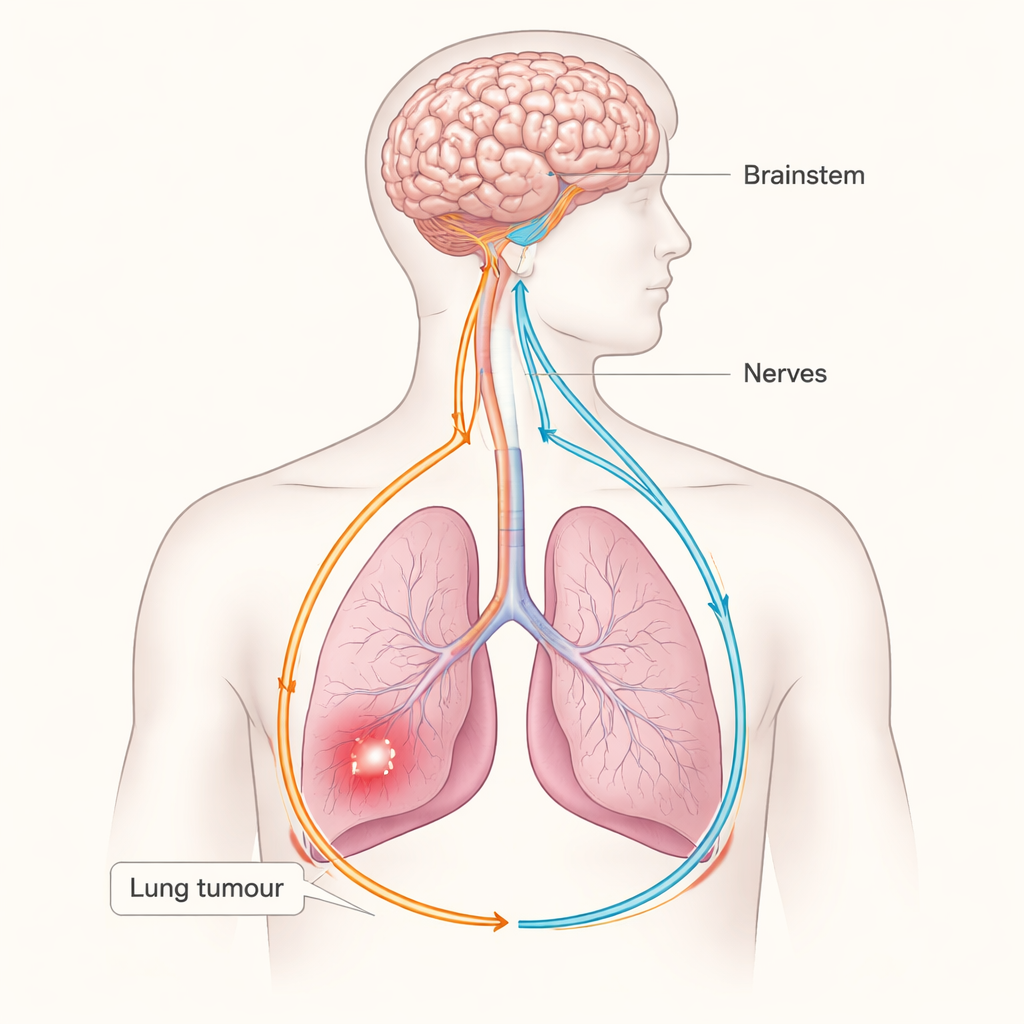
Tümörün İçine Büyüyen Sinirler
Araştırma ekibi, insan hastalığını yakından taklit eden gelişmiş fare modellerinde yaygın bir akciğer kanseri türü olan akciğer adenokarsinomunu inceledi. Tüm organ 3B görüntüleme ve genetik etiketleme kullanarak, akciğerlerdeki tümörlerin yoğun sinir lifleriyle donatıldığını buldular. Bu sinirler rastgele değildi: birçokları, normalde organ sağlığına dair bilgiyi beyne taşıyan vagus sinirindeki belirli bir duyu hücresi grubundan geliyordu. Tümör hücrelerinin, bu vagal duyu liflerinin filizlenmesini ve tümöre girmesini teşvik eden sinir büyüme faktörü gibi büyümeyi destekleyen proteinler salgıladığı gözlendi. Aynı zamanda, duyu nöronlarının kendilerinin gen etkinlikleri değişmişti; bu da tümörün, sağlıklı akciğer dokusundakinden farklı yanıt vermeleri için onları yeniden programladığını düşündürüyor.
Tümöre Dost Sinyaller İçin Tek Yönlü Bir Güçlendirme
Tüm vagus bağlantılı duyu nöronları işin içinde değildi. Araştırmacılar, NPY2R ve TRPV1 adlı iki molekül tarafından işaretlenen bir alt tipin başrol oynadığını belirledi. Bu nöronlar tümör bölgeleri içinde bolca bulunurken, yakındaki normal akciğerde büyük oranda yoktu. Bilim insanları bu NPY2R/TRPV1 grubunu genetik hileler, hedefli toksinler veya bir ilaçla kapatılabilen tasarım reseptörleri kullanarak seçici şekilde ortadan kaldırdıklarında veya susturduklarında—akciğer tümörleri dramatik şekilde küçüldü ve fareler daha uzun yaşadı, kilo ve davranışları düzeldi. Buna karşın, diğer akciğer yapılarını innerve eden farklı bir duyu alt grubunun kaldırılması tümör büyümesini yavaşlatmadı; bu da yalnızca belirli bir duyu “kanalının” kanser kontrolüne bağlı olduğunu vurguluyor. 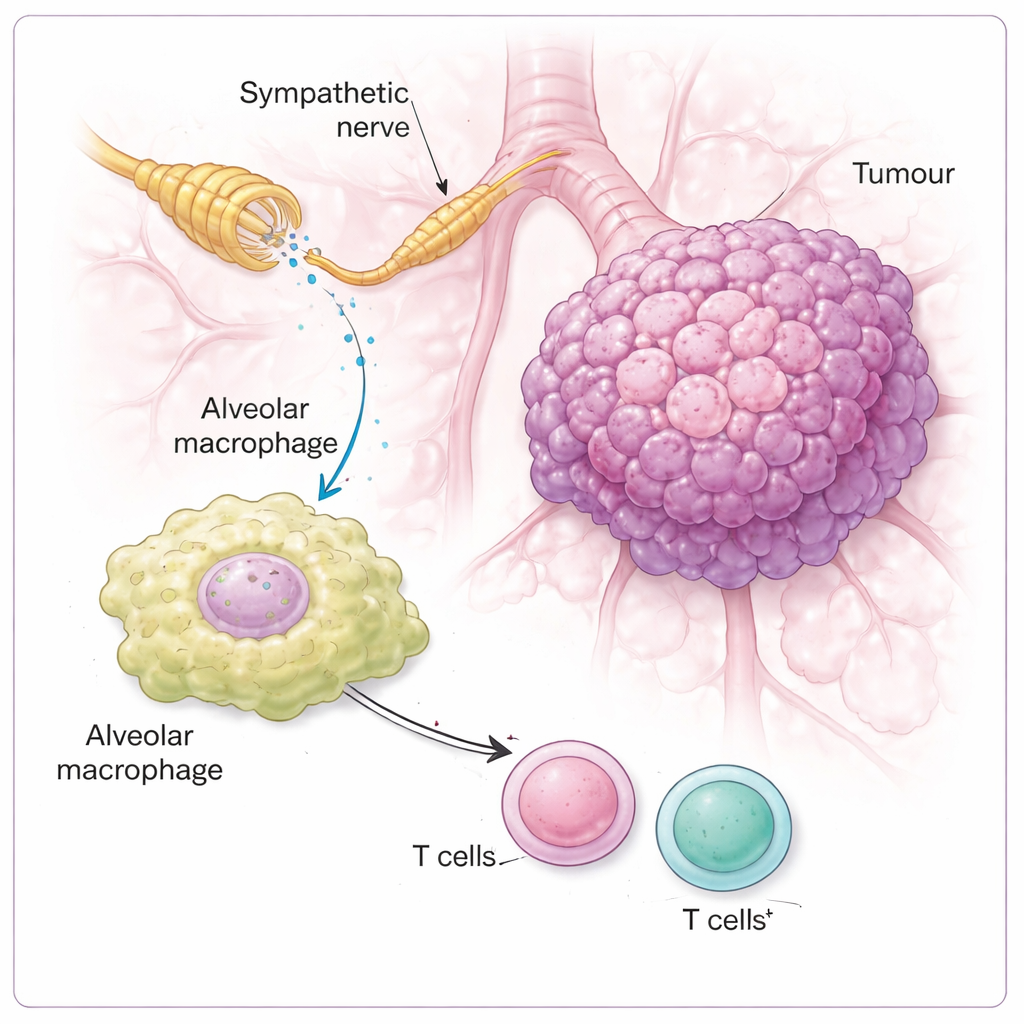
Beyin sapından akciğerde stres-benzeri sinyallere
Bu duyu sinyallerinin beyin tarafından nasıl işlendiğini görmek için ekip devreyi yukarı doğru izledi. Aktivitiyı işaretleyen göstergeler, akciğer tümörleri mevcut olduğunda vagal girdi alan beyin sapı bölgelerinin özellikle rostral ventrolateral medulla adı verilen ve sempatiği (savaş ya da kaç) artıran önemli bir merkezin aktifleştiğini gösterdi. NPY2R/TRPV1 duyu nöronlarını kapatmak bu beyin sapı aktivitesini sakinleştirdi ve tümör bölgesindeki sempatik sinir liflerinin sayısını ve stres habercisi noradrenalin düzeylerini azalttı. Beyin sapındaki hub’ı doğrudan susturmak da tümör büyümesini yavaşlattı. Birlikte, bu sonuçlar kapalı bir döngüyü özetliyor: tümör vagal duyu sinirlerini uyarıyor, beyin sapı sempatik çıkışı artırarak yanıt veriyor ve sempatik sinirler kanseri avantajlı kılan biçimde akciğer ortamına geri besleme yapıyor.
Yerel Aracı Hücreler Yoluyla Bağışıklık Hücrelerini Kapatmak
Çalışma daha sonra tümör çevresindeki hangi hücrelerin gerçekten sempatik sinyalleri “duyduğunu” sordu. Şaşırtıcı şekilde, noradrenalinin bir petri kabındaki tümör hücresi büyümesi üzerinde doğrudan çok az etkisi vardı. Bunun yerine kilit tepki verenler bağışıklık hücreleri, özellikle akciğerin hava keseciklerinde bulunan nöbetçi hücreler olan alveoler makrofajlardı. Bu makrofajlar noradrenalini algılayan β2-adrenerjik reseptörü yüksek düzeyde taşıyordu. Bu reseptör yok olduğunda ya da noradrenalin sinyallemesi engellendiğinde tümörler daha az büyüdü ve T hücrelerinin bağışıklık saldırısı güçlendi. Sinir devresi sağlam olan farelerde noradrenalin makrofajları daha baskılayıcı bir duruma itti; bu durum ARG1 adlı enzimin daha yüksek seviyeleriyle işaretlendi ve ARG1’in T hücrelerini baskıladığı biliniyor. Makrofajlar bu şekilde yeniden programlandığında, yakındaki CD4 ve CD8 T hücreleri—normalde vücudun ön saflarındaki kanser katilleri—güçlü bir yanıt oluşturmakta daha az başarılı oldu.
Kanser Tedavisi Açısından Neden Önemli
Özetle, yazarlar akciğer tümörlerinin vagus siniri aracılığıyla beyinle “konuşabildiğini” ve sempatik sinirler üzerinden yerel makrofajlara T hücrelerini yatıştırmalarını söyleyen zararlı bir yanıt alabildiğini gösteriyor. Bu döngüdeki herhangi bir önemli bağın—duyu girişi, beyin sapı rölesi, sempatik çıkış veya makrofajlardaki β2-adrenerjik sinyalleme—kesilmesi, daha güçlü anti-tümör bağışıklığı geri getirip farelerde kanseri yavaşlatmaya yetti. İnsan akciğer kanseri verileri de, tümörlerinde bu sinir yollarının daha yüksek imzalarını gösteren hastaların genelde daha kötü gittiğini ve tümörlerinde daha az katil T hücre bulunduğunu öne sürdü. Bu çalışma, beta-blokerler gibi kalp hastalığı ve anksiyete için zaten kullanılan ilaçların veya belirli sinir devrelerini hedef alan gelecekteki tedavilerin, tümörlerin bağışıklıktan kaçmak için kullandığı “kabloları kesmek” amacıyla yeniden değerlendirilebileceği veya rafine edilebileceği olasılığını gündeme getiriyor.
Atıf: Wei, H.K., Yu, C.D., Hu, B. et al. Tumour–brain crosstalk restrains cancer immunity via a sensory–sympathetic axis. Nature 650, 1007–1016 (2026). https://doi.org/10.1038/s41586-025-10028-8
Anahtar kelimeler: kanser nörobilim, akciğer kanseri bağışıklığı, vagus siniri, sempatik sinir sistemi, tümör mikroçevresi