Clear Sky Science · tr
Bireyselleştirilmiş mRNA aşıları, adjuvan TNBC'de kalıcı T hücre bağışıklığı uyandırıyor
Meme kanseri tedavisinden sonra yeni bir umut
Üçlü negatif meme kanseri adı verilen agresif bir formla yaşayan birçok kadın için kemoterapi ve cerrahi bittikten sonra korku bitmiyor. Bu kanserin tekrarlama ve yayılma riski yüksek olup genellikle sadece birkaç yıl içinde yeniden ortaya çıkabiliyor. Burada anlatılan çalışma, her hastanın kendi tümör mutasyonlarından oluşturulan son derece kişiselleştirilmiş bir aşıyı test ediyor; amaç, bağışıklık sistemini yıllarca nöbet tutacak şekilde eğitip standart tedavi tamamlandıktan sonra nüks riskini azaltıp azaltamayacağını görmek.
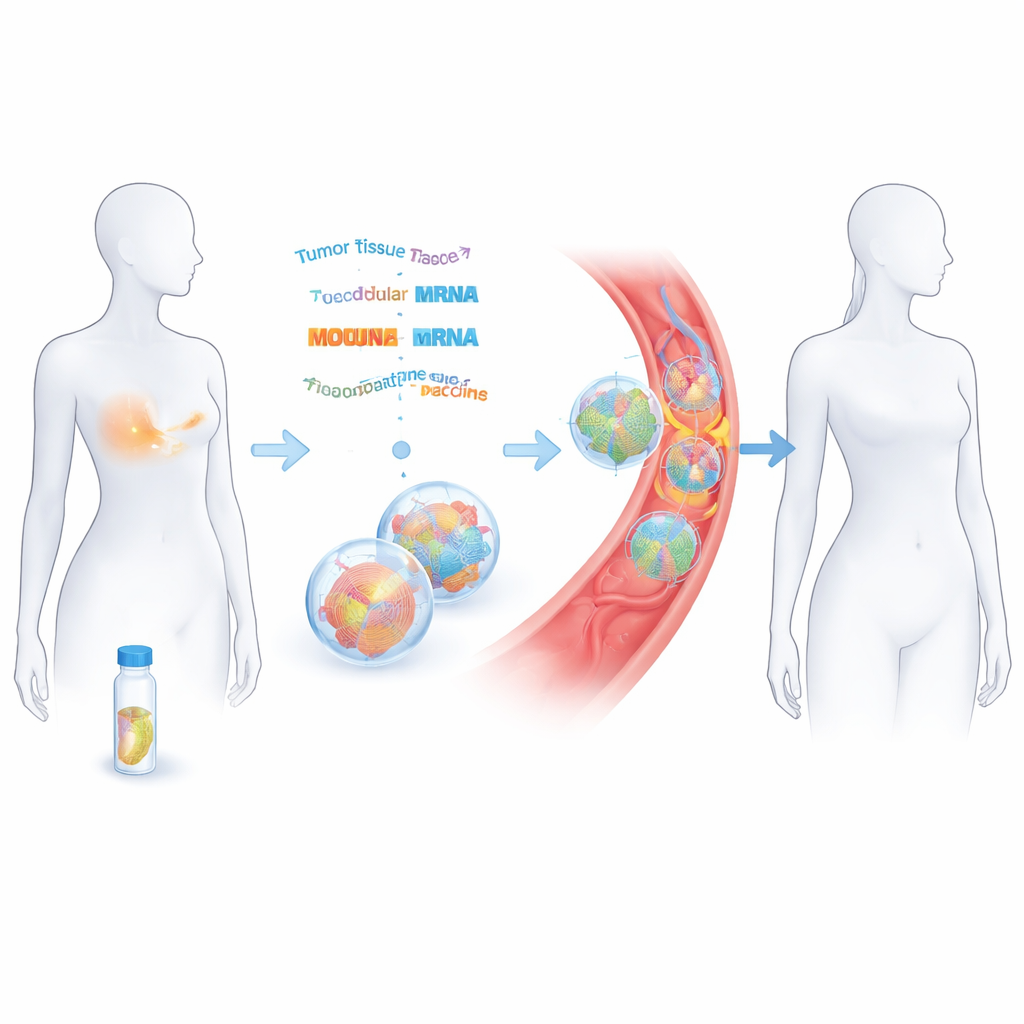
Alınan tümörü nasıl özel bir aşıya dönüştürdüler
Araştırmacılar, cerrahi ve kür amaçlı kemoterapi görmüş erken evre üçlü negatif meme kanserli 14 kadınla çalıştı. Çıkarılan tümör dokusundan DNA ve RNA dizilimi yaparak kanserin benzersiz mutasyonlarını katalogladılar. Bilgisayar araçları kullanarak, bu değişikliklerden hangilerinin bağışıklık hücreleri tarafından yabancı olarak algılanabileceğini tahmin ettiler. Seçilen bu “neoantijen”lerden en çok 20 tanesi bir araya getirilip haberci RNA (mRNA) iki zincire kodlandı; temel ilke olarak COVID‑19 aşılarına benziyor ama her hasta için özel olarak tasarlandı. Bu mRNA zincirleri küçük yağ baloncukları içinde paketlendi ve yaklaşık iki aylık sürede damardan sekiz doz halinde verildi.
Aşı, bağışıklık savunucularını nasıl uyandırıyor
Vücuda girdikten sonra mRNA, dendritik hücreler adı verilen bağışıklık nöbetçilerine bu neoantijen proteinlerini kısa süreliğine üretmelerini ve bunların parçalarını yüzeylerinde sergilemelerini talimatlandırır. Bu, T hücreleri için bir aranan kişi afişi gibi davranır; T hücreleri bağışıklığın başlıca kanser yok edici gücüdür. Ekip, aşılama öncesi ve sonrasında birkaç zaman noktasında kan alarak neoantijene özgü T hücrelerinin ortaya çıkıp çıkmadığını ve ne kadar güçlü olduklarını test etti. Hassas laboratuvar testleriyle, her hastanın seçilen mutasyonlardan en az birine karşı yeni veya güçlenmiş T hücre yanıtı geliştirdiği ve çoğunun birkaçına yanıt verdiği bulundu. Birçok durumda, dolaşımdaki T hücrelerinin büyük kesimleri—genellikle yalnızca güçlü hücre terapilerinde görülen seviyeler—tümöre özgü hedefleri tanımaya ayarlandı.
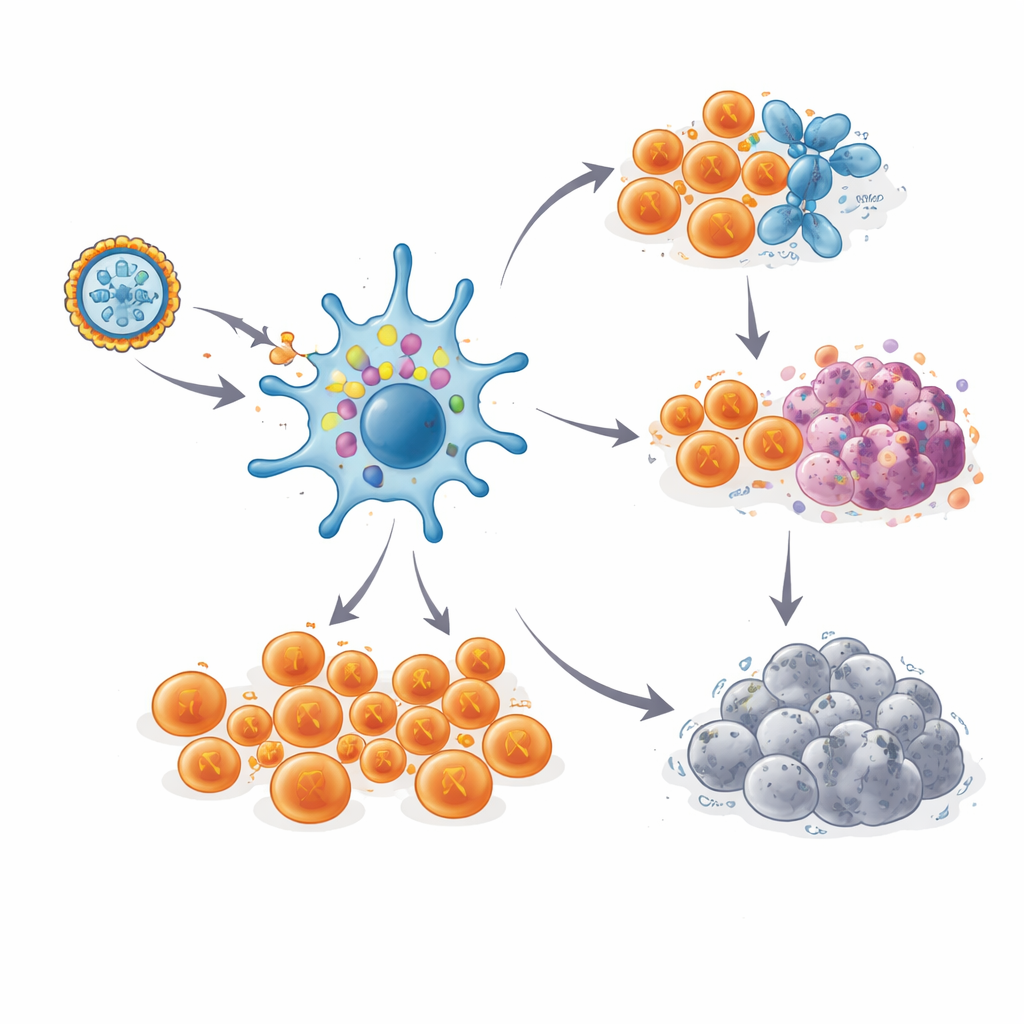
Uzun ömürlü bağışıklık hafızası
Önemli olarak, bu T hücre yanıtları hızla kaybolmadı. Çoğu hastada güçlü yanıtlar aşılama döneminde zirve yaptı, biraz düştü ve ardından takviye olmadan bir ila üç buçuk yıl boyunca yüksek seviyelerde kaldı. Bireysel T hücresi klonlarının benzersiz reseptör “barkodlarını” izleyerek araştırmacılar, kanserden uzak kalan bir hastada belirli neoantijene reaksiyon veren hücreleri altı yıla kadar takip edebildi. Tek hücre analizleri, bu hücrelerin iki ana kaderini gösterdi. Birçoğu doğru neoantijeni taşıyan herhangi bir hücreyi yoklamaya hazır, güçlü silahlanmış öldürücü T hücrelere dönüştü. Diğerleri ise kendini yenileme belirtileri taşıyan daha nadir, kök‑benzeri bir hafıza havuzuna gelişti; bu da kanser hücreleri yeniden ortaya çıkarsa yeni savaşçı dalgalarını üretebilecek bir rezervuar olduğunu düşündürüyor.
Hastalara ne oldu
İlk aşı dozundan itibaren ortanca biraz üzerinde beş yıllık takip sonunda, on dört kadından on birinde kanserin geri dönüşü gözlenmedi; bunlardan biri remisyon halindeyken ilişkili olmayan nedenlerle yaşamını yitirdi. Üç kadın nüksetti ve bu vakalar, kişiselleştirilmiş aşıların bazen neden başarısız olabileceğine dair ipuçları sunuyor. Bir hastada yalnızca zayıf bir T hücre yanıtı oluştu ve daha sonra anti‑PD‑1 antikoru gibi farklı bir immünoterapi ilacından yarar gördü, fakat sonunda yaygın hastalığa yenik düştü. İkinci hastada kalıtsal risk ve her iki memede tümörler vardı; aşı tasarımı için yalnızca bir tümör kullanılmıştı ve daha sonra elde edilen kanıtlar nüksün genetik olarak farklı, aşılanmamış tümörden kaynaklandığını gösterdi. Üçüncü hastada güçlü aşı kaynaklı T hücreleri nüks eden tümörü infiltre etti, ancak kanser hücreleri yüzeylerinde neoantijenleri göstermek için gerekli anahtar moleküllerin büyük ölçüde kaybını yaşamıştı, böylece bağışıklıktan etkin bir şekilde saklandılar.
Gelecek için neden önemi var
Bu erken aşama çalışma küçük ve kontrol grubuna sahip değildi, dolayısıyla aşının tek başına nüksleri önlediğini kanıtlayamaz. Yine de, bir hastanın kendi tümöründen karmaşık, özel bir mRNA aşısı oluşturmanın rutin hastane koşullarında yapılabilir olduğunu, genel olarak iyi tolere edildiğini ve birden çok kanser‑özgü hedefe karşı güçlü, uzun ömürlü T hücresi ordularını tetikleyebileceğini gösteriyor. Bulgular ayrıca tümörlerin antijen gösterim mekanizmasını kaybetme veya hedeflenmemiş lezyonlardan kaynaklanma gibi kaçış yollarını vurguluyor; bu da diğer immünoterapilerle kombinasyonlara ve daha kapsamlı tümör dizilemesine işaret ediyor. Üçlü negatif meme kanseriyle yüzleşen hastalar için bu çalışma, standart tedaviden sonra uygulanan kişiye özel bir aşının, bağışıklık sistemlerini kalıcı, yüksek özgüllüğe sahip bir savunma hattına dönüştürerek hastalığın geri dönmesini engellemeye bir gün yardımcı olabileceğini düşündürüyor.
Atıf: Sahin, U., Schmidt, M., Derhovanessian, E. et al. Individualized mRNA vaccines evoke durable T cell immunity in adjuvant TNBC. Nature 651, 1088–1096 (2026). https://doi.org/10.1038/s41586-025-10004-2
Anahtar kelimeler: üçlü negatif meme kanseri, mRNA kanser aşıları, neoantijen immünoterapisi, T hücresi bağışıklığı, tümör nüksü