Clear Sky Science · tr
Poliamine-bağımlı metabolik kalkan alternatif eklemeyi düzenler
Hücrelerin Genlerini Nasıl Okuduğuna Küçük Moleküller Nasıl Yardımcı Olur
Her hücrenin içinde aynı DNA metni birçok farklı şekilde okunabilir; bu sayede sınırlı sayıda gen çok çeşitli proteinler üretebilir. Bu esneklik, proteinlere dönüşmeden önce RNA mesajlarını düzenleyen alternatif ekleme adlı bir sürece dayanır. Bu makale, pozitif yüke sahip küçük moleküller olan poliaminlerin, hücrelerin hangi RNA versiyonlarını üreteceğine karar vermesine yardımcı olan koruyucu bir kalkan gibi bu düzenleme adımını sessizce yönlendirdiğini ortaya koyuyor. Alternatif ekleme kanser, beyin fonksiyonu ve kök hücrelerde kritik olduğundan, bu gizli kontrol katmanının ortaya çıkarılması sağlık ve hastalık için geniş kapsamlı çıkarımlar taşıyor.
Her Hücredeki Küçük Yüklü Yardımcılar
Poliaminler çok sayıda pozitif yük taşıyan küçük, esnek moleküllerdir. Hücreler onları temel besinlerden üretir ve özellikle tümörler gibi hızlı çoğalan hücrelerde büyüme ve hayatta kalma yardımcıları olarak uzun zamandır bilinirler. Yazarlar, poliaminlerin yalnızca yakıt değil, aynı zamanda birer sinyal görevi görüp görmediğini sordular. Prostat kanseri hücrelerinde ve farelerde poliamin üretimini kısmen engelleyerek, proteinlerin ve RNA’nın zaman içinde nasıl değiştiğini ölçtüler. Toplam poliamin düzeyleri dramatik şekilde düşmeden çok önce, özellikle hücresel RNA düzenleme mekanizmasının bileşenleri olan spliceozom üzerinde, protein fosforilasyonunda—protein anahtarlarını açıp kapatan kimyasal etiketlerde—güçlü bir değişim dalgası olduğunu buldular.
Hücrenin RNA Düzenleyicisini Yeniden Kabllama
Takım, özellikle RNA’ya bakarak, poliamin sentezi engellendiğinde alternatif eklemeyi derin dizileme ile izledi. Yüzlerce RNA segmenti kanser hücre hatlarında, normal hücre tiplerinde ve fare dokularında farklı şekilde atlandı ya da dahil edildi. Bu değişiklikler basitçe daha yavaş hücre bölünmesinin ya da hipusinasyon adıyla bilinen başka bir poliamin-bağımlı sürecin yan ürünü değildi. Bunun yerine, araştırmacılar hücrelere dışarıdan poliamin sağlayınca birçok ekleme değişikliğinin normale doğru geri döndüğünü gördüler. Poliaminleri düşüren hem ilaçlar hem de genetik araçlar benzer ekleme desenleri üretirken, poliaminleri ilaç kombinasyonuyla daha da azaltmak değişiklikleri güçlendirdi; bu da etkinin poliamin mevcudiyetiyle sıkı şekilde ilişkili olduğunu doğruladı.
Gizli Bir Hedef: SF3 Ekleme Modülü
Poliaminlerin ekleme makinesinin neresinde etkili olduğunu belirlemek için yazarlar, poliamin düzeylerini düşürmenin yol açtığı ekleme imzasını, 300’den fazla bilinen ekleme faktörünün tek tek susturulmasıyla oluşturulmuş geniş bir referans haritasıyla karşılaştırdı. En yakın eşleşme, RNA’daki temel işaretleri tanımaya yardımcı olan spliceozomun SF3 altkompleksinin belirli bir parçasına işaret etti. Kamuya açık protein–RNA bağlanma verilerinin hesaplamalı analizi bu bağlantıyı destekledi: poliamin kaybıyla eklemesi değişen RNA’lar özellikle SF3 proteinleri tarafından bağlanma eğilimindeydi. Takım SF3 bileşenlerini kısmen genetik olarak veya bir ilaçla devre dışı bıraktığında, poliamin tükenmesinin ekleme etkileri büyük ölçüde ortadan kalktı; bu da sağlam SF3 aktivitesinin bu yeni düzenleyici yol için gerekli olduğunu gösterdi. 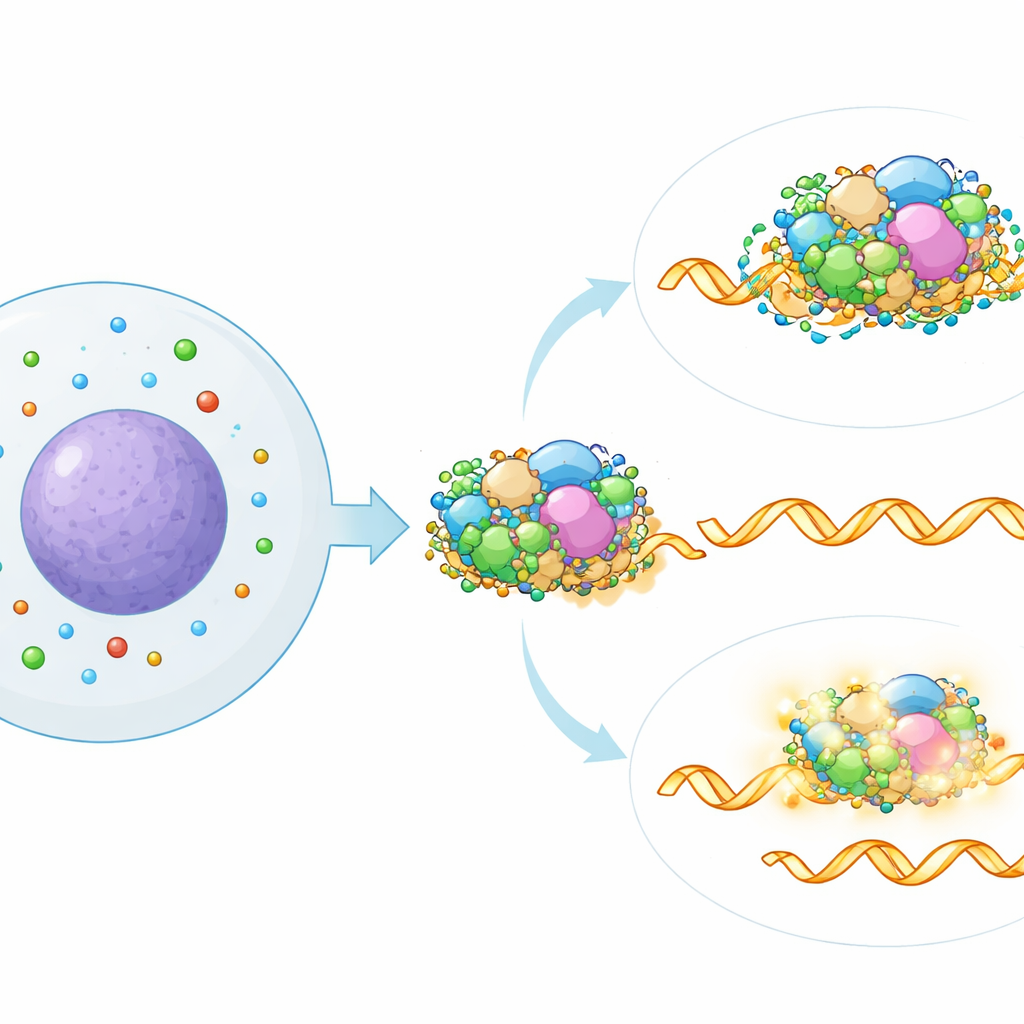
Metabolik Kalkan: Poliaminlerin Protein Etiketlemesini Nasıl Engellediği
Daha derine indiklerinde, araştırmacılar SF3 proteinlerindeki en güçlü etkilenen fosforilasyon bölgelerinin negatif yüklü aminoasitlerle zengin kısa diziler içinde kümelendiğini fark ettiler. Moleküler modelleme ve nükleer manyetik rezonans deneyleri, poliaminlerin bu asidik yamalara yerleşip çoklu elektrostatik temaslar kurduğunu ve genellikle fosfat gruplarının eklendiği yakınlardaki serin kalıntılarını kısmen örttüğünü gösterdi. Bu fiziksel “sarılma”, bu noktaların protein kinazlar—fosfat ekleyen enzimler—için erişilebilirliğini azaltıyor. Deney tüpü deneylerinde poliamin eklemek, CK1 adlı bir kinazın SF3 proteinlerini fosforilemesini doğrudan engelledi. Hücrelerde CK1 ve yakını CK2’yi inhibe etmek, poliamin kaybının yol açtığı ekleme değişikliklerini azalttı; özel olarak tasarlanmış ve SF3A3 proteini üç ana fosforilasyon sitesinden yoksun fareler ise poliamin-bağımlı ekleme kaymalarına büyük ölçüde duyarsız hale geldi. 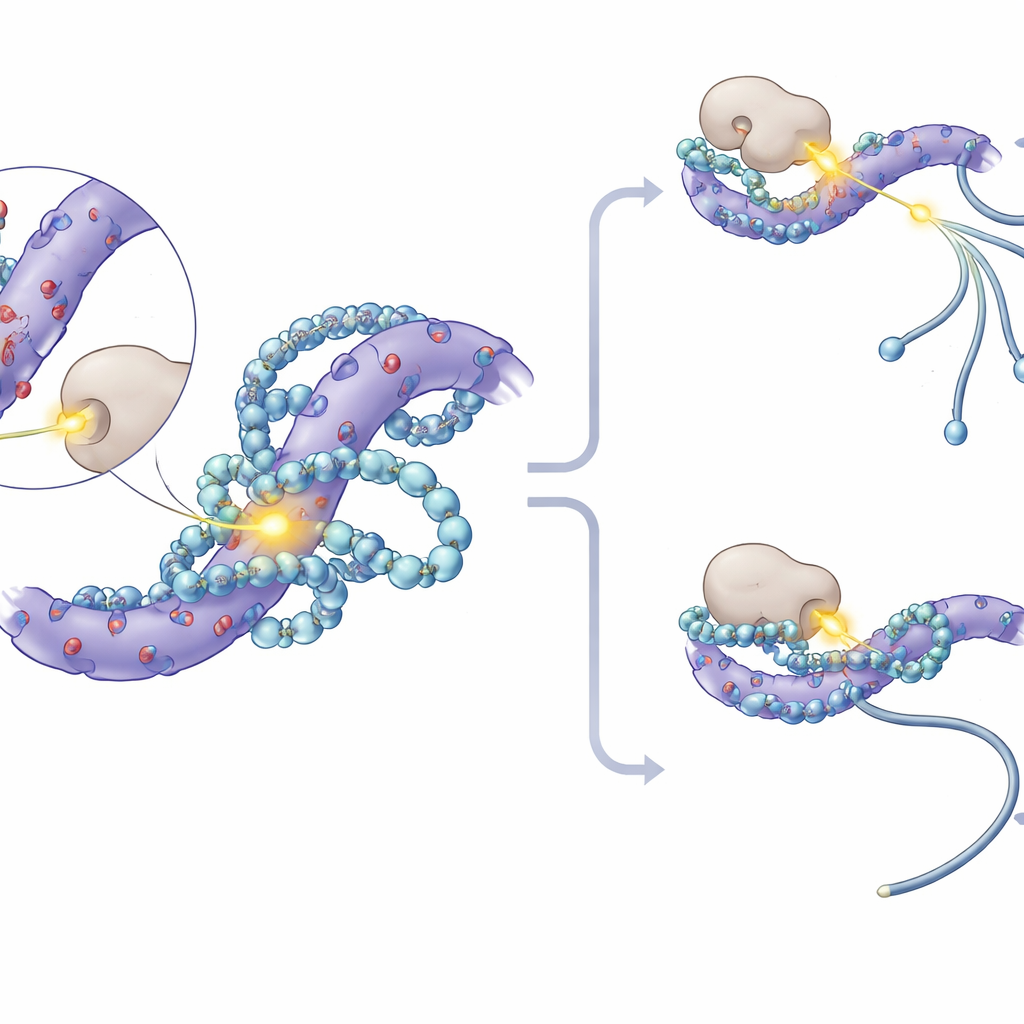
Rolleri Ayıran Tasarım Molekülü
Çalışma ayrıca, hücrenin kendi poliamin üretimini aynı anda kapatan ancak daha güçlü pozitif yüke sahip poliamin-benzeri bir ilaç olan BENSpm’i tanıtıyor. BENSpm, doğal poliaminler gibi SF3 asidik yamalarına sıkı bağlandı ve kinaz etkisini engelledi; ancak gerçek poliaminler kısıtlıyken hücre büyümesini kurtarmadı. Bu, yazarların klasik poliamin işlevlerini (büyüme ve metabolizmayı destekleme) yeni tanımlanan kalkan rolünden ayırmasını sağladı. Fare embriyonik kök hücrelerinde poliaminlerin tükenmesi, hücreleri “kök hücrelik” belirteci Nanog’u kaybetmeye itip ekleme manzaralarını değiştirdi. BENSpm, normal poliamin sentezinin süregelen baskılanmasına rağmen ekleme profilini ve Nanog ifadesini geri getirdi; bu da metabolik kalkanlamanın kök hücre kimliğinin korunması için kilit bir gereklilik olduğunu gösteriyor.
Bu Keşfin Önemi
Günlük terimlerle, bu çalışma poliaminlerin anahtar ekleme proteinlerinin hassas kısımları etrafında küçük koruyucu eldivenler gibi davrandığını gösteriyor. Eldivenler takılıyken kinazlar bu bölgeleri kolayca yakalayıp etiketleyemiyor ve hücrenin RNA düzenlemesi yolunda kalıyor. Poliaminler azaldığında ise eldivenler çıkar, fosforilasyon artar ve ekleme desenleri değişir; bu durum hem kanser hücreleri hem de kök hücreler için sonuçlar doğurur. Bu “metabolik kalkan” mekanizmasını tanımlayarak ve bunu seçici olarak taklit eden bir araç molekül sunarak çalışma, DNA’yı değiştirmeden gen okumasını ayarlamanın yeni yollarına kapı açıyor; bu da gelecekte kanser ve rejeneratif tıpta eklemeyi hedef alan terapilere ilham verebilir.
Atıf: Zabala-Letona, A., Pujana-Vaquerizo, M., Martinez-Laosa, B. et al. Polyamine-dependent metabolic shielding regulates alternative splicing. Nature 651, 819–828 (2026). https://doi.org/10.1038/s41586-025-09965-1
Anahtar kelimeler: poliaminler, alternatif ekleme, RNA işlenmesi, metabolik sinyalizasyon, kök hücre düzenlemesi