Clear Sky Science · tr
Ligand-spesifik aktivasyon yolları hücrelerde GPCR sinyalini belirler
Bir Reseptörün Nasıl Birçok Anahtar Gibi Davranabildiği
Günümüzdeki birçok ilaç, hücre yüzeyinde yer alan ve G-protein–bağlantılı reseptörler (GPCR’ler) olarak adlandırılan büyük bir protein ailesi üzerinde etki gösterir. Bu reseptörler kalp atış hızını, ruh halini, solunumu ve sayısız diğer bedensel işlevi etkiler. On yıllarca basit açma–kapama anahtarları gibi düşünüldüler: bir ilaç bağlanır, anahtar çevrilir ve hücre içine sinyal akar. Bu makale, gerçeğin çok daha zengin olduğunu gösteriyor. Reseptörün içine doğrudan yerleştirilen yeni bir tür floresan “casus” kullanarak, yazarlar canlı hücrelerde farklı ilaçların aynı reseptörü farklı aktivasyon yollarına —şehri kat eden farklı rotalar seçmeye benzer biçimde— yönlendirdiğini ve böylece farklı sinyal desenleri ürettiğini izliyor. Bu gizli yolları anlamak, istenen faydayı sağlarken yan etkilerden kaçınan ilaçların tasarımına yardımcı olabilir.
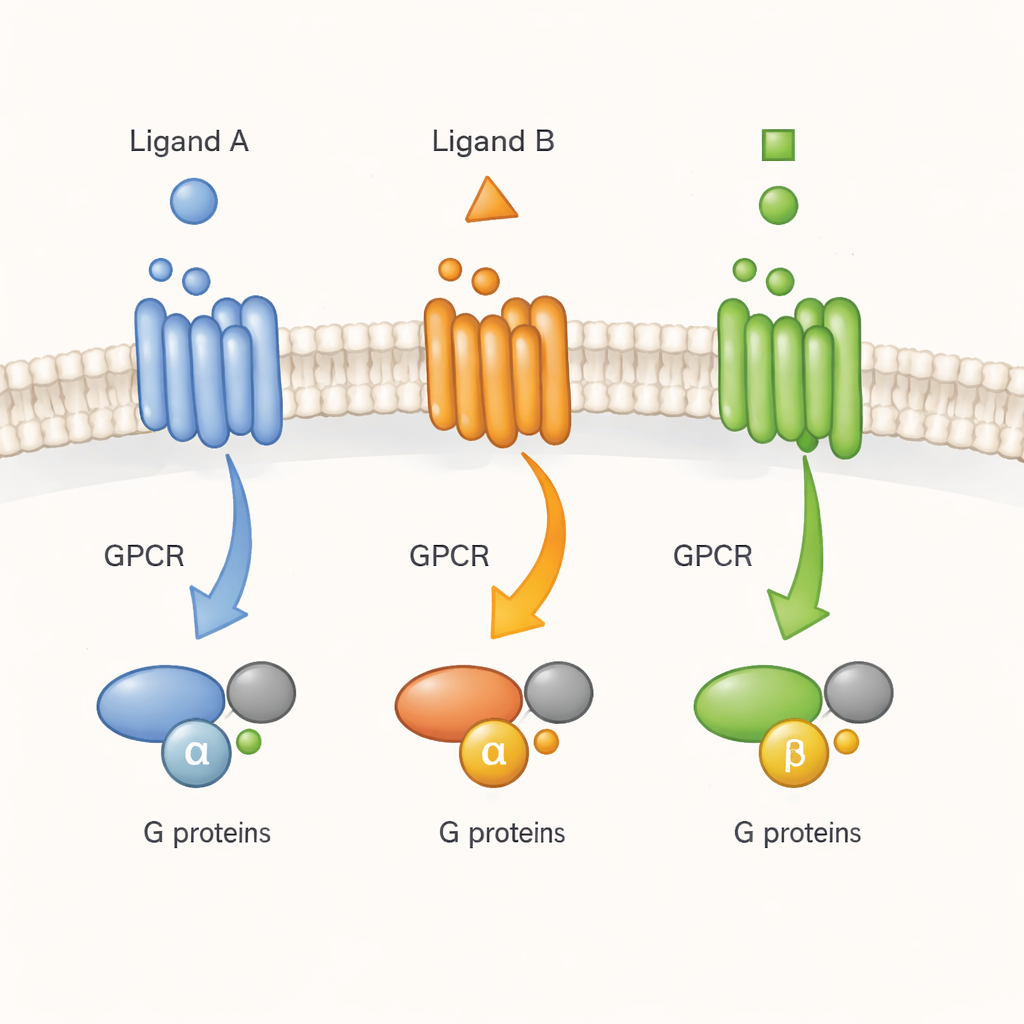
Bir Hücrenin Kapı Ziline Gerçek Zamanlı Bakmak
GPCR’ler sıklıkla moleküler kapı zilleri olarak tanımlanır: dışarıdan bir sinyal molekülü (ligand) çalar ve reseptör mesajı hücre içindeki G proteinlerine iletir. Önceki çalışmalar, deterjan içindeki saflaştırılmış reseptörlerle GPCR’lerin yalnızca bir inaktif ve bir aktif şekil arasında gidip gelmediğini değil, bunun yerine ilaçların farklı derecelerde stabilize edebildiği birçok şekil denediğini öne sürmüştü. Ancak aynı karmaşıklığın canlı bir hücrenin kalabalık ve dinamik ortamında da var olup olmadığı belirsizdi. Burada yazarlar, kalp ve sinir aktivitesinin önemli bir düzenleyicisi olan temsilî bir reseptör, M2 muskarinik asetilkolin reseptörüne odaklanıyor ve farklı ligandların gerçek hücresel sinyalleme için önemli olan farklı aktif formlara sürükleyip sürüklemediğini sorguluyorlar.
Reseptör Yüzeyine Küçük Işık Raporörleri İnşa Etmek
Reseptörün hareketlerini normal işlevini bozmayacak şekilde izleyebilmek için ekip, reseptörün dış yüzeyindeki seçili pozisyonlara özel tasarım bir aminoasit yerleştirmelerini sağlayan genetik kod genişletme teknolojisini kullandı. Bu kimyasal “çapa”, canlı hücrelerde küçük bir floresan boya ile tıklanarak bağlanabiliyor. 72 pozisyonu tarayarak ve hâlâ normal reseptörler gibi davrananları seçerek, her biri farklı bir dış-döngü bölgesinde tek bir boya taşıyan yedi M2 reseptör varyantından oluşan bir panel oluşturdular. Doğal habercisi asetilkolin uygulandığında, bu bölgelerdeki boya parlaklığı karakteristik biçimlerde yükselip azaldı ve sinyalleşme başladıkça reseptörün dış yüzeyinin her bir kısmının nasıl yer değiştirdiğini ortaya koydu. Önemli olarak, bu etiketli reseptörler hâlâ G proteinlerini aktive edebiliyor ve normal internalizasyona uğrayabiliyordu; bu da raporlayıcıların bozucu değil, güvenilir olduğunu gösterdi.
İlaçlar Farklı “Konformasyonel Parmak İzi” Bırakıyor
Araştırmacılar daha sonra M2 reseptörünü açan fakat farklı güçlerde etkili olan birkaç ilacı karşılaştırdı: vücudun kendi asetilkolini, iperoxo adlı süper güçlü sentetik bir agonist ve iki daha zayıf kısmi agonist olan arekolin ve pilokarpin. Her ilaç, yedi raporör bölgesi boyunca benzersiz bir floresans değişim deseni —bir konformasyonel parmak izi— üretti. Çoğu pozisyonda hareketin büyüklüğü, ilacın reseptörü ne kadar güçlü aktive ettiğini yansıttı. Ancak iki bölgede ilişki tersine döndü: daha zayıf ilaçlar en büyük değişiklikleri üretirken, en güçlü ilaç neredeyse hiçbir değişiklik üretmedi. Böyle bir davranış tek bir aktif durumla açıklanamaz. Bunun yerine, aynı reseptörün canlı hücrelerde güçlü ilaçların tercih ettiği ve zayıf ilaçların tercih ettiği farklı birkaç aktif şekil alabileceğini gösterir.
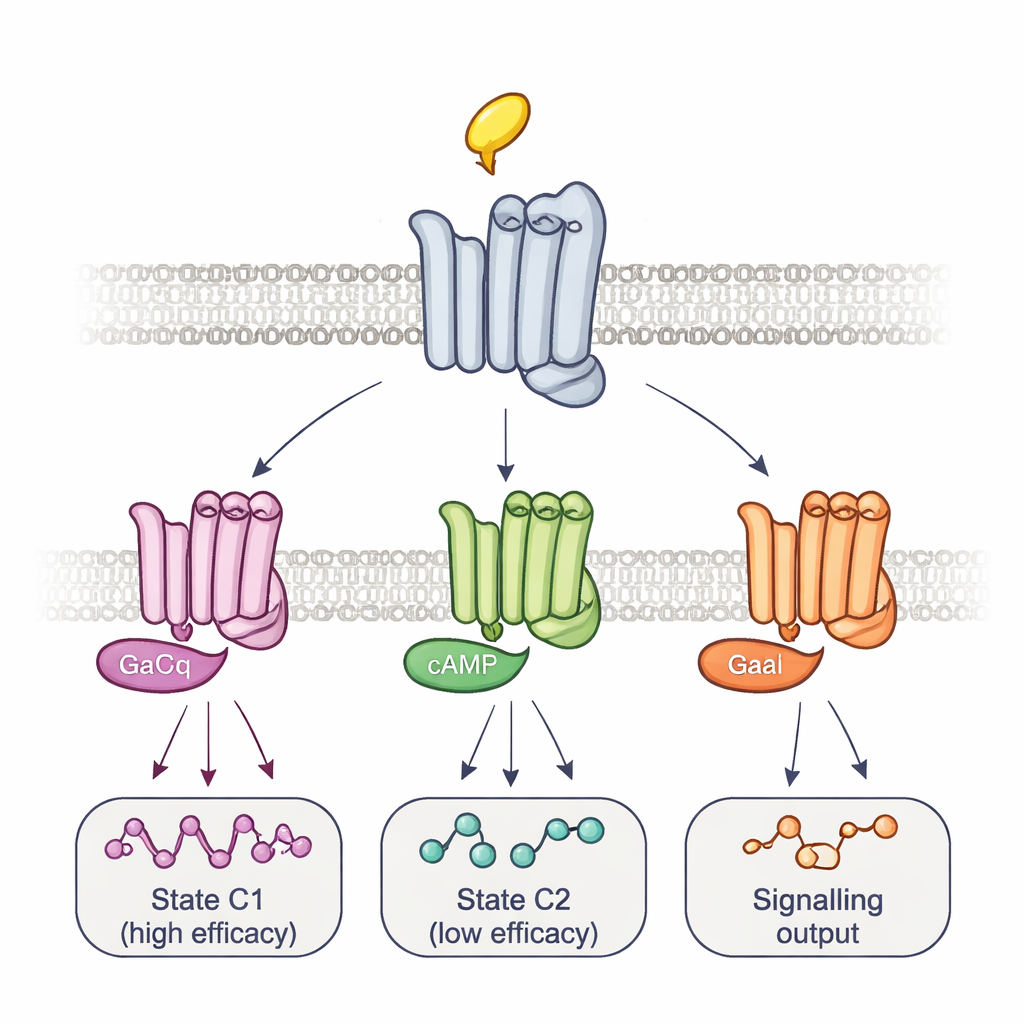
Çoklu Kompleksler ve Zamanlanmış Sinyal Yolları
Bu şekilleri gerçek sinyallemeye bağlamak için ekip, G proteinlerini kendileri değiştirdi. Reseptörlerle çok sıkı, uzun ömürlü kompleksler oluşturan mutant bir G proteinin aşırı eksprese edilmesi, bazı raporör bölgelerinin sinyalini seçici olarak yok ederken diğerlerini güçlendirdi. Bu desen, birlikte floresans değişikliklerinin zamanlamasıyla, en az iki ana reseptör–G protein kompleksini ortaya koydu: hızlı oluşan, yüksek etkinlikli bir kompleks ve daha yavaş, düşük etkinlikli bir kompleks. Farklı ilaçlar bu kompleksler arasındaki dengeyi kaydırdı ve oraya ulaşmak için farklı ara adımlar kullandı; ilaç-spesifik aktivasyon rotalarını izlediler. 14 G-protein alt tipini izleyen ayrı bir biolüminesans testinde yazarlar, bu dengelerin sadece bir ilacın genel olarak sinyali ne kadar güçle aktive ettiğini değil, hangi kesin G proteinlerinin açıldığını da belirlemeye yardımcı olduğunu gösterdi. Örneğin arekolin belirli Go proteinlerini tercihli olarak aktive ederken, pilokarpin düşük etkinlikli kompleksi güçlü biçimde tercih etti.
İyi İlaçlar İçin Neden Önemli
Uzman olmayanlar için temel mesaj şudur: tek bir reseptör yalnızca bir anahtar değil, farklı yollarla ulaşılan ve her biri biraz farklı aşağı akış etkilerine bağlı ilişkili anahtarlar kümesidir. Bu çalışma, bu yolların ve durumların hücre bütünlüğü içinde, basitleştirilmiş test tüpü sistemleri yerine doğrudan görünümünü sağlıyor. Belirli ilaçların reseptörü hangi komplekslere ve hangi G-protein ortaklarına yönlendirdiğini haritalandırarak araştırmacılar, faydalı sinyalleri tetikleyen, yan etkilerle ilişkili olanlardan kaçınan “daha akıllı” ilaçlar tasarlamak için bir plan elde ediyor. Burada geliştirilen floresan biyosensör stratejisi birçok başka reseptöre uyarlanabilir olmalı ve canlı hücrelerde ilaç etkisinin gerçek zamanlı koreografisine bir pencere açıyor.
Atıf: Thomas, R., Jacoby, P.S., De Faveri, C. et al. Ligand-specific activation trajectories dictate GPCR signalling in cells. Nature 650, 1053–1062 (2026). https://doi.org/10.1038/s41586-025-09963-3
Anahtar kelimeler: GPCR sinyalleşmesi, ligand etkinliği, G proteinleri, konformasyonel biyosensörler, ilaç keşfi