Clear Sky Science · tr
İki Yönlü CRISPR ekranları GLIS3’e bağlı bir fibrotik hücre devresini çözümlüyor
İyileşme Zarara Dönüştüğünde: Yararlı Bir Sürecin İz Bırakan Sonucu
Bağırsaklarımız her çizik ve tahrişten sonra kendini onarmak üzere tasarlanmıştır. Ancak Crohn hastalığı ve ülseratif kolit gibi kronik hastalıklarda bu onarım süreci kontrolden çıkabilir ve bağırsağı daraltan, sert ve kalınlaşmış skar dokusuna yol açabilir; bu da bazen cerrahi gerektirir. Bu çalışma, skara yol açan bağırsaktaki bağışıklık hücreleri ile yapı hücreleri arasındaki gizli iletişimi açığa çıkarıyor ve döngüyü kırabilecek potansiyel bir anahtar anahtarı — GLIS3 adlı bir geni — işaret ediyor.
İltihaplı Bağırsaklarda Gizli Bir Ağ
Neden bazı hastaların inatçı iltihap ve fibroz (skarlaşma) geliştirdiğini anlamak için araştırmacılar insan bağırsağının hücresel bir “atlasını” oluşturdular. Tek hücreli RNA dizileme ile bireysel hücrelerde hangi genlerin aktif olduğunu okuma yöntemini, gerçek doku dilimlerinde hücrelerin nerede bulunduğunu haritalayan mekansal profilleme ile birleştirdiler. Crohn hastalığı, ülseratif kolit ve kontrol örneklerinden alınan materyallerle bağırsak duvarı boyunca dört milyondan fazla hücreyi haritaladılar. Bu kalabalık içinde bir fibroblast alt grubu öne çıktı: inflamasyon ilişkili fibroblastlar (IAF’ler). Bu hücreler aktif ve kronik kolit bölgelerinde kümelenmişti ve standart anti–TNF tedavilerine dirençle ilişkilendirilen bir gen imzası taşıyordu; bu da onların tedavisi zor hastalıkta merkezi bir rol oynadığını düşündürüyor. 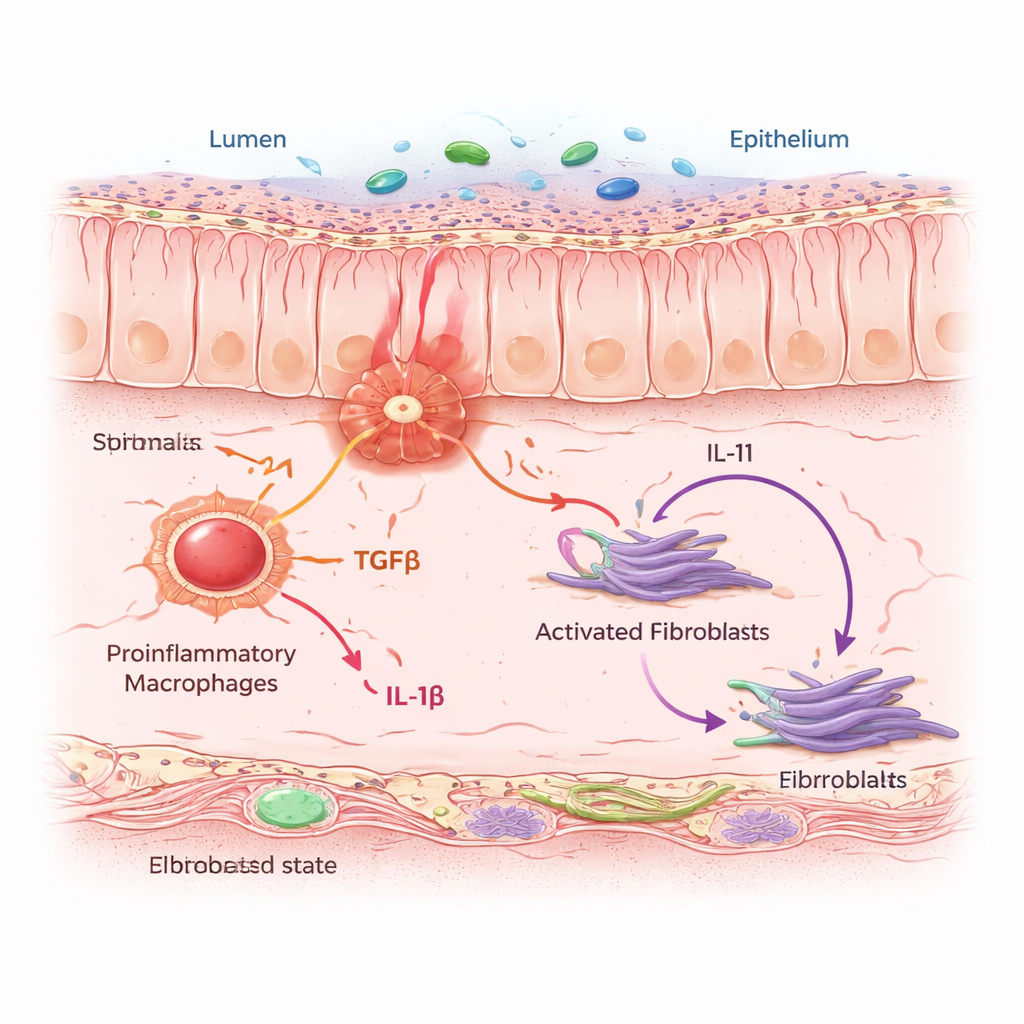
Makrofajlar Fısıldar, Fibroblastlar Skar Oluşturur
IAF’ler tek başına hareket etmiyordu. Pro-inflamatuvar makrofajlarla yoğun “mahalle”ler halinde kümeleniyorlardı—tehlikeyi algılayan ve alarm sinyalleri salan bağışıklık hücreleri. Hesaplamalı modeller ve hücre ortak kültürü deneyleri kullanılarak, makrofajlar inflamatuvar bir duruma yönlendirildiğinde iki ana haberci protein salgıladıkları gösterildi: TGFβ ve IL-1β. Yakınlardaki fibroblastlar bu sinyalleri belirli reseptörler aracılığıyla algılıyor. Her iki sinyal birlikte ulaştığında fibroblastlar IAF durumuna geçiyor ve zaten fibrozisi teşvik ettiği şüphe edilen bir sitokin olan IL-11’i, ayrıca kolajen ve bağırsak duvarını kalınlaştırıp sertleştiren diğer matriks proteinlerini üretmeye başlıyorlar. Kronik kolit rejimine maruz kalan farelerde IL-11’i engellemek veya fibroblastlarda seçici olarak silmek, ilk iltihabı engellemeden kolajen birikimini azalttı; bu da IL-11’in skarlaşma evresinin kritik bir sürücüsü olduğunu gösterdi.
GLIS3: Fibrotik Fibroblastlarda Ana Anahtar
Korelasyonlardan mekanizmalara geçmek için yazarlar güçlü genoma çapında CRISPR araçları kullandılar. IL-11 üretimi izlenebilecek şekilde floresan bir etikete sahip insan fibroblastları tasarladılar, ardından genom çapında ya genleri devre dışı bırakan ya da etkinleştiren paralel ekranlar gerçekleştirdiler. TGFβ ve IL-1β stimülasyonundan sonra Olağandışı yüksek veya düşük miktarlarda IL-11 üreten hücreleri sıralayarak bu yanıtı kontrol eden genleri tanımladılar. Birçok sinyal bileşeni arasında bir transkripsiyon faktörü—GLIS3—önde gelen bir düzenleyici olarak ortaya çıktı. GLIS3 devre dışı bırakıldığında fibroblastlar çok daha az IL-11 üretiyordu; yükseltildiğinde IL-11 artıyordu. Ek deneyler, GLIS3’ün makrofaj sinyallerine yanıt olarak fibroblast çekirdeğine girdiğini, IL11 geninin ve diğerlerinin yakınındaki DNA’ya doğrudan bağlandığını ve kolajenler ile daha fazla bağışıklık hücresini çeken faktörler dahil olmak üzere geniş bir inflamatuvar ve fibrotik gen programını aktive ettiğini gösterdi. 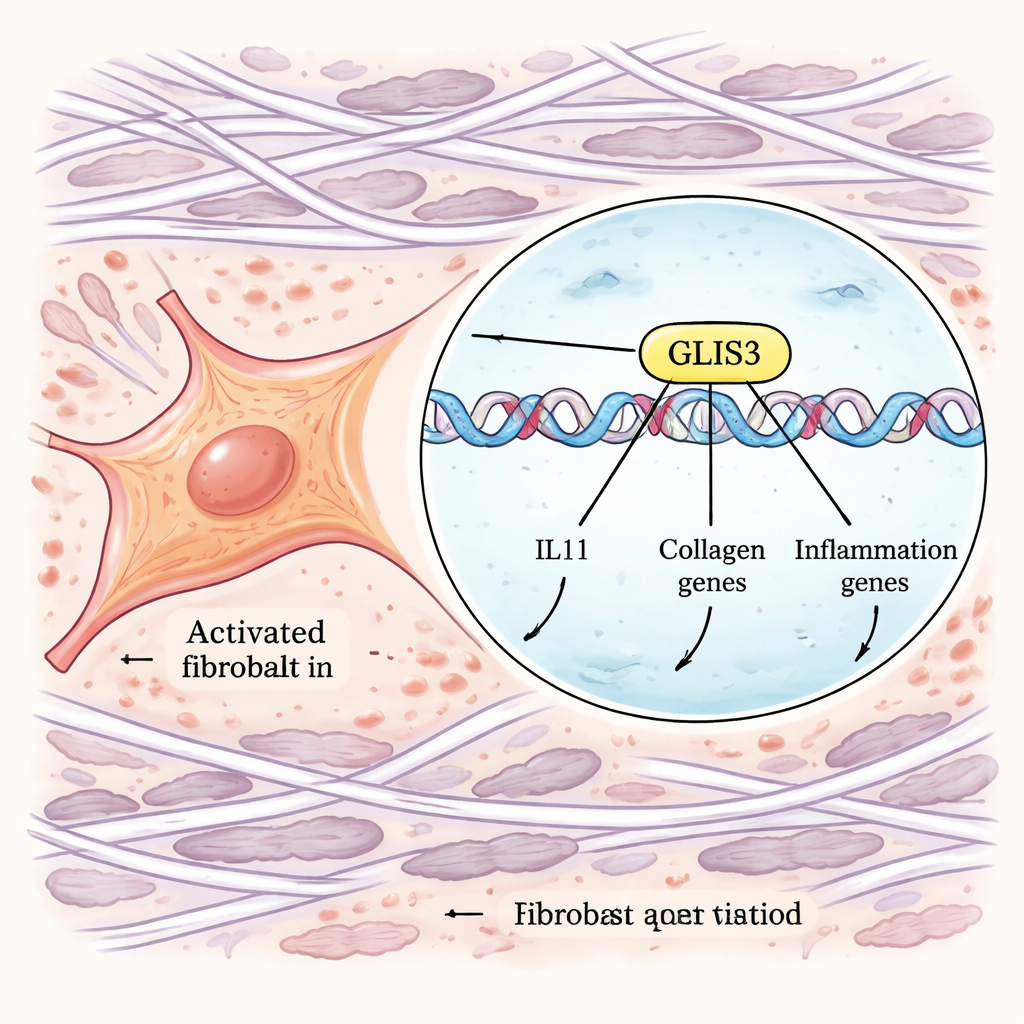
Fare Modellerinden Hasta Ciddiyetine
Araştırmacılar daha sonra bu GLIS3 kaynaklı programın canlı organizmalarda önemli olup olmadığını sordular. Farelerde GLIS3’ün yalnızca fibroblastlardan çıkarılabildiği bir soy oluşturdular. Bu hayvanlar kronik kolite maruz bırakıldığında daha az intestinal skar gelişti, daha düşük kolajen ve fibrotik gen ekspresyon düzeyleri gördüler ve normal farelere kıyasla azalmış iltihap gösterdiler. Mekansal haritalama, GLIS3 eksikliğine sahip farelerin daha az IL-11 üreten fibroblastı ve daha az yakın aktive makrofaj ve nötrofil içerdiğini doğruladı; bu da GLIS3’ü bozmanın tüm inflamatuvar-fibrotik devreyi zayıflattığını gösteriyor. Büyük bir pediatrik ülseratif kolit kohortuna döndüklerinde, yazarlar 50 genlik bir GLIS3 “imzası” belirlediler ve kolon biyopsilerindeki etkinliğinin hastalık şiddeti ile IAF’lerin ve aktive makrofajların bolluğunu yakından izlediğini buldular; bu yolun doğrudan hasta sonuçlarıyla bağlantısını kuruyor.
İltihap ve Skar Döngüsünü Kırmak
Uzman olmayanlar için sonuç şu: Bu çalışma kendini güçlendiren bir döngüyü ortaya koyuyor: inflamatuvar makrofajlar fibroblastları skar oluşturan IAF’lere dönüştürüyor; bu IAF’ler GLIS3 kontrolü altında IL-11, kolajen ve dokuyu yeniden şekillendiren ve daha fazla inflamatuvar hücre çeken diğer faktörleri salgılıyor. Bağışıklık sistemini geniş kapsamlı bastıran standart ilaçlar bu döngüyü tam olarak bozmayabilir; bu da birçok hastanın sonunda mevcut tedavilere yanıt vermemesini açıklamaya yardımcı olur. GLIS3’ü ve IL-11 üreten fibroblast durumunu inflamasyon–fibroz devresinin merkezi düğümleri olarak tanımlayarak bu çalışma, yalnızca bağışıklık hücrelerine değil fibroblastlara yönelik daha hedefli stratejilere işaret ediyor; bu stratejiler bir gün inflamatuvar bağırsak hastalığında ve muhtemelen diğer kronik inflamatuvar durumlarda skarlaşmayı önleyebilir veya tersine çevirebilir.
Atıf: Pokatayev, V., Jaiswal, A., Shih, A.R. et al. Bidirectional CRISPR screens decode a GLIS3-dependent fibrotic cell circuit. Nature 650, 997–1006 (2026). https://doi.org/10.1038/s41586-025-09907-x
Anahtar kelimeler: inflamatuvar bağırsak hastalığı, intestinal fibroz, fibroblastlar, makrofajlar, GLIS3