Clear Sky Science · tr
Stres, histon H3 ubikitinlenmesi aracılığıyla heterokromatin kalıtımını kontrol eder
Hücreler Stresi Nasıl Hatırlar
Hücrelerimiz, ısı, besin eksikliği veya ilaç maruziyeti gibi geçmiş stresleri "hatırlamanın" yollarına ihtiyaç duyar; böylece bir dahaki sefere daha hızlı yanıt verebilirler. Güçlü bir bellek sistemi, belirli genleri birçok hücre bölünmesi boyunca kapalı tutan sıkı paketlenmiş DNA olan heterokromatina dayanır. Bu makale, hücrelerin bu belleği strese yanıt olarak nasıl aktif biçimde ayarladığını araştırıyor ve çevresel sinyaller ile gen aktivitesinde kalıcı değişiklikleri birleştiren moleküler bir merkezin varlığını ortaya koyuyor. Bu kontrol sistemini anlamak, mantarların ilaç direncini nasıl geliştirdiğini ve stresin kendi hücrelerimizin epigenetik manzarasını nasıl yeniden şekillendirdiğini açıklamaya yardımcı olabilir.
Genom Üzerinde Bir Kilit
Heterokromatin, yakınındaki genleri sessiz tutan DNA bölgelerine takılmış moleküler bir kilit gibi düşünülebilir. Bu kilit, özellikle H3K9me3 adlı işaret olmak üzere histon proteinlerindeki kimyasal etiketlerden oluşur. Bir kez kurulduğunda, DNA kopyalandığında kendini kopyalayabilir ve böylece gen baskılanması kalıtsal olarak aktarılabilir; alttaki DNA dizisini değiştirmeye gerek yoktur. Şimdiye kadar çoğu çalışma, bu kendini kopyalamanın esas olarak bir "oku‑yaz" geri besleme döngüsüne dayandığını öne sürmüştü: bir enzim kompleksi mevcut H3K9me3 işaretlerini tanır ve komşu histonlara aynı işareti ekleyerek sessiz bölgeyi kademeli olarak yayar. Ancak bu model, çevresel koşulların heterokromatin yayılmasını nasıl hızlandırdığını, yavaşlattığını veya yönlendirdiğini tam olarak açıklayamıyordu.
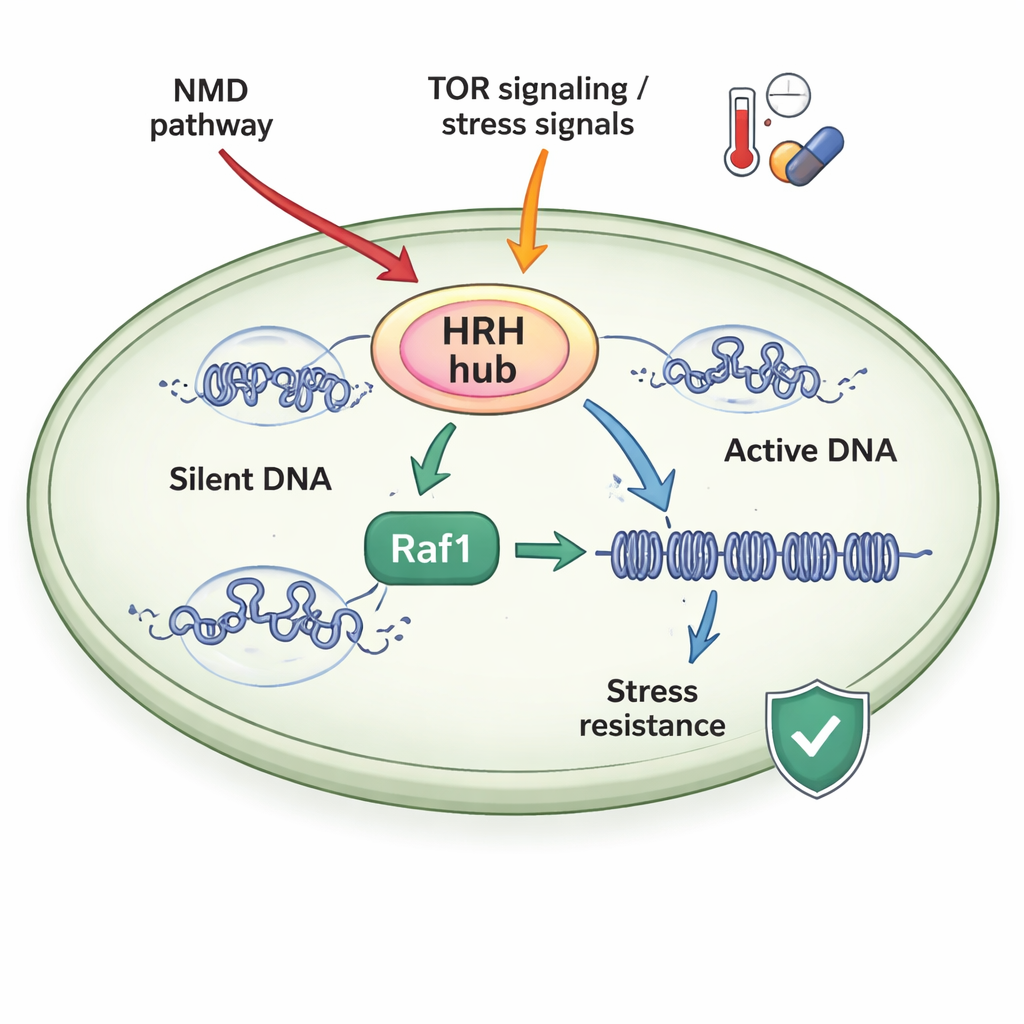
Strese Duyarlı Bir Kontrol Merkezi
Yazarlar, kromatin mekanizması daha yüksek organizmalara benzeyen basit bir model organizma olan bölünmüş maya (fission yeast) üzerinde çalıştılar. H3K9me3 işaretini yazan ve aynı zamanda histon H3'ün başka bir pozisyonuna (H3K14ub) küçük bir protein olan ubikitini ekleyen ClrC adlı bir komplekse odaklandılar. ClrC’nin ana alt birimlerinden biri olan Raf1, sınırlayıcı bir “kapı bekçisi” gibi davranır: Raf1 kıt olduğunda, ana enzim (Clr4) kompleks içinde kromatinle birleşmek yerine büyük ölçüde serbest halde yüzebilir ve sessiz domainler yayılmaz. Raf1 bol olduğunda ise daha fazla ClrC bir araya gelir ve DNA'ya kararlı şekilde bağlanır; bu da H3K14ub ve H3K9me3 işaretlerinin kromozom boyunca uzanmasına ve gen susturmasını güçlendirmesine izin verir.
Ubikitin ile Kilidi İnce Ayarlamak
Genom boyunca kromatin işaretlerini eşleyerek ekip, H3K14ub’nin heterokromatin oluşan her yerde güçlü biçimde zenginleştiğini ve Raf1 kaldırıldığında bu işaretin neredeyse yok olduğunu gösterdi. Hücrelerde ubikitin ekleme adımını engelleyen bir mutasyon bulunduğunda (başlangıç noktasında H3K9me3 korunurken), sessiz domainler dışa doğru yayılamıyor. Başka bir deyişle, H3K14ub sadece süs değil; heterokromatin ön saflarını ileri itmek için gereklidir. Biyokimyasal ve görüntüleme deneyleri bunun nedenini ortaya koyuyor: H3K14ub, Clr4 enziminin aktivitesini büyük ölçüde artırır ve tüm kompleksin kromatina bağlı kalmasına yardımcı olur; bu da yerel H3K9me3 yoğunluğunu kararlı kalıtım için gereken eşik üzerine çıkarır. Dikkate değer biçimde, Raf1 düzeylerinin artırılması, normalde bu sessiz domainleri sürdürmek için gerekli olan diğer birkaç faktörün yokluğunu telafi edebilir; bu da Raf1 kaynaklı ubikitinasyonun merkezi bir kontrol kolu olduğunu vurgular.
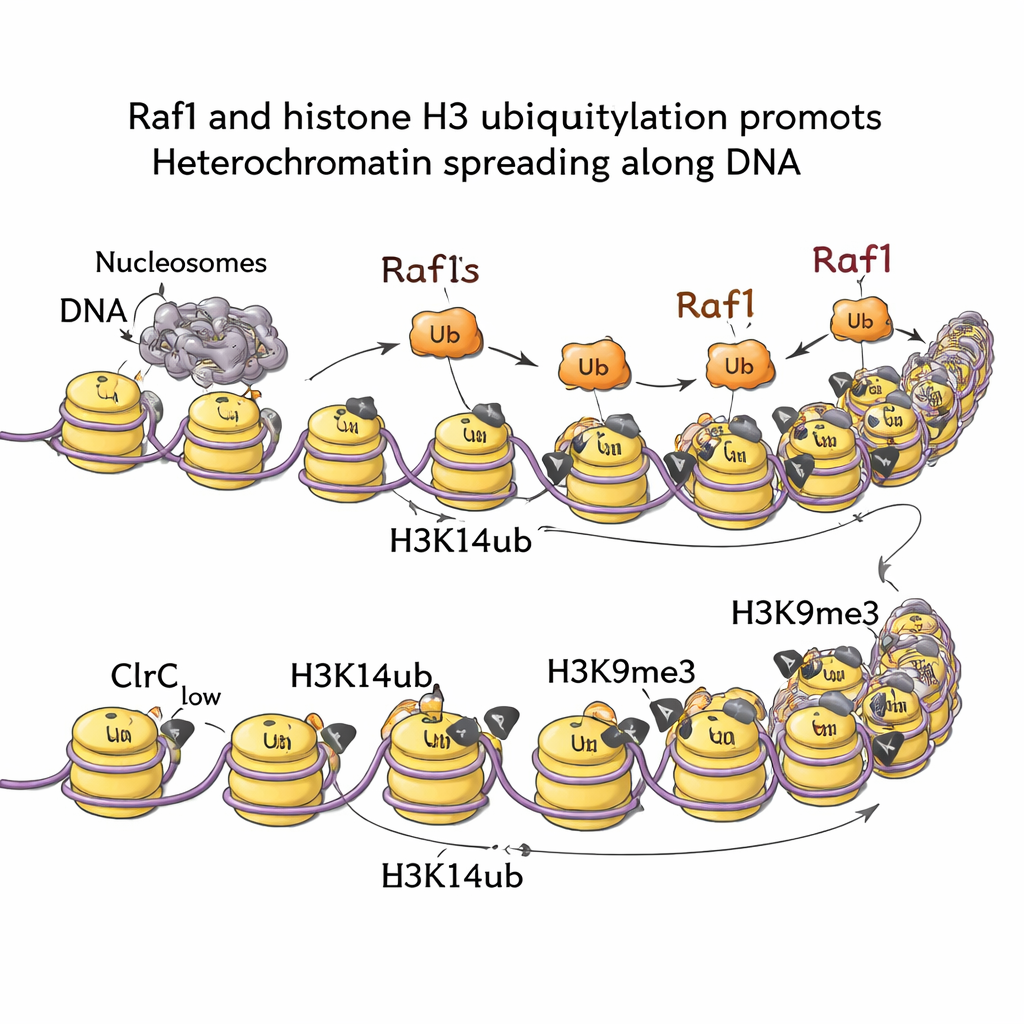
RNA Bozunması ve Büyüme Yollarından Gelen Sinyaller
Hücreler Raf1 düzeylerini şansa bırakmaz. Çalışma, iki büyük stres‑yanıtlı sistemin yazarların Raf1 merkezli heterokromatin kalıtılabilirlik düzenleme merkezi (HRH) olarak adlandırdığı merkeze bilgi aktardığını gösteriyor. Birincisi, hatalı haberci RNA’ları yok etmesiyle bilinen anlamsız‑arasal bozunma (nonsense‑mediated decay, NMD) yolu, Raf1’i kodlayan haberciyi hedefleyerek normal koşullarda Raf1 düzeylerini düşük tutar. NMD devre dışı bırakıldığında Raf1 RNA’sı stabil hale gelir, Raf1 protein bolluğu artar ve aksi halde sessiz domainleri sürdüremeyen mutantlarda heterokromatin yayılması geri gelir. İkincisi, Gad8 kinazı aracılığıyla hareket eden TORC2 adlı bir büyüme ve stres sensörü, Raf1 ifadesini destekler. Yüksek sıcaklık bu yolu kapatır, Raf1 düzeylerini düşürür, heterokromatini zayıflatır ve Raf1 deneysel olarak artırılmadıkça hücrelerin sessiz durumları sürdürmesini zorlaştırır.
Stres, İlaç Direnci ve Daha Geniş Çıkarımlar
Yazarlar ardından bu moleküler merkezi gerçek dünyadaki adaptasyonla ilişkilendiriyor. Mayayı kafeine maruz bırakmak—başka sistemlerde NMD’yi zayıflattığı bilinen bir stres—Raf1 düzeylerini yükseltir ve heterokromatinin yeni bölgelere yayılmasını güçlendirir; bu bölgeler arasında susturulması kafein ve antifungal ilaçlara direnç sağlayan genler de bulunur. Benzer şekilde, yapay olarak yükseltilmiş Raf1’e sahip hücreler, yaygın antifungal ajanlar olan flukonazol ve klotrimazole’a karşı daha dirençli hale gelir. Tersine, Raf1 ısı veya TORC2–Gad8 sinyalinin kaybıyla azaltıldığında, heterokromatin kararsızlaşır ve epigenetik bellek silinir; Raf1 geri gelmedikçe bu durum düzelmez. Raf1 benzeri proteinlerin, ClrC kompleksinin ve H3K14ub işaretinin patojenik mantarlarda ve memelilerde karşılıklarının bulunması, benzer bir stres algılayan epigenetik merkezin birçok türde ilaç direncini, gelişimi ve hastalığı şekillendirebileceğini düşündürür.
Bu Neden Önemli
Günlük terimlerle, bu çalışma kromatin yoluyla gen susturmasının katı bir kilit değil, akıllı ve ayarlanabilir bir sistem olduğunu gösteriyor. Hücreler, çevresel ipuçlarını—sıcaklık değişimleri, besin durumu, kimyasal stresler—okumak ve Raf1’i yukarı veya aşağı ayarlamak için merkezi bir hub kullanır. Bu da, genomun ne kadarının uzun süreli sessizlikle sarıldığına ve hücrelerin DNA’sını mutasyonlamadan kendilerini ne kadar kolay "yeniden programlayabildiğine" karar verir. Histon H3 ubikitinlenmesi ve Raf1 dozunun bu süreçteki kilit rolünü ortaya koyarak, çalışma stresin epigenetik manzarayı hızlıca nasıl yeniden şekillendirebileceğine dair bir kroki sunuyor—ve mantarlardaki ilaç direncini veya insan hastalığındaki anormal gen susturmayı etkilemenin yeni yollarına işaret ediyor.
Atıf: Bhatt, B., Wei, Y., Pradhan, A.K. et al. Stress controls heterochromatin inheritance via histone H3 ubiquitylation. Nature 650, 768–778 (2026). https://doi.org/10.1038/s41586-025-09899-8
Anahtar kelimeler: heterokromatin, epigenetik kalıtım, histon ubikitinasyonu, stres adaptasyonu, mantar ilaç direnci