Clear Sky Science · tr
Modifiye tümör hücrelerinden tasarlanmış biomimetik veziküller, ameliyat sonrası kanser immünoterapisi için kişiye özel aşı görevi görür
Tümör Artıkları İkinci Savunma Hattına Dönüştürülüyor
Katı tümörleri olan birçok kişi için cerrahi, uzun bir mücadelenin yalnızca ilk etabıdır. Tümörün çoğu çıkarılsa bile, küçük kanser hücresi kümeleri kaçabilir ve daha sonra ölümcül metastazlara yol açabilir. Bu çalışma, hastanın kendi tümör hücrelerini ameliyat sonrası kalanları avlamak ve bağışıklık sisteminin kanserin geri dönmesini engellemesine yardımcı olmak üzere tasarlanmış kişiye özel bir aşıya dönüştürmenin yaratıcı bir yolunu araştırıyor.
Ameliyat Sonrası Kalan Kanser Hücrelerini Silmenin Zorluğu
Standart tedaviler, cerrahın ana tümör kitlesini çıkardıktan sonra geride kalan hücrelerle başa çıkmakta zorlanır. Bu dağınık hücreler genellikle uzak organlarda saklanır ve ilaçlardan ile bağışıklık saldırılarından korunur. Mevcut immün tabanlı aşılar vücudu tümör belirteçlerini tanımaya eğitmeye çalışır; bunun için dendritik hücreler adı verilen özel bağışıklık hücreleri kullanılır, ancak bu canlı aşılar üretim açısından zordur, önemli bağışıklık organlarına verimli şekilde ulaşmazlar ve klinikte sınırlı fayda göstermiştir. Temel zorluk, her hastanın kanserinin benzersiz bir mutasyon karışımı taşımasıdır; bu yüzden tek tip aşılar genellikle önemli hedefleri kaçırır.
Kanser Hücrelerini Daha Tanınır Kılan Gizli Bir Anahtar
Araştırmacılar, hücrelerin içerdiklerini bağışıklık nöbetçilerine daha iyi gösterir hale getiren doğal anahtarları aramakla başladı. Normalde bağışıklık hücrelerinde bol bulunan ancak birçok tümörde az olan syntaxin 11 adlı bir proteine odaklandılar. Bu proteini fare modellerinden alınan agresif meme kanseri hücrelerinde artırarak, kanser hücrelerinin profesyonel immün nöbetçilere daha çok benzediğini gözlemlediler: bu hücreler yüzeylerinde daha yüksek düzeyde moleküler “isim etiketi” ve yardımcı sinyaller sergiledi. Etkilenilen tümör hücreleri, özelliklerini gizlemek yerine benzersiz özelliklerini bağışıklık sistemine daha fazla ortaya koyacak şekilde yeniden programlandı.
Küçük Taklit İmmün Haberci Baloncukları İnşa Etmek
Yeniden programlanmış bu tümör hücreleriyle ekip, hücrelerin dış zarlarını soydu ve biyobozunur nanopartikülleri, küçük bir immün uyarıcı ilaçla yüklü şekilde kaplamak için bu zarları kullandı. Ortaya, her biri o tümörün tüm belirteç koleksiyonunu ve öldürücü T hücreleri için yerleşik “git” sinyallerini taşıyan nanoskalalı kabarcıklar sürüsü çıktı. Ameliyat sonrası farelerin derisi altına enjekte edildiğinde bu veziküller yakındaki lenf düğümlerine etkin biçimde giderek bağışıklık hücrelerinin eğitildiği yerde toplandılar. Orada doğrudan öldürücü T hücreleriyle etkileşebiliyor ve doğal immün nöbetçiler tarafından yutularak tepkileri daha da güçlendiriyorlardı. Deneyler, bu veziküllere maruz kalan T hücrelerinin daha hızlı çoğaldığını ve daha basit nanoparçacık tasarımlarıyla uyarılanlara kıyasla kanser hücrelerini yok etmede daha başarılı olduğunu gösterdi.
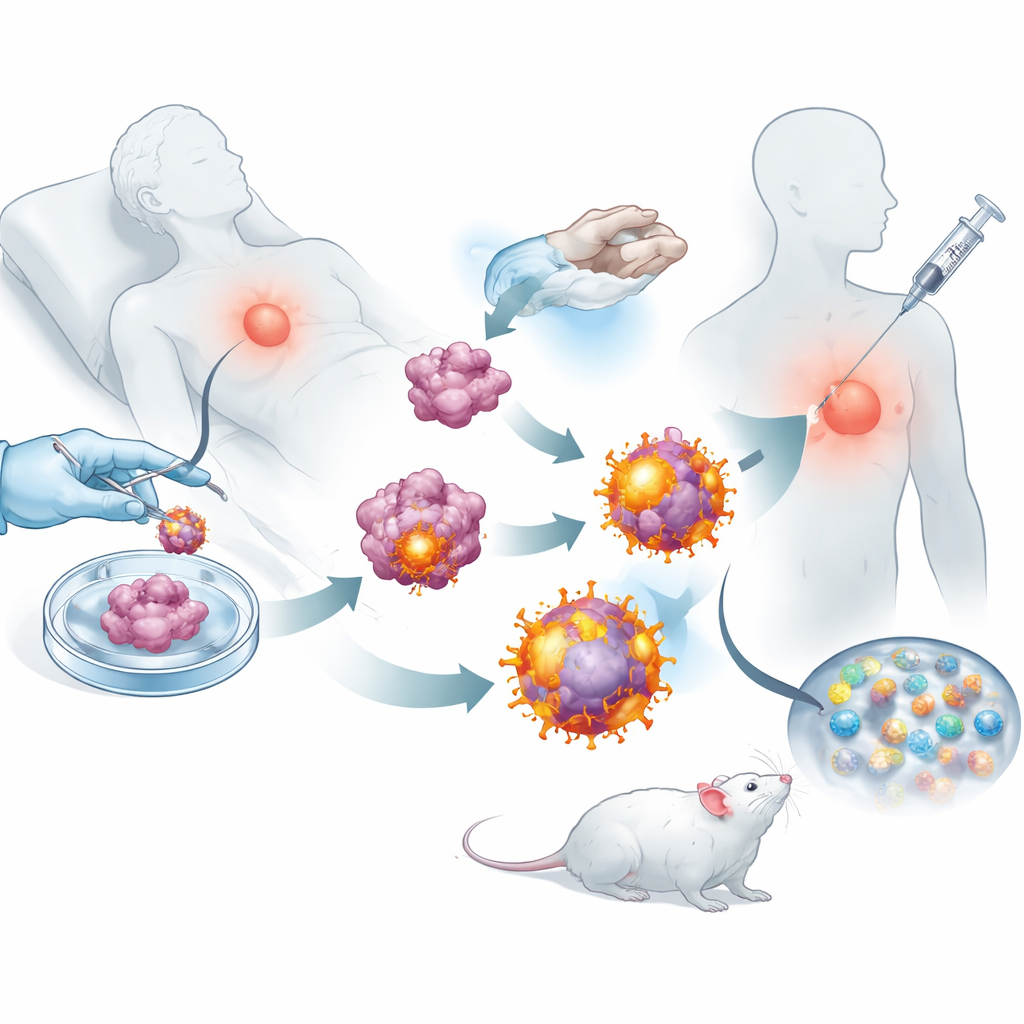
Ameliyat Sonrası Kanseri Uzak Tutmak
Araştırmacılar, bu özelleştirilmiş aşının hastalığın seyrini gerçekten değiştirip değiştiremeyeceğini görmek için birkaç meme kanseri ve melanom fare modeli kullandılar. Meme tümörünün çoğu cerrahiyle çıkarılan hayvanlarda, aşılanan farelerde nükslerin daha küçük olduğu ve akciğer metastazlarının kontrolsüz hayvanlara göre çok daha az görüldüğü bulundu. Tedavi edilen farelerin lenf düğümleri, dalağı ve tümörleri aktif öldürücü T hücreleri ve uzun ömürlü bellek hücreleriyle doluydu; bu, bağışıklık sisteminin hem uyarıldığını hem de uzun vadeli eğitim aldığını gösteriyordu. T hücrelerini felçleştirmeyi engelleyen onaylı bir immün kontrol noktası engelleyici antikorla birleştirildiğinde aşı, kalıcı tümör kontrolü sağladı ve birçok farede tam gerileme ile uzun süreli sağkalım elde edildi.
Kişiye Özel Bir Tedaviyi Hızlandırmak
Bu kavramı gerçek dünyada bir tedaviye dönüştürmenin önündeki engellerden biri zamandır: tümör hücrelerini yeniden programlamak için gen tabanlı yöntemler yavaş olabilir. Buna çözüm olarak ekip, doğal bileşikleri taradı ve anahtar protein düzeylerini ve aynı immün uyarıcı yüzey belirteçlerini hızla yükselten deoksipodofilotoksin adlı küçük bir molekül keşfetti. Bu kestirme yolu kullanarak, benzer vezikül kaplı nanoparçacıkları daha kısa sürede ürettiler ve güçlü, tümöre özgü immün yanıtları uyandırma yeteneğini korudular. Testler, bu ilaçla yapılan aşıların gen tabanlı yöntemle üretilenler kadar etkili olduğunu ve faydalarının genel bir kanser zehirlenmesine değil doğru tümör tipinin tanınmasına dayandığını gösterdi.
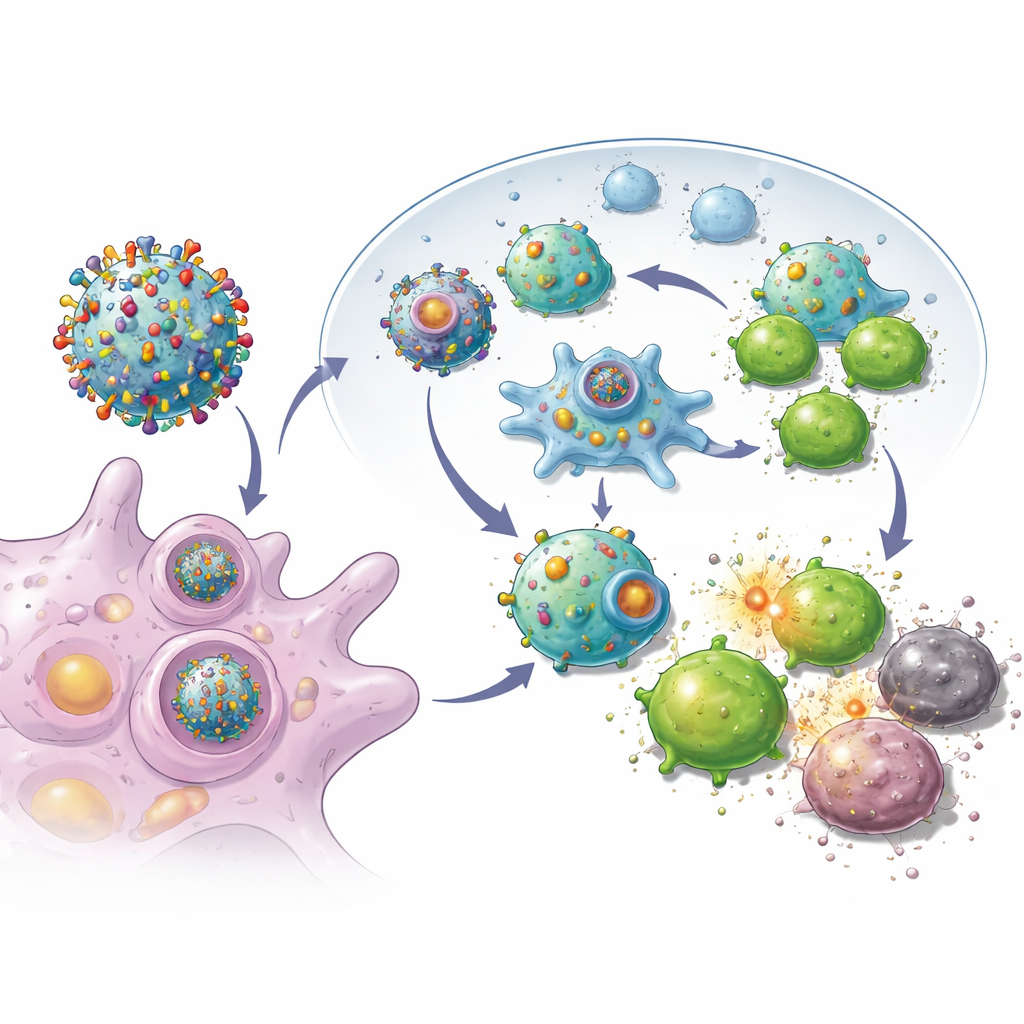
Geleceğin Kanser Bakımı İçin Ne Anlama Gelebilir
Uzman olmayan bir okuyucu için çıkarılması gereken mesaj şudur: bir hastanın kendi tümörü, bağışıklık sistemi için minyatür bir eğitim aracına dönüştürülebilir. Kanser hücrelerini zengin, kişiselleştirilmiş bilgi kaynaklarına çevirip bu bilgileri dayanıklı nanoskala taşıyıcılar üzerine paketleyerek bu yaklaşım, cerrahinin geride bıraktığı hücreleri toplama ve yeni büyümelerin yerleşmesini önleme amacını güder. Böyle aşıların insanlara rutin olarak sunulabilmesi için güvenlik ve etkinliğin insan tümörlerinde kanıtlanması ve güvenilir üretim hatlarının kurulması gibi birçok adım gerekmekte olsa da, bu çalışma cerrahın başladığını bağışıklığın bitirmesine yardım eden yüksek düzeyde bireyselleştirilmiş ameliyat sonrası tedavilere giden bir yolu tasvir ediyor.
Atıf: Yu, P., Jin, Z., Meng, L. et al. Biomimetic vesicles engineered from modified tumour cells act as personalized vaccines for post-surgical cancer immunotherapy. Nat. Nanotechnol. 21, 443–454 (2026). https://doi.org/10.1038/s41565-025-02113-w
Anahtar kelimeler: kanser aşısı, immünoterapi, nanomedisin, operasyon sonrası tedavi, kişiselleştirilmiş onkoloji