Clear Sky Science · tr
Canlı organizmada DNA origami yapısal bütünlüğünün ve farmakokinetiğinin çözülmesi
Vücudun İçinde Küçük DNA Makinelerini İzlemek
DNA, kağıt gibi katlanarak mikroskobik üç boyutlu şekillere dönüştürülebilir; bu tekniğe DNA origami denir. Bu nanoyapılar, ilaçları, aşıları veya sinyal moleküllerini olağanüstü bir hassasiyetle taşımak üzere programlanabilir. Ancak vücuda enjekte edildiklerinde, işlerini yapacak kadar uzun süre bütün halde kalıyorlar mı, yoksa hızla parçalanıyorlar mı? Bu makale, bu DNA makinelerini canlı hayvanların içinde izlemeye yarayan yeni bir yaklaşımı tanıtıyor; ne kadar süre hayatta kaldıklarını, kan dolaşımı içinde nasıl yol aldıklarını ve hatta her yapının hangi parçalarının önce bozulduğunu ortaya koyuyor.
DNA’yı Katlamanın Tıbbı Neden Değiştirebileceği
DNA origami, genetik bilgimizi depolayan aynı baz eşleşmesi kurallarından yararlanır, ancak bunları nanoskopik nesneler inşa etmek için yeniden amaçlar. Araştırmacılar, bu nesneler üzerine proteinleri, ilaçları veya bağışıklık uyaran sinyalleri Lego plakası üzerindeki çıkıntılar gibi düzenleyebilir; kanser, otoimmün hastalıklar ve enfeksiyonlar için yüksek kontrollü tedaviler oluşturabilirler. Bu kadar hassas tedavilerin güvenli ve etkili olabilmesi için, düzenleyiciler ve bilim insanları bu yapıların vücutta ne ölçüde bütün kaldığını ve ne kadar hızlı temizlendiklerini —birlikte farmakokinetikleri olarak bilinen— bilmeli. Mevcut izleme yöntemleri genellikle floresan boyalar bağlamak ya da DNA parçalarını saymak gibi yaklaşımlar kullanır; bu da dağılmış kalıntıların tamamen sağlam nanoyapılarmış gibi görünmesine neden olabilir. Bugüne kadar, canlı hayvanlarda, orijinal DNA origami şekillerinin kendilerinin hâlâ bütün olup olmadığını pratik olarak ayırt etmenin bir yolu yoktu.
DNA Origami İçin Moleküler Bir “Bütünlük Testi”
Araştırma ekibi, PLASTIQ adını verdikleri bir yöntemi geliştirdi; açılımı structural tracking and integrity quantification için proximity ligation assay (yapısal izleme ve bütünlük nicelleştirmesi için yakınlık ligasyonu testi). Temel fikir, DNA origaminin kendi durumunu raporlamasına izin vermektir. Her yapıda belirli pozisyonlara, origami doğru şekilde katlandığında bir heliks boyunca omuz omuza duran kısa DNA staplları çiftleri yerleştirirler. Her çiftin bir üyesi, sadece sağlam bir iskele zinciri tarafından hâlâ yakın tutuluyorlarsa enzimatik olarak birleştirilmelerine (ligasyon) izin veren küçük bir kimyasal etiket taşır. Yapı erirse, koparsa veya enzimlerce parçalanırsa, bu iki parça ayrılır ve artık ligasyon gerçekleştirilemez. Ligation sonrası, birleştirilen çiftler standart polimeraz zincir reaksiyonu ile çoğaltılır ve hassas qPCR veya dizileme ile nicelenir; böylece kanın sadece birkaç mikrolitresinden alınan ölçülebilir sinyallere çevrilerek yerel sağlam segmentlerin varlığı bildirilir.
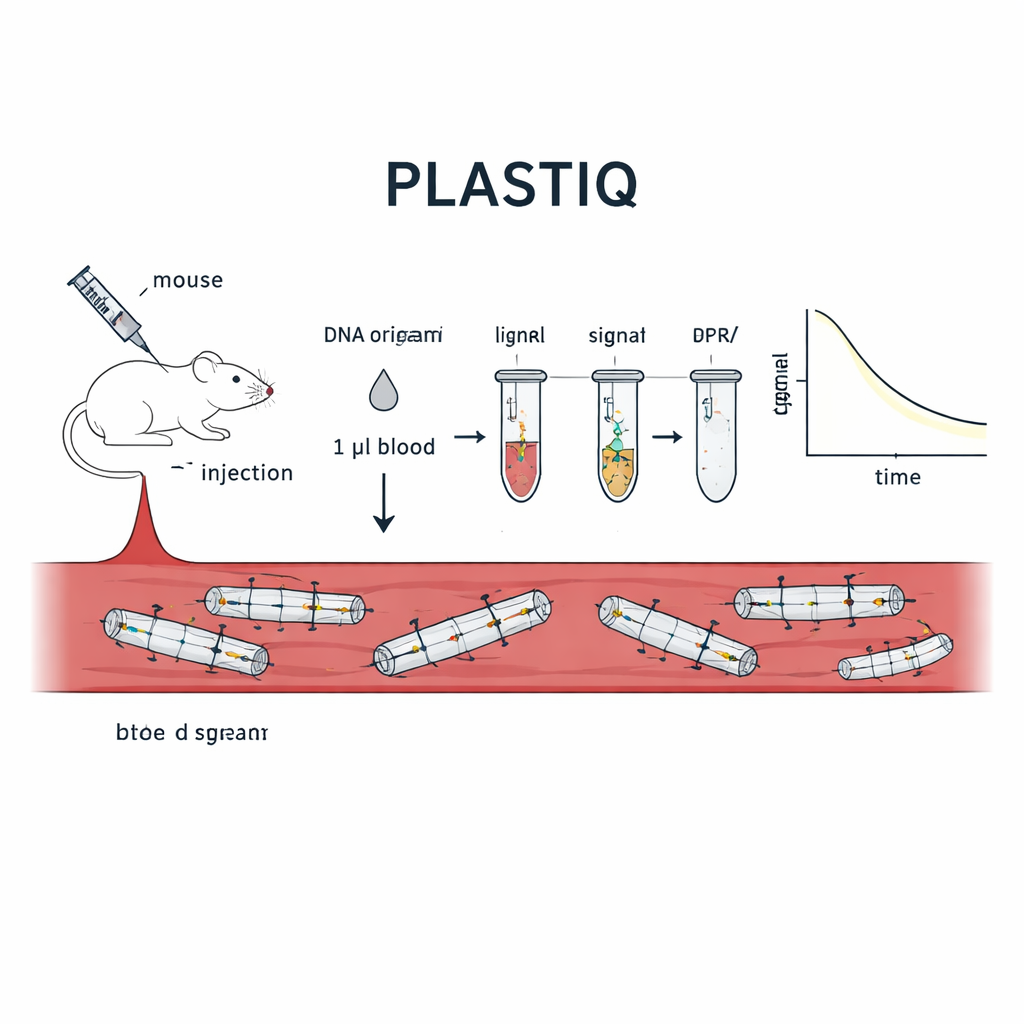
Testi Canlı Farelerde Uygulamak
PLASTIQ’in gerçekten yapısal bütünlüğü ölçtüğünü kanıtlamak için, yazarlar önce bunu basit çubuk şeklindeki DNA origami tasarımlarına tüp deneylerinde uyguladılar. Sinyaller yalnızca çubuklar sağlam olduğunda ortaya çıktı ve ısıyla açılma sonrası kayboldu; geleneksel DNA tabanlı testler ise şekilden bağımsız olarak hâlâ DNA kaydetmeye devam etti. Ardından bu çubukları farelere farklı yollarla enjekte ettiler—doğrudan kan dolaşımına, karın boşluğuna, kas içine ve deri altına—ve farklı zamanlarda sadece bir mikrolitre kan aldılar. PLASTIQ, sağlam yapıların konsantrasyonunun enjekte etme yoluna bağlı olarak nasıl yükselip düştüğünü ortaya koydu; bu, ilaç farmakolojisinden beklenen genel eğilimlerle uyumluydu fakat çok daha ayrıntılı yapısal bilgi sağladı. Yöntem 0.01 femtomolar düzeyine kadar hassasiyet gösterdi, yine de çok az kan gerektirdiği için aynı hayvandan saatler içinde tekrarlı örnekleme yapılmasına izin verdi.
Koruyucu Kaplamaları ve Gizli Zayıf Noktaları Test Etmek
Birçok grup DNA origamiyi PEG gibi polimerlerle kaplayarak, zincirleri ultraviyole ışıkla çapraz bağlayarak veya kimyasal bağlayıcılar ekleyerek korumaya çalışır; ancak bu hilelerin vivo ortamda ne kadar işe yaradığını görmek zordu. PLASTIQ’i kullanarak, yazarlar PEG kaplı çubukların kan dolaşımında çıplak olanlara göre biraz daha uzun süre sağlam kaldığını ancak dolaşıma ulaştıklarında daha hızlı temizlendiklerini ve kaplamanın PLASTIQ enzimlerinin işini yapmasını engellemediğini gösterdiler. PLASTIQ’i basit matematiksel modellerle birleştirerek, farklı enjekte etme yolları ve kaplamalar için absorbsiyon ve eliminasyon hızlarını çıkardılar ve hatta tekrarlanan doz rejimlerini simüle edebildiler. Yöntemi bir adım daha ileri taşıyarak içi dışına göre daha sık paketlenmiş çift katmanlı namlu şeklinde bir origami kullandılar. PLASTIQ ölçümleri, açığa maruz kalan dış yüzeydeki staplların iç boşluğa bakanlara göre bütünlüğünü daha hızlı kaybettiğini gösterdi; bu da gömülü helikslerin kanda bozunma enzimlerinden korunduğunu doğrudan doğruladı.
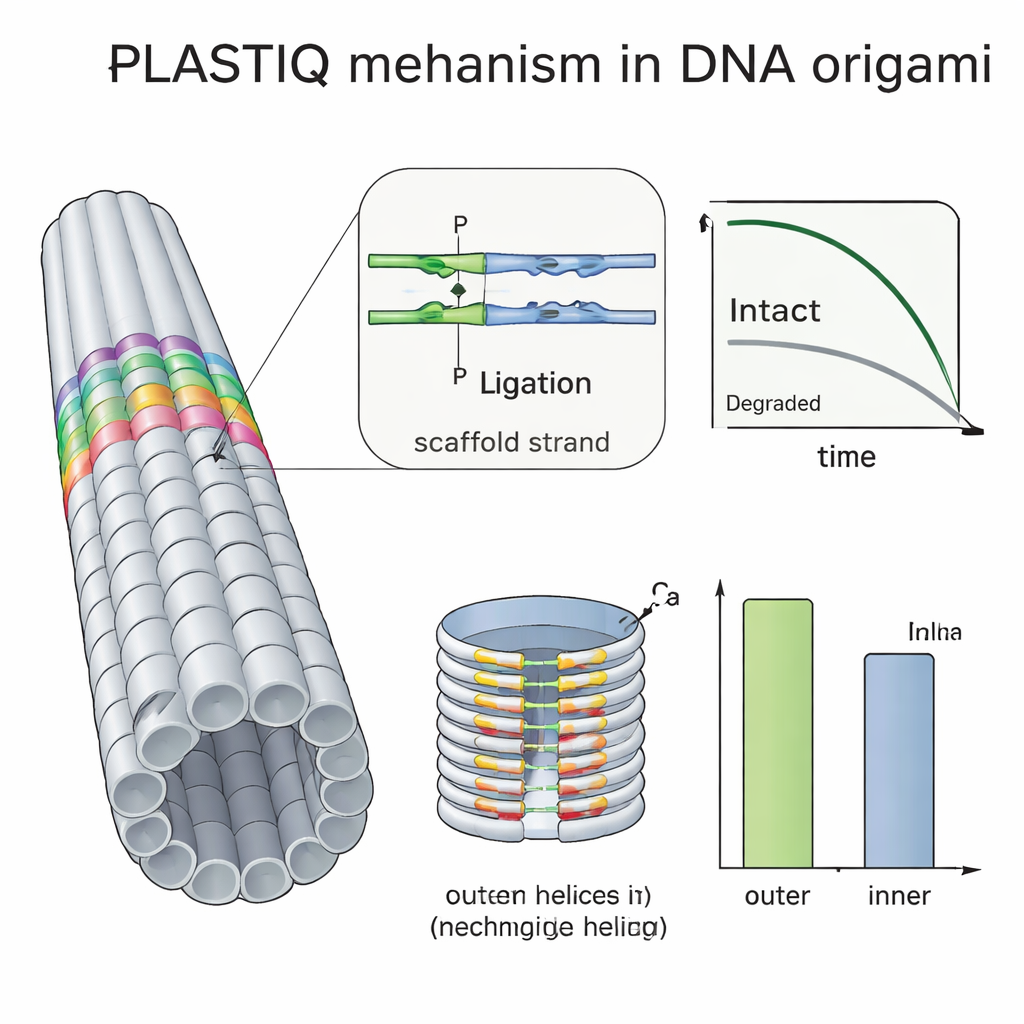
Bu, DNA Tabanlı Gelecek Terapiler İçin Ne Anlama Geliyor
Bir uzman olmayan için PLASTIQ, vücut içinde dolaşan nanoskopik DNA cihazları için yapılan yapısal bir kontrol muayenesi olarak görülebilir. Sadece “burada DNA var mı?” diye sormak yerine “bu DNA hâlâ tasarladığımız hassas nesne şeklinde katlanmış mı?” sorusunu sorar. Bu soruya küçük kan örneklerinden yüksek hassasiyetle yanıt vererek, PLASTIQ ilaç geliştiricilerine DNA origami tabanlı ilaçların ve aşıların tasarımını, kaplamasını ve dozlamasını optimize etme yolu sağlar. Zamanla, bu tip detaylı ve nicel içgörüler, bu nanoyapıların gerçek biyolojik ortamlarda nasıl davrandığına dair bilgi biriktikçe, DNA origamiyi laboratuvardaki zarif bir konudan güvenilir, düzenleyiciye hazır terapilere dönüştürmeye yardımcı olabilir.
Atıf: Wang, Y., Rocamonde-Lago, I., Waldvogel, J. et al. Resolving DNA origami structural integrity and pharmacokinetics in vivo. Nat. Nanotechnol. 21, 268–276 (2026). https://doi.org/10.1038/s41565-025-02091-z
Anahtar kelimeler: DNA origami, nanomedisin, ilaç taşıma, farmakokinetik, nanoteknoloji