Clear Sky Science · tr
Antiretroviral tedavi kesildikten sonra rhesus maymunlarında SIV yeniden alevlenmesinin başlangıç bölgeleri
Neden Virüs Geri Gelir
Günümüzün HIV ilaçları, kandaki virüsü standart testlerin görmediği düzeylere kadar düşürebiliyor. Yine de tedavi durduğunda virüs neredeyse her zaman geri dönüyor. SIV adını taşıyan, HIV’e yakın bir virüsle enfekte edilmiş rhesus makaklarında yapılan bu çalışma, temel ama kritik bir soruyu soruyor: bu viral geri dönüşün ilk kıvılcımı vücudun içinde tam olarak nerede ortaya çıkıyor ve hangi doku türleri bunu alevlendiriyor?
Viral Barkodları İzlemek
Virüsü olağanüstü bir hassasiyetle izlemek için araştırmacılar, her virüs parçacığının benzersiz bir genetik “barkoda” — kısa, zararsız bir dizi ve adeta seri numarası gibi işleyen — taşıdığı özel bir SIV kullandılar. Yirmi dört makak, bu barkodlu virüslerin binlerce karışımı ile enfekte edildi ve ardından hızla güçlü üçlü bir antiretroviral rejime başlandı. İlaçlar kandaki virüsü pratikte saptanamaz düzeye çekti ve bir yılı aşkın süre boyunca orada tuttu; bu, insanlardaki etkili uzun süreli HIV tedavisini taklit ediyordu. Her barkod ayrı bir viral aileyi işaretlediği için ekip, tedavi kesildiğinde hangi özgül viral soyların uyandığını ve uyanmanın vücutta ilk olarak nerede yerleştiğini daha sonra belirleyebildi.
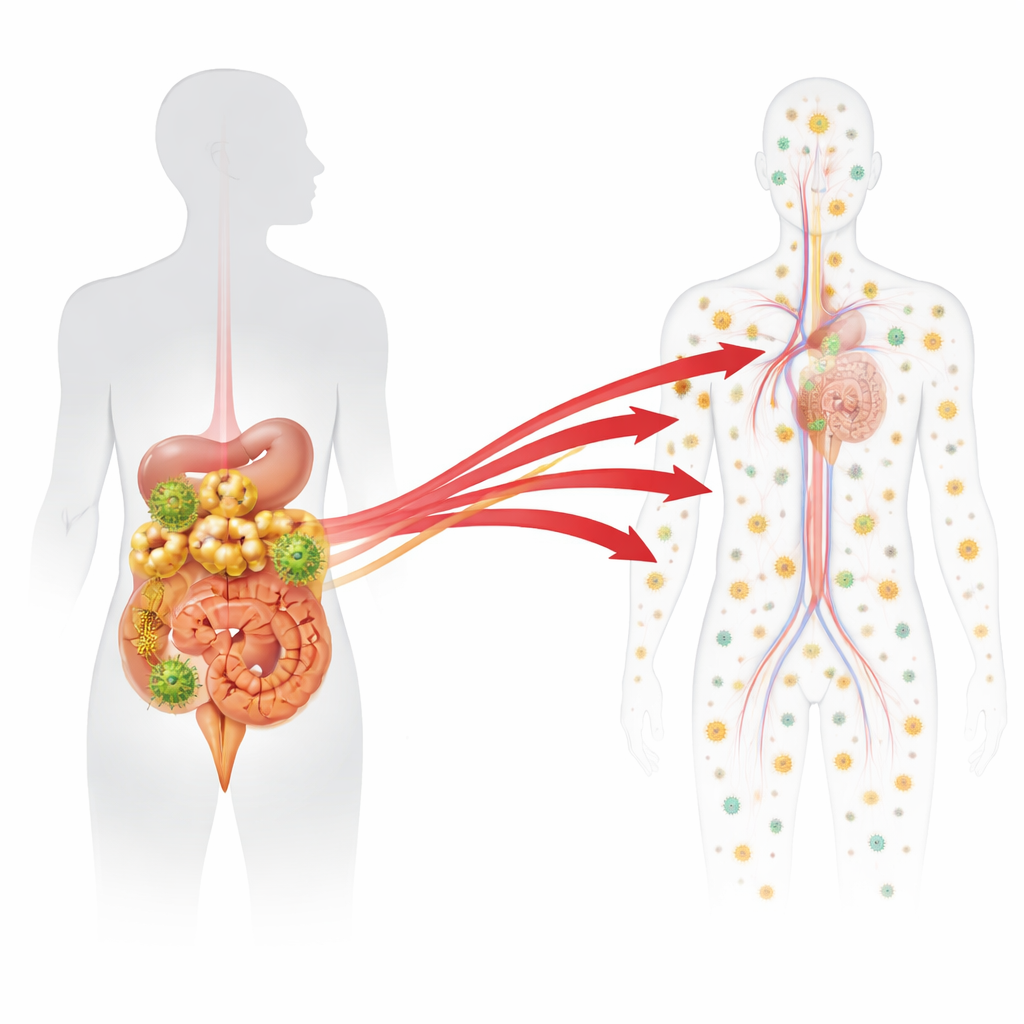
Tedavi Sırasında ve Sonrasında Dokulara Bakmak
Uzun tedavi döneminin sonunda makaklar gruplara ayrıldı. Bazıları, ilaç tedavisi devam ederken, ilaçlara rağmen düşük düzeyde kalmaya devam eden viral genetik materyalin normal arka plan paterni tanımlansın diye incelendi. Diğerlerinin tedavisi durduruldu ve ya virüs kan dolaşımında yeniden görünmeden hemen önce ya da göründüğü anda, beş veya yedi gün sonra değerlendirildi. Her hayvandan, bağırsak, çeşitli lenf düğümleri, kemik iliği gibi kan yapan organlar ve karaciğer ve akciğer gibi bağışıklık dışı organlar da dahil olmak üzere yaklaşık 90 doku örneği toplandı ve analiz edildi. Her doku için, her barkodun ne kadar viral DNA (enfekte hücrelerin göstergesi) ve viral RNA (aktif virüs üretiminin göstergesi) içerdiği ölçüldü. Ardından istatistiksel modeller kullanılarak, belirli bir dokudaki RNA düzeyi, tedavi altındayken görülen düşük düzeyli arka plan aktiviteden çok daha yüksek olan herhangi bir barkod işaretlendi.
Yeniden Alevlenmenin İlk Kıvılcımlarını Belirlemek
Araştırmacıların “aykırı” olarak adlandırdığı bu sıra dışı aktif barkodlar, ilaç çekildikten sonra taze çoğalma patlamaları ve yerel yayılma geçiren viral soyları öne çıkardı. Tüm hayvanlar içinde 32 böyle aykırı barkod tespit ettiler. Kritik olarak, virüs kan dolaşımında yeniden belirdiğinde, plazmada bulunan barkodların yaklaşık yarısı dokulardaki bu aykırılarla eşleşiyordu; bu da belirli doku bölgelerini sistemik yeniden alevlenmenin en erken aşamasıyla doğrudan ilişkilendiriyordu. Çoğu aykırı yalnızca tek bir doku örneğinde ortaya çıktı, bu da çok yerel bir başlangıç noktasına işaret ederken, daha küçük bir kesim komşu bağırsak segmentlerine ve bunların drenaj yapan lenf düğümlerine yayılmıştı. Kanda açıkça daha yüksek virüs düzeyleri görülen tek bir hayvanda ekip, uzaktaki dokular da dahil olmak üzere birden çok dokunun yeniden tohumlandığına dair kanıt gördü. Bu, kademeli bir ilerlemeyi düşündürüyor: önce tek bir yerde sessiz bir tutuşma, sonra yerel genişleme, ardından vücut geneline yayılma.
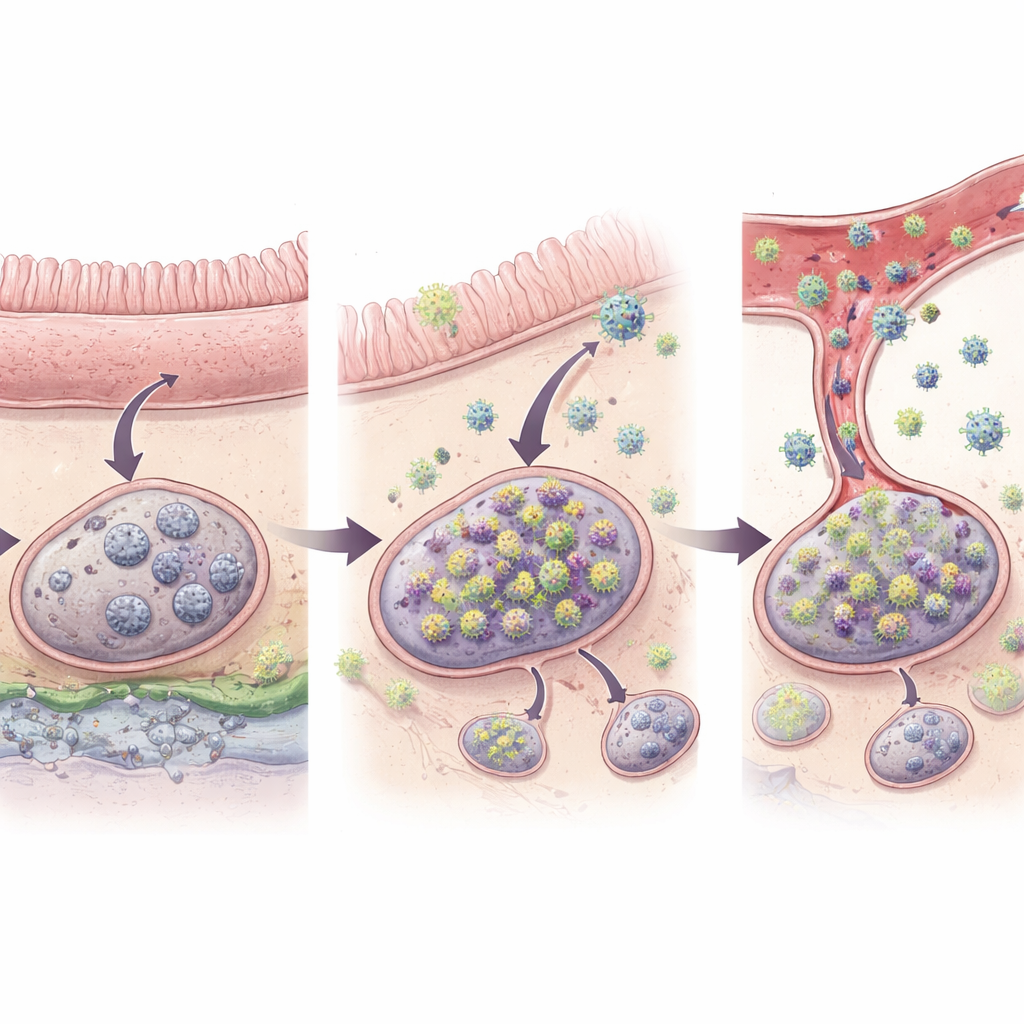
Bağırsak Neden En Önemli
Öne çıkan bir bulgu vardı: erken yeniden alevlenme olaylarının neredeyse tamamı sindirim kanalına ve ona hizmet eden bağışıklık dokularına kadar izlenebiliyordu. Yeniden alevlenmenin gerçek kökenlerini temsil ettiği değerlendirilen 27 barkodun %96’sı doğrudan bağırsaklarda veya mezenterik düğümler gibi bağırsakla ilişkili lenf düğümlerindeydi. Sadece tek bir köken yeri bağırsakla ilişkilendirilmeyen bir lenf düğümünde göründü ve karaciğer, akciğer veya kemik iliği gibi organlarda hiç köken tespit edilmedi. İstatistiksel analizler, enfekte hücre sayısının hesaba katılmasından sonra bile, bağırsakla ilişkili lenfoid dokuların diğer lenfoid bölgelerden yaklaşık on kat daha fazla olasılıkla yeniden alevlenen virüse kaynaklık ettiğini gösterdi. Bağırsakların benzersiz ortamı — sürekli olarak yiyecek ve mikroplara maruz kalma ve HIV benzeri enfeksiyonlarda sıkça görülen inflamasyon — oradaki enfekte hücreleri daha aktif tutabilir ve yeniden virüs üretimine daha kolay itebilir.
Gelecekteki Kürler için Anlamı
Özetle, bu çalışma güçlü HIV-benzeri ilaçlar durdurulduğunda virüsün neredeyse her zaman vücudun her köşesinden eşit olarak değil, bağırsak ve çevresindeki birkaç gizli rezervuardan yeniden başladığını savunuyor. Erken dönemde bu parlama olayları çok küçük ve tek bir doku yamacına sınırlı, ama virüs kana ve uzak organlara ulaştığında düzeyler hızla yükseliyor. Uzun süreli remisyonda kalmayı veya kür sağlamayı hedefleyen çabalar için bu, tedavilerin bağırsaklardaki bağışıklık dokularına nüfuz etmesi ve orada etkili olması gerektiği anlamına geliyor. İnsanlarda bu zor erişilen bölgeleri görselleştirebilen veya örnekleyebilen araçlar ya da oralarda özellikle etkili olacak şekilde ayarlanmış ilaçlar, yeniden alevlenmenin ilk kıvılcımlarının asla tutuşmasını önlemede anahtar rol oynayabilir.
Atıf: Keele, B.F., Okoye, A.A., Immonen, T.T. et al. Initial sites of SIV rebound after antiretroviral treatment cessation in rhesus macaques. Nat Microbiol 11, 648–663 (2026). https://doi.org/10.1038/s41564-025-02258-3
Anahtar kelimeler: HIV yeniden alevlenmesi, viral rezervuarlar, bağırsak lenfoid dokusu, rhesus makak modeli, antiretroviral tedavi kesintisi