Clear Sky Science · tr
Enterovirüs A ve B’de derin mutasyon tarama veri kümelerinin karşılaştırmalı analizi işlevsel farklılaşma ve terapötik hedefleri tanımlıyor
Neden küçük RNA virüsleri bizim için önemli
Enterovirüsler, dünyada sessizce dolaşan, genellikle hafif soğuk algınlıkları veya mide rahatsızlıklarına yol açan, ancak bazen felç, kalp hasarı ya da diğer ciddi hastalıklara neden olabilen geniş bir küçük RNA virüsleri grubudur. Bunlara karşı etkili çok az aşı ve daha da az ilaç bulunur; bunun bir nedeni bu virüslerin çok hızlı evrim geçirmesidir. Bu çalışma, görünüşte basit ama pratik açıdan büyük öneme sahip bir soruyu ele alıyor: bu virüsler mutasyona uğradığında, makinelerinin hangi parçaları özgürce değişebilir ve hangi parçalar o kadar hayati ki evrim onları neredeyse sabit tutar? Yanıtlar, virüsün kolayca üstesinden gelemeyeceği tedaviler tasarlamak için yeni stratejilere işaret ediyor.
Virüsün kullanım kılavuzunu tek bir mutasyonla okumak
Araştırmacılar, çok farklı hastalıklara yol açan iki insan enterovirüsüne odaklandı: çocuklarda ağır nörolojik hastalıklarla ilişkilendirilen Enterovirüs A71 ve kalp iltihabına ve hatta pankreas kanserine bağlanan koksaki B3 virüsü. Derin mutasyon tarama adı verilen bir teknik kullanarak, her virüsün proteinlerindeki neredeyse her pozisyonun sistematik olarak değiştirildiği viral kütüphaneler oluşturdular. Bu mutant virüslere hücre kültüründe enfekte olmalarına izin verildi ve yüksek verimli dizileme her değişikliğin viral büyümeyi nasıl etkilediğini ölçmek için kullanıldı. Her mutant, orijinal virüsle karşılaştırılarak viral proteomdaki hangi bölgelerin değişime toleranslı, hangilerinin güçlü şekilde kısıtlı olduğunun ayrıntılı bir haritası çıkarıldı. 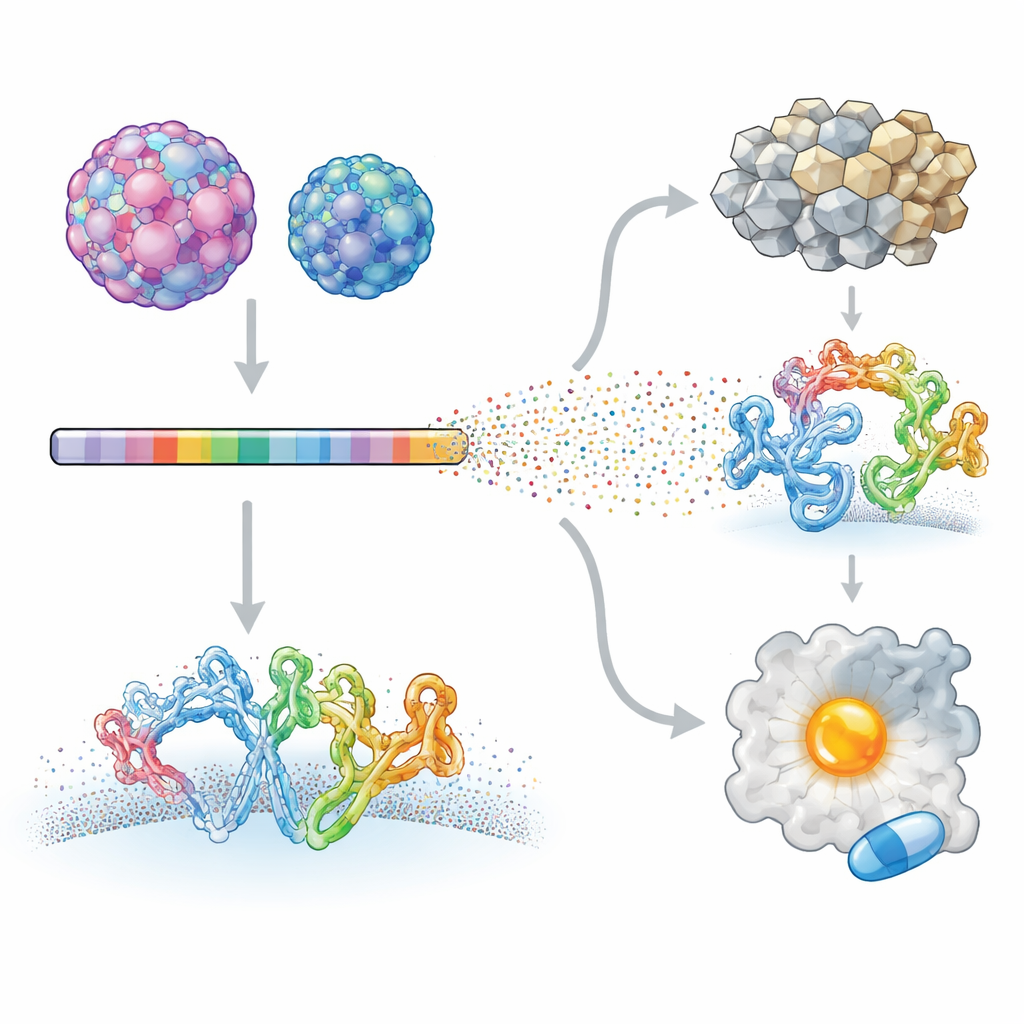
Paylaşılan sert sınırlar ve virüse özgü esneklik
Amino asit dizilerinin yalnızca yaklaşık yarısını paylaşmalarına rağmen, iki virüs benzer genel kısıtlama desenleri sergiledi. Genomu kopyalayan, viral proteinleri kesen ve RNA’yı açan içsel enzimatik “işgüzarlar” her iki virüste de mutasyona karşı son derece hassastı. Benzer şekilde, protein kabuğunu ya da kapsidi bir arada tutan gizli yüzeyleri değiştirmek virüsü bozmak olmadan zor çıktı. Buna karşılık, dışa bakan ve konakla etkileşen birçok bölge daha serbest değişebiliyor ve sıklıkla iki tür arasında keskin farklılıklar gösteriyordu. Yapısal analiz, mutasyona toleranssız korunmuş bölgelerin aktif bölgeler ve montaj ara yüzleri etrafında kümelendiğini; konak reseptörleri, membranlar veya bağışıklık molekülleriyle temas eden bölgelerin ise türlere özgü esneklik için sıcak noktalar olduğunu gösterdi.
Virüslerin hücrelerle buluşma ve savunmalardan kaçma yolları
Ardından ekip, virüsle konak arasındaki moleküler tokalaşmaya odaklandı. Enterovirüs A71 ve koksaki B3, giriş için farklı hücresel reseptörler kullanıyor ve çalışma, kapsid yüzeyindeki tam temas ayak izlerinin mutasyon toleransı açısından en farklı bölgeler arasında olduğunu ortaya koydu. Bir virüs için reseptörü kavrayan kalıntılar o virüste güçlü biçimde kısıtlıyken, diğerinde görece hoşgörülüydü; bu her birinin kenetlenme platformunu nasıl incelikle ayarladığını yansıtıyor. Benzer şekilde, hücre zarlarını yeniden şekillendirmeye ve genom replikasyonu için konak faktörleri toplamaya yardımcı olan küçük bir membran-bağlı protein olan 3A’da da farklılaşma belirlendi. Modelleştirme, iki virüsün aynı konak faktör GBF1 ile etkileşmek için kısmen farklı temas yamaları kullandığını ve bu proteini membranlara farklı derinliklerde yerleştirebileceklerini öne sürdü. Bu farklılıklar, yakın ilişkili virüslerin neden farklı dokuları enfekte edebildiğini ve farklı hastalık paternleri tetikleyebildiğini açıklamaya yardımcı olur.
Laboratuvar evrimi neyi ıskalar—ve neyi doğru yakalar
Hücre kültürü deneylerini gerçek dünya bağlamına yerleştirmek için yazarlar, mutasyon haritalarını hasta örneklerinden elde edilen binlerce doğal virüs dizisiyle karşılaştırdı. Genel olarak laboratuvarda esnek olan bölgeler doğada da değişken olma eğilimindeydi; özellikle daha geniş tür düzeyi karşılaştırmalarda bu belirgindi. Ancak her pozisyonda hangi spesifik amino asitlerin tercih edildiğini incelediklerinde, doğal evrim ile laboratuvar seçilimi en yakın uyumu tek bir virüs türü içinde gösterdi. Öne çıkan uyumsuzluklar dış kapsid yüzeyinde ve yapısal olmayan proteinler 2A ile 3A’nın konak-etkileşim bölgelerinde kümelendi—tam da bağışıklık tepkilerinin ve karmaşık konak ortamlarının en çok önem taşıması beklenen yerler. Bu, derin mutasyon taramanın viral proteinlerin temel mekanik kısıtlamalarını yakaladığını, gerçek enfeksiyonların ise in vitro’de yeniden üretmesi daha zor olan bağışıklık ve doku trofizmi gibi ek baskılar eklediğini düşündürür.
Gelecek ilaçlar için paylaşılan bir zayıf nokta bulmak
Son olarak araştırmacılar, bu haritaların ilaç geliştirme için ortak bir Aşil topuğu öne çıkarıp çıkaramayacağını sordular. Hesaplamalı araçlar kullanarak her iki virüste de küçük molekül ilaçların bağlanabileceği protein yüzeyleri üzerindeki cepleri aradılar. Ardından hangi ceplerin virüsün kendine zarar vermeden kolayca değiştiremeyeceği kalıntılardan oluştuğunu görmek için mutasyon verilerini örtüştürdüler. 2C helikaz üzerinde bulunan bir cep öne çıktı—viral RNA’yı açmaya yardımcı olan halka şeklinde bir motor. Şekli ve içerdiği kalıntılar dört büyük insan enterovirüs türü arasında yüksek derecede korunmuş, bilinen aktif bölgelerden uzakta yer alıyor ve değişiklikler doğada nadir olduğu gibi laboratuvar testlerinde de ciddi şekilde zararlıydı. 
Gelecekteki tedaviler için anlamı
Her iki önemli enterovirüste her olası tek-harf değişikliğin etkisini sistematik olarak sorgulayarak bu çalışma, paylaşılan, sert bir viral makine çekirdeği ile konakla daha esnek, virüse özgü ara yüzler arasında açık bir ayrım ortaya koyuyor. Korunmuş çekirdek, virüsün dayanıklılığını feda etmeden mutasyona uğratmasının zor olduğu, geniş spektrumlu antiviraller için cazip bir hedef yapan 2C helikaz üzerindeki yeni vurgulanan bir cebi de içeriyor. Aynı zamanda, daha uyumlu dış yüzeyler ve konak temas bölgeleri, yakın ilişkili virüslerin vücutta neden bu kadar farklı davrandığını açıklıyor ve aşılar ile bağışıklık temelli terapilerin hızlı evrimle neden başa çıkmak zorunda olduğunu gösteriyor. Birlikte, bu bulgular virüsün kendi evrimsel sınırlarını kullanarak tedaviler tasarlamak için bir yol haritası sağlıyor.
Atıf: Álvarez-Rodríguez, B., Bakhache, W., McCormick, L. et al. Comparative analysis of deep mutational scanning datasets in enteroviruses A and B identifies functional divergence and therapeutic targets. Nat Ecol Evol 10, 467–480 (2026). https://doi.org/10.1038/s41559-026-02993-8
Anahtar kelimeler: enterovirüsler, viral evrim, derin mutasyon tarama, antiviral hedefler, 2C helikaz