Clear Sky Science · tr
Monovalent sahte-doğal ürünler IDO1'in yerel E3 ligazı KLHDC3 tarafından yıkımını güçlendiriyor
Kanser Dostu Bir Enzimi Kapatmak
Bağışıklık sistemimiz sürekli olarak kanser hücrelerini arar, ancak tümörler sıklıkla vücudun kendi kimyasını ele geçirerek karşılık verir. Bu çekişmede kilit oyunculardan biri, tümörlerin bağışıklık hücrelerini etkisizleştirmesine yardımcı olan IDO1 adlı bir enzimdir. Bu çalışma, IDO1’in aktivitesini sadece bloke etmekle kalmayıp hücreleri enzimi tamamen ortadan kaldırmaya ikna eden yeni bir küçük molekül sınıfını tanımlıyor. Hücrenin doğal atık-bertaraf mekanizmasını kullanarak bu bileşikler, önceki ilaçların başaramadığı biçimde tümörlere karşı bağışıklık saldırılarını yeniden canlandırabilir.
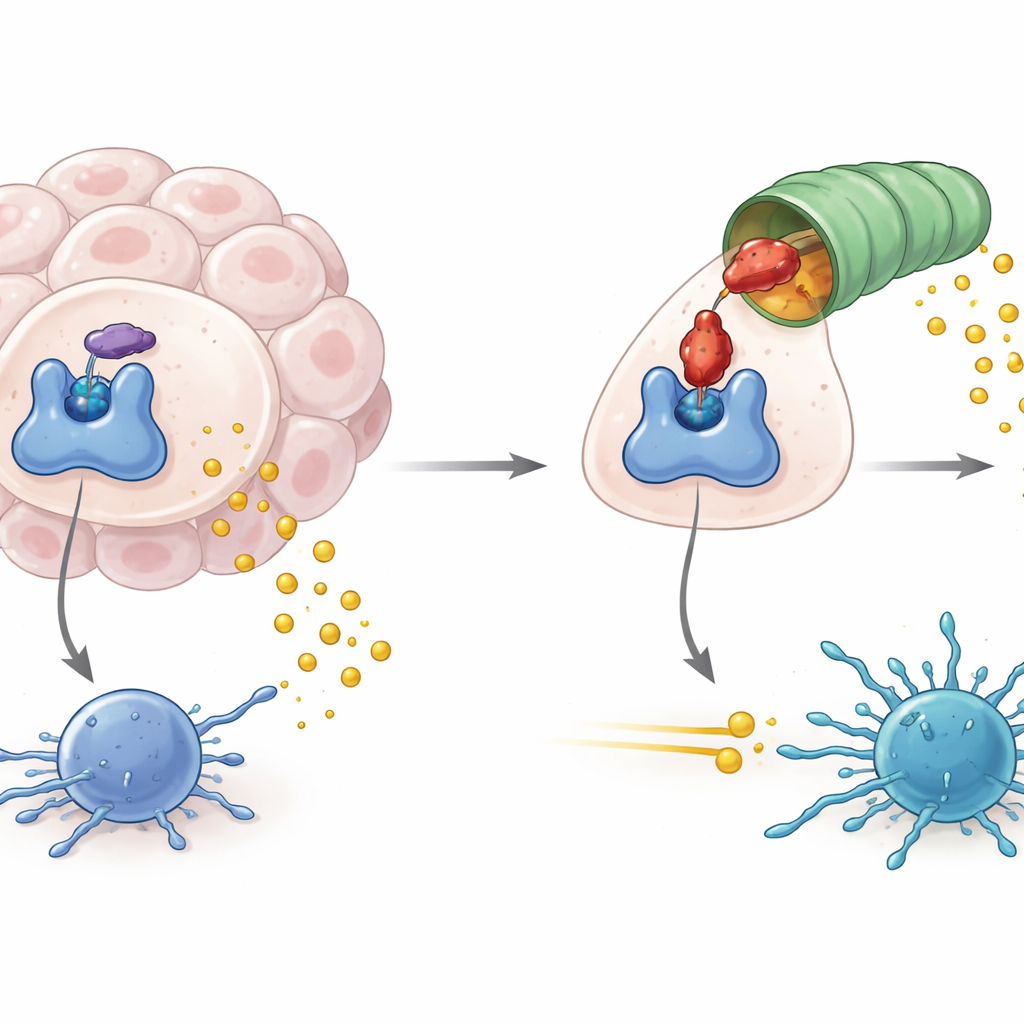
Tümörlerin Metabolik Bir Kapıcıyı Nasıl Sömürdüğü
IDO1, triptofan amino asidini kininurenin adlı ürüne dönüştüren bir metabolik yolun giriş noktasında yer alır. IDO1 bol ve aktif olduğunda triptofan seviyeleri düşer ve kininurenin yükselir; bu kimyasal ortam, tümörle savaşan T hücreleri de dahil olmak üzere bağışıklık hücrelerinin aktivitesini azaltır. Yüksek IDO1 aktivitesi yalnızca zayıf anti-tümör bağışıklığıyla değil, aynı zamanda virüs kaynaklı lenfomalar ve bazı nörodejeneratif formlarla da ilişkilendirilmiştir. Bu nedenle ilaç geliştiriciler, bu immünsüpresif sinyali kesip mevcut kanser immünoterapilerinin etkinliğini artırmak umuduyla IDO1’in enzim aktivitesini bloke etmeye odaklandı.
Basit Enzim Blokerlerinin Neden Yetersiz Kaldığı
Hayvan çalışmalarında güçlü sonuçlara rağmen, geleneksel IDO1 inhibitörlerinin klinik denemeleri hayal kırıklığı yarattı. Ortaya çıkan bir açıklama, IDO1’in sadece basit bir katalizör olmaktan öte olduğu yönünde. Kimyası engellendiğinde bile protein kendisi hâlâ tümör büyümesini ve yayılmasını destekleyen bir sinyal merkezi olarak işlev görebilir. Bazı inhibitörler hatta IDO1’i stabilize ederek hücrelerde protein miktarını artırır. Başka bir deyişle, yalnızca katalitik işlevi kapatmak, onun tümörle ilişkili enzim dışı rollerini dokunulmamış bırakabilir—veya daha kötüsü, bu rolleri güçlendirebilir.
Kendi Kendini İmha Ettiren Bileşikler Tasarlamak
Yazarlar, doğal ürünlerden esinlenen parçalar kullanılarak yeni biçimde yeniden birleştirilen sentetik bileşiklerden oluşan geniş bir “sahte-doğal” molekül kütüphanesini taradılar. (−)-myrtanol adlı bitkisel benzeri bir yapı taşından türetilen iDeg adı verilen bir molekül ailesi buldular. Bu bileşikler, IDO1’in demir içeren kofaktörü haem için ayrılmış olağan cebine bağlanır. Haemi yerinden çıkararak iDeg’ler hem IDO1’in kininurenin üretme yeteneğini zayıflatır hem de kritik olarak proteinin kuyruk bölgesinin bir kısmının yeniden şekillenmesine yol açar. Yüksek çözünürlüklü kristal yapılar, iDeg’ler haem bölgesini işgal ettiğinde C-terminus heliksinin gevşediğini ve normalde sıkı, korunaklı bir konformasyonda tutulan kısmının kısmen düzensizleştiğini gösteriyor.
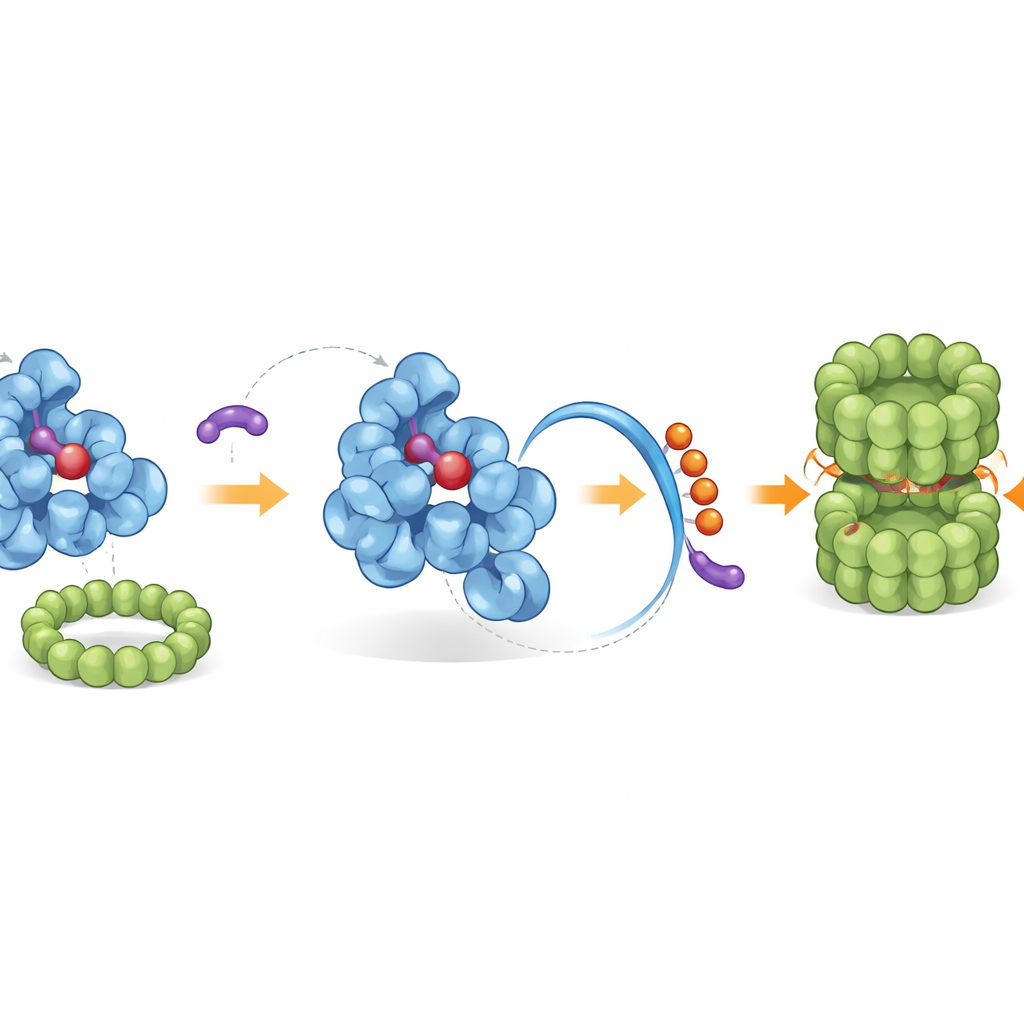
Hücrenin Yerel Temizlik Ekibini Çağırmak
Yeniden yapılandırılmış kuyruk, hücrenin atık-bertaraf mekanizmasının tanıdığı yerleşik bir “son etiketi” açığa çıkarır. Genetik taramalar ve biyokimyasal yeniden oluşturma kullanarak, araştırmacılar IDO1’in açığa çıkan kuyruğuna doğal olarak küçük ubiquitin “bayrakları” takan belirli bir ligaz kompleksini, CRL2–KLHDC3 olarak adlandırılanı tanımladılar; bu bayraklar proteazom tarafından yıkım için işaretler. Normal koşullarda yalnızca haem içermeyen IDO1 formu bu şekilde verimli bir şekilde etiketlenirken, haem bağlı IDO1 korunur. iDeg’ler yalnızca haem içermeyen formuna bağlanarak bu dengeyi değiştirir ve doğal yok etme yolunu güçlendirir. Serinin güçlü üyeleri yalnızca kininurenin üretimini bloke etmekle kalmaz, aynı zamanda IDO1 üzerindeki ubiquitin etiketlenmesini artırır ve çeşitli kanser hücre tiplerinde proteinin düzeyini keskin şekilde azaltır.
IDO1’in Kaderini ve Bağışıklık Yanıtlarını Değiştirmek
Bu çift etkili davranışın fonksiyonel sonuçları önemlidir. Yumurta kanseri hücreleriyle yapılan göç testlerinde, enzimi stabilize eden klinik olarak incelenmiş bir IDO1 inhibitörü aslında hücre hareketini hızlandırdı; bu, IDO1’in enzim dışı, tümör yanlısı rolü ile uyumludur. Buna karşılık bir iDeg bileşiği göçü yavaşlattı; bu hem enzimatik inhibisyon hem de proteinin kaybıyla tutarlıdır. Bu çalışma bu nedenle IDO1’i manipüle etmenin yeni bir yolunu açığa çıkarıyor: onu kaba kuvvetle ilgisiz bir ligaza sürüklemek yerine, hücrede zaten var olan yerel bir yıkım yolunu “aşırı şarj etmek.”
Gelecekteki Kanser Tedavileri İçin Ne Anlama Gelebilir
Uzman olmayanlar için ana mesaj, enzim inhibisyonunun niceliğinin yanında niteliğinin de önemli olduğudur. Bu yeni küçük moleküller, IDO1’i hücrenin yok etmeye hazır olduğu savunmasız bir şekle kilitleyen hassas anahtarlar gibi davranır; böylece hem metabolik hem de sinyal verme katkılarını keserler. iDeg’ler kompakt, ilaç benzeri ve IDO1’in ortadan kaldırılması için hücrenin kendi ligazına dayandığından, daha ağır ve yapay “protein-yıkıcı” ilaçlara kıyasla daha ince ve geniş uygulanabilir bir yaklaşım sunabilirler. Benzer stratejiler diğer sorunlu proteinlere uygulanabilirse, bu çalışma hastalıklı hücreleri kendi moleküler silahlarını parçalamaya teşvik eden yeni bir ilaç nesline işaret ediyor olabilir.
Atıf: Hennes, E., Lucas, B., Scholes, N.S. et al. Monovalent pseudo-natural products supercharge degradation of IDO1 by its native E3 KLHDC3. Nat. Chem. 18, 585–596 (2026). https://doi.org/10.1038/s41557-025-02021-5
Anahtar kelimeler: IDO1, kanser immünoterapisi, hedefe yönelik protein yıkımı, ubiquitin ligaz, küçük moleküllü degraderlar