Clear Sky Science · tr
Geçiş metali koordinasyonunda biyouyumlu ligand dengelenmesi, hücre içinde zararsız protein arilasyonu sağlıyor
Metalleri Nazik Hücre Araçlarına Dönüştürmek
Birçok güçlü kimyasal reaksiyon metallere dayanır, ancak aynı metalleri canlı hücrelerin yakınına getirince genellikle sorun çıkar: hasar, stres ve hücre ölümü. Bu çalışma, bir nikel atomunun etrafına doğru moleküler “tutmaç” konduğunda, hücrelere zarar vermeden karmaşık bir reaksiyonun hücre içinde gerçekleştirilebileceğini gösteriyor. Bu atılım, bilim insanlarının proteinlerin binlerce belirli noktasını işaretlemesine ve izlenmesi zor patojenlerin ortaya çıkışını takip etmesine olanak vererek, hücrelerin sağlıklı ya da hastalıklı durumlarda gerçekte neler yaptığını haritalamanın yeni yollarını açıyor.
Metallerin Hem Dost Hem Düşman Olmasının Nedenleri
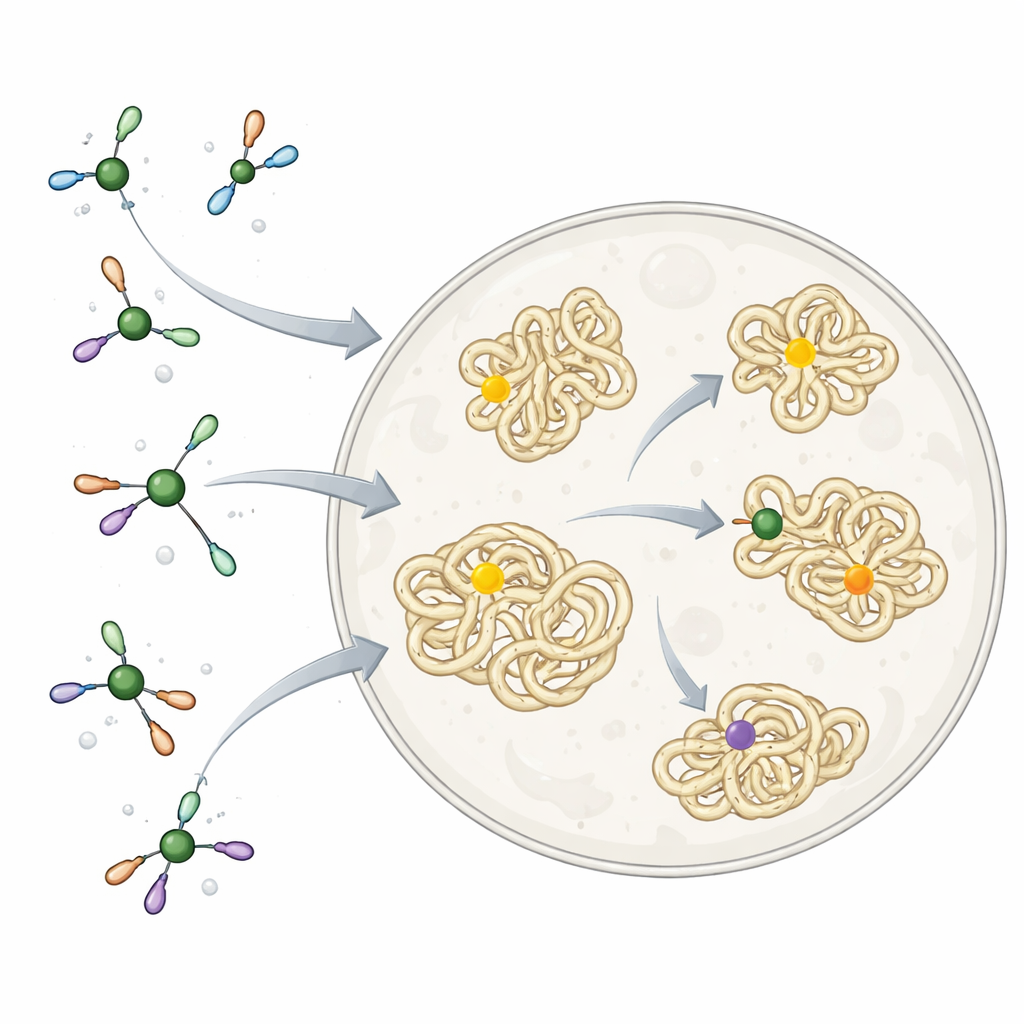
Nikel ve diğer metaller vücutlarımızda doğal enzimlerin parçaları olarak sessizce çalışır, ancak yanlış yerde bağlandıklarında toksik olabilirler. Doğa bunu, metalleri doğru hedeflere yönlendiren ve istenmeyen reaksiyonları engelleyen dikkatle seçilmiş küçük moleküller ve proteinlerle çevreleyerek çözer. Buna karşılık kimyacılar genellikle son derece reaktif ve canlıya özgü uyarlanmış olmayan metal reaktifleri kullanır. Bu reaktifler bir şişede karmaşık moleküller oluşturmak için mükemmel araçlar olmuştur, ancak özellikle bir proteindeki belirli bir aminoaside küçük bir “etiket” eklemek gibi hücrenin geri kalanını bozmayacak işler için hücre içinde serbestçe kullanılmayacak kadar serttir.
Daha Nazik Bir Nikel Reaktifi Tasarlamak
Araştırmacılar, hücrelerin nikeli nasıl ele aldığından ilham aldılar. TMEDA adlı basit, biyouyumlu bir ligandla sarılmış bir dizi nikel kompleksi inşa ettiler. Bu küçük molekül yumuşak bir kıskaç gibi davranır: nikelin yanlış hücresel bileşenlere yapışmasını engelleyecek kadar sıkı, ancak anahtar bir reaksiyonu gerçekleştirmesine izin verecek kadar gevşek. Reaksiyon, ilaçlarda sıkça bulunan düz, halka biçimli bir grup olan “aril” fragmanını proteinlerdeki sisteinin kükürt atomuna bağlar. Saflaştırılmış proteinlerde çözeltide bu nikel kompleksleri aril gruplarını tek bir sistein sitesine çok hızlı ve seçici biçimde bağladı ve birçok farklı protein şekli ve konumunda çalışarak kimyanın gerçek biyolojik moleküllerle geniş ölçüde uyumlu olduğunu gösterdi.
Canlı Hücre İçinde Protein Düzenleme
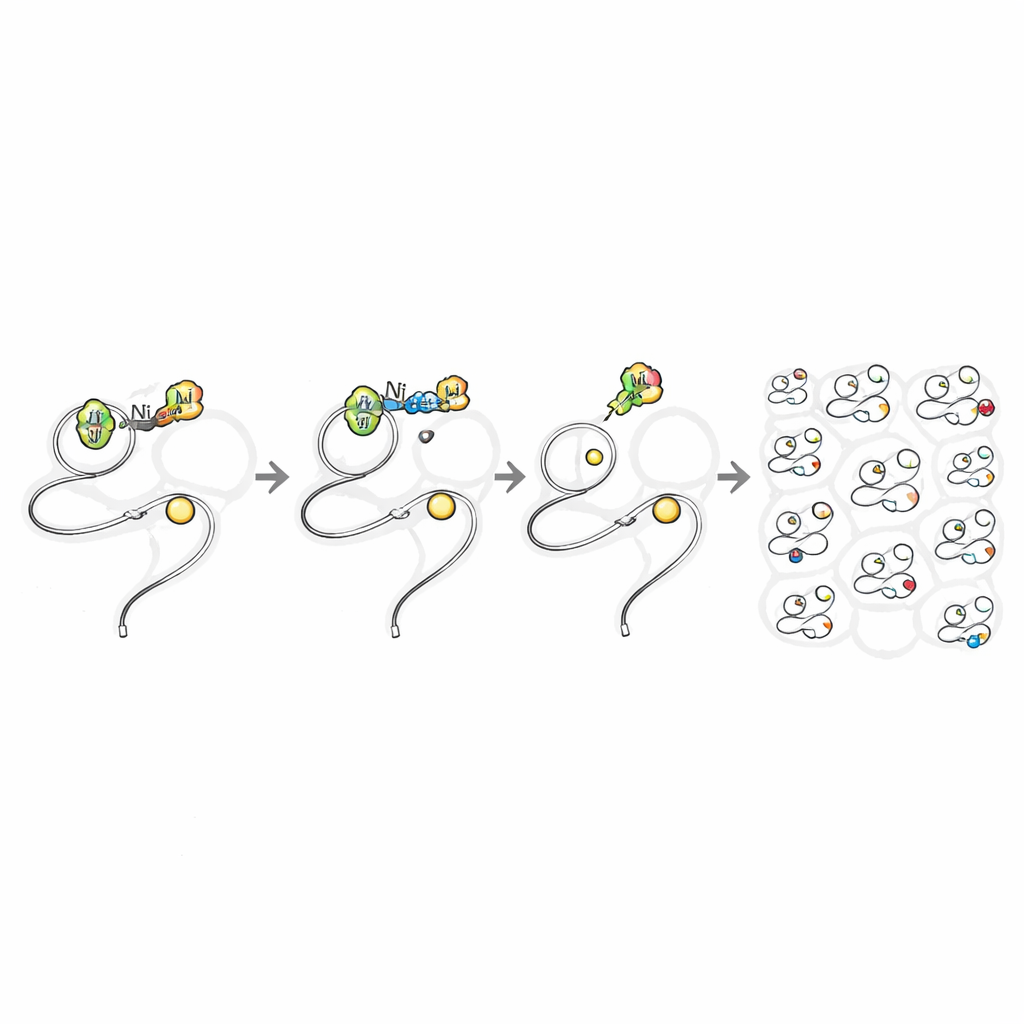
Bir sonraki adım, aynı reaktiflerin zehirli olmadan canlı hücreler içinde çalışıp çalışmayacağını test etmekti. Araştırmacılar, zararlı olduğu bilinen basit nikel tuzları ile TMEDA’ya bağlı nikel komplekslerini karşılaştırdı. Memeli hücrelerinde sade nikel kaynakları nispeten düşük dozlarda ciddi hücre ölümüne neden olurken, ligand dengeli kompleksler milimolar konsantrasyonlarda bile iyi tolere edildi. Bu güvenlik penceresi, araştırmacıların nikel reaktifleriyle bakteriyel ve memeli hücreleri yeterince uzun süre muamele ederek reaktiflerin hücre içine sızıp proteinleri modifiye etmesine izin verdi. Aril grubunun bir versiyonuna bir azid “tutmaç” koyarak, reaksiyon sonrası floresan boyalar veya biotin etiketleri tıklanarak eklenebildi; bu, canlı hücrelerin sitoplazması ve çekirdeği boyunca doza bağımlı belirgin protein boyanması ortaya koydu.
Proteomda Reaktif Protein Bölgelerinin Haritalanması
Güvenli ve hızlı bir hücre içi reaksiyon elde edildikten sonra yazarlar bunu bir keşif aracına dönüştürdü. Canlı insan hücrelerini azid taşıyan nikel reaktifi ile muamele edip sonra fotokoparılabilir bir biotin etiketi ve gelişmiş kütle spektrometrisi kullandılar; hangi sisteinlerin modifiye edildiğini tam olarak gördüler. Tek bir deneyde neredeyse 11.000 sistein sitesini ve yaklaşık 5.000 proteini tespit ettiler—bu, önceki tüm canlı hücre sistein profilleme çalışmalarının toplamından yaklaşık iki kat daha fazla proteine karşılık geliyor. Etiketleme sisteine karşı yüksek seçicilik gösterdi ve belirli protein tipleri, konumları veya bilinen aktif bölgeler konusunda az önyargı sergiledi. Dikkat çekici olarak, hedeflenen birçok protein mevcut ilaç keşfi standartlarına göre “ligandlanamaz” sayılanlar arasındaydı; bunlar arasında düşük bollukta sinyal ileten proteinler ve yalnızca genetik yöntemlerle çalışılması güç olan redoks‑duyarlı anahtarlar yer alıyordu.
Gizli Patojenleri Gerçek Zamanlı Takip Etme
Aynı kimya, enfeksiyon sırasında yapılan yabancı proteinleri yakalayacak kadar hassas olduğunu da kanıtladı. Latent viral dizilere sahip insan hücrelerinde yöntem, alternatif ekon biçimleri de dahil olmak üzere son derece düşük düzeylerde bulunan viral transkripsiyon faktörlerini tespit etti. Araştırma ekibi daha sonra iki çok farklı patojeni hücrelere enfekte etti: hücre içi bakteri Chlamydia trachomatis ve chikungunya ile ilişkili bir RNA virüsü olan Sindbis virüsü. Enfekte hücreleri nikel reaktifiyle farklı zamanlarda impulslayarak, bakterinin yaşam döngüsü evreleri arasında geçiş yaparken önemli bakteriyel ribozomal ve düzenleyici proteinlerdeki sistein sitelerini, ve RNA replikasyonunu yönlendiren kritik viral yapısal olmayan proteinlerdeki siteleri yakalayabildiler. Bu işaretlenmiş bölgeler artık gelecekte antiviral veya antibakteriyel stratejiler için potansiyel zayıf noktalar olarak öne çıkıyor.
Geleceğin Hücresel Kimyası İçin Anlamı
Nikel çevresindeki ligand kabuğunu dikkatle dengeleyerek, bu çalışma geleneksel olarak riskli bir metalin canlı hücrelerin derinliklerinde hassas, kovalent bir protein düzenleme reaksiyonunu minimum zararla gerçekleştirebileceğini gösteriyor. Bu, proteom çapında nadir, geçici veya ilaçlanması zor proteinler dahil olmak üzere reaktif sistein bölgelerinin ayrıntılı, fonksiyonel bir haritasını çıkarmayı mümkün kılıyor. Ayrıca patojenleri konak hücreleri içinde tek tek aminoasit düzeyinde takip etmek ve incelemek için bir yol sunuyor. Daha geniş anlamda, çalışma birçok diğer “yasaklı” metal kimyasının benzer biçimde evcilleştirilebileceğini düşündürüyor ve sentetik kimyanın güçlü araçlarının canlı sistemlerde güvenle çalıştığı yeni bir çağın kapısını aralıyor.
Atıf: Fu, X., Liu, W., Demyanenko, Y. et al. Biocompatible ligand balancing in transition metal coordination enables benign in-cell protein arylation. Nat. Chem. 18, 457–472 (2026). https://doi.org/10.1038/s41557-025-02017-1
Anahtar kelimeler: sistein profilleme, nikel biyokonjugasyonu, canlı hücre protein etiketleme, kemoproteomik, patojen proteom eşlemesi