Clear Sky Science · tr
RNA'ya özgü yerel çeviri, çokçekirdekli hücre büyümesi için kondensatlar tarafından düzenlenir
Büyük hücreler uzak görevleri nasıl eşzamanlar
Vücudumuzdaki hücreler genellikle tek bir çekirdeğe sahip, küçük ve bağımsız birimlerdir. Ancak bazı organizmalar — belirli mantarlar ve kas hücreleri gibi — aynı sitoplazmayı paylaşan çok sayıda çekirdekle dolu devasa bölmeler oluştururlar. Bu devlerde sinyallerin ve moleküllerin bir yerden başka bir yere difüze olması uzun zaman alabilir; bu da şu soruyu doğurur: Bu kadar geniş alanlarda büyüme ve bölünmeyi nasıl kaybetmeden koordine ederler? Bu çalışma, çokçekirdekli bir mantarda küçük damlacıkların hücre içinde gerektiği yerde protein üretimini nasıl yerel olarak ayarladığını ortaya koyarak bu soruyu ele alıyor.
Devasa bir hücreyi düzenleyen küçük damlacıklar
İpliksi mantar Ashbya gossypii'de hifa adı verilen uzun tübüler hücreler, büyümenin çoğunlukla uçlarda gerçekleştiği ve çekirdeklerin eşzamanlı olmayan biçimde bölündüğü çok sayıda çekirdek içerir. Önceki çalışmalar Whi3 adlı bir proteinin, hücre döngüsü ve uç büyümesinin anahtar düzenleyicilerini kodlayan belirli haberci RNA'larla (mRNA'lar) mikroskobik damlacıklar ya da kondensatlar oluşturduğunu göstermişti. Burada yazarlar bu kondensatların gerçekten ne yaptığını anlamayı amaçladılar. Hızlı üç boyutlu görüntüleme kullanarak Whi3 kondensatlarının hücrenin neresinde olduklarına ve yerel büyüme ile çekirdek bölünme durumuna bağlı olarak boyut ve sayı bakımından değiştiğini buldular. Yavaş büyüyen hif uçlarının yakınında büyük kondensatlar kümeleşirken, daha küçük ve değişken kondensatlar belirli hücre döngüsü aşamalarındaki çekirdeklerin etrafını sarıyordu. Normal kondensatları oluşturamayan mutant mantarlar uçlarda daha hızlı büyüdü ve çekirdek bölünmeleri daha senkron görünerek kondensat özelliklerinin bu süreçleri koordine etmeye yardımcı olduğunu düşündürdü.
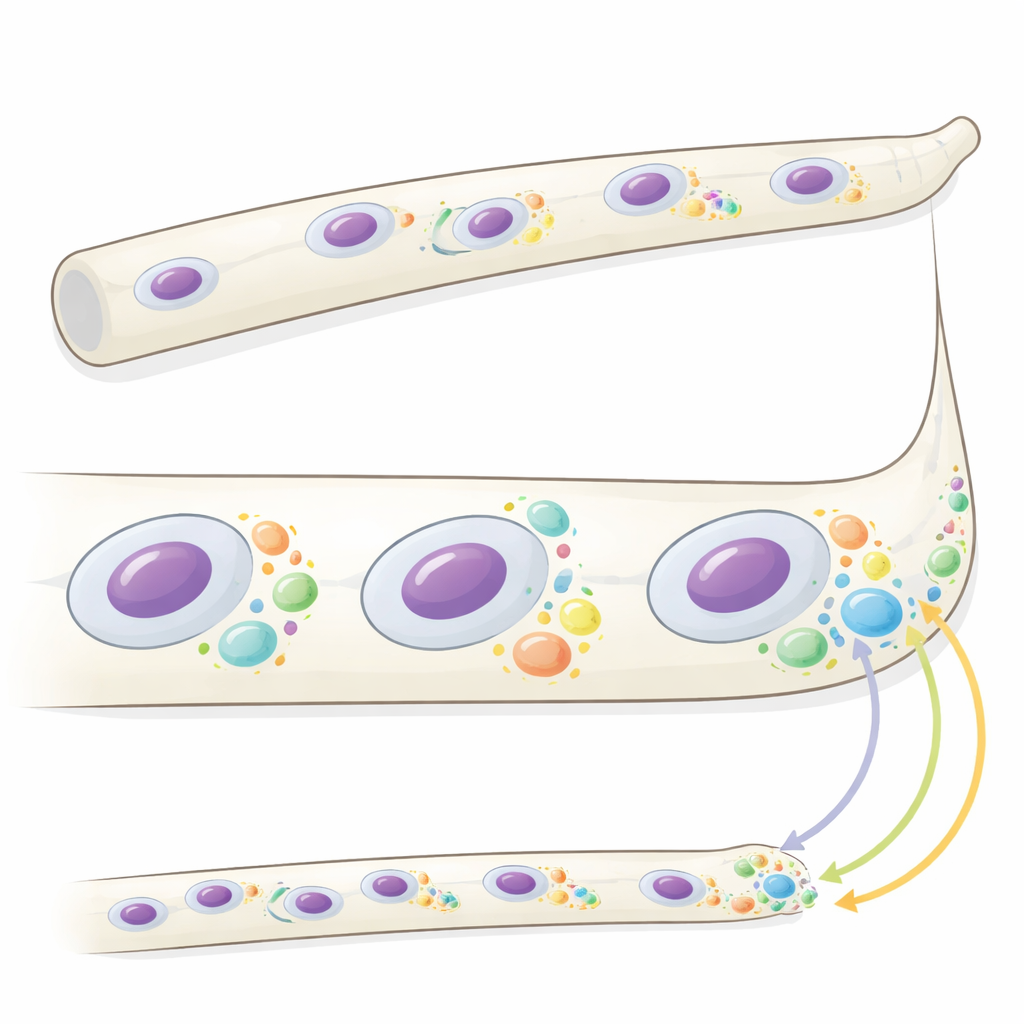
Yerel protein üretimi uzay ve zamanda yazılmış
Whi3 kondensatlarının proteinlerin nerede yapıldığını kontrol edip etmediğini görmek için ekip iki önemli Whi3-bağlı iletinin çevirisini — mRNA'yı proteine çevirme sürecini — ölçtü. Bunlardan biri CLN3, hücreleri bölünme döngüsünden geçirmeye yardımcı olan bir siklin kodluyor; diğeri BNI1 ise hifa ucundaki büyümeyi şekillendiren bir faktörü kodluyor. Bireysel endojen mRNA moleküllerinde aktif ribozomları algılayan hassas bir floresan tabanlı yöntem kullanarak araştırmacılar CLN3'ün özellikle belirli çekirdeklerin yakınında ve döngülerinin belirli evrelerinde, özellikle mitotik çekirdeklerin etrafında yoğun olarak çevrildiğini gösterdiler. BNI1 mRNA'ları hifa uçlarında kümeleniyordu, ancak oradaki çeviri genellikle seyrek ve değişkendi. Whi3'ün davranışı bir fosfo-mimik mutasyonla değiştirildiğinde BNI1 çevirisi uçlarda güçlü biçimde zenginleşti ve uç büyümesi hızlandı; bu da Whi3'ün durumuna ve konumuna bağlı olarak çeviriyi ya baskılayabileceğini ya da izin verebileceğini ortaya koydu.
Asgari parçalar, çok sayıda çıktı
Bu ayarlamanın kondensat bileşenlerinin içsel bir özelliği olup olmadığını test etmek için yazarlar sistemi hücre dışı özütlerde yeniden oluşturdular. CLN3 veya BNI1 mRNA'larının düzenleyici bölgelerine bir lüçiferaz raporlayıcı bağlayıp bu RNA'ları farklı konsantrasyonlarda saflaştırılmış Whi3 ile karıştırdılar. Damlacık oluşmadığı düşük seviyelerde çeviri çok az değişti. Kondensat oluşumunu tetikleyen daha yüksek seviyelerde ise CLN3'e bağlı çeviri, Whi3 konsantrasyonu ve kondensat boyutu arttıkça güçlü biçimde baskılandı. BNI1 farklı davrandı: ılımlı kondensat düzeyleri çevirisini artırırken, daha bol ya da daha büyük kondensatlar sistemi baskıya çevirdi. Daha küçük veya daha az damlacık oluşturan Whi3 mutantları ya da daha az Whi3 bağlanma bölgesi içeren RNA'lar bu yanıtları kaydırdı; çoğunlukla baskıyı hafifleterek çeviriyi artırdılar. Bu deneyler aynı temel bileşenlerin — Whi3, hedef RNA'ları ve onların kondensatları — yalnızca konsantrasyon, etkileşim gücü veya damlacık boyutu değiştirilerek bir çeviri durumu sürekliliği üretebildiğini gösteriyor.
Çevirinin olduğu yer: damlacığın kenarında
Toplu ölçümler birçok molekülü ortaladığı için kondensat içinde veya çevresinde çevirinin nerede gerçekleştiğini ortaya koyamaz. Bunu doğrudan görselleştirmek için ekip yeni protein zincirleri ribozomlardan çıktığında parlayan bir “MoonTag” raporlayıcı kullandı. İn vitro olarak Whi3–RNA damlacıkları üzerinde ve içinde MoonTag sinyallerinin biriktiğini gördüler; bu, bu kondensatların sadece depo alanları değil, gerçekten aktif çeviri bölgeleri olabileceğini kanıtlıyor. Çarpıcı biçimde ribozomlar ve yeni sentezlenen protein sinyalleri damlacık ara yüzünde en güçlüydü ve her kondensatın etrafında parlak bir halka oluşturdular. Hacme göre daha fazla yüzey alanına sahip daha küçük kondensatlar, RNA başına daha fazla çeviriyi destekleyerek daha büyük, genel olarak daha baskılayıcı damlacıklardan daha fazla aktivite gösterdi. RNA valansı veya Whi3’ün yük durumu değiştirilince çeviri-izin veren bölgenin yüzeyde mi yoksa daha derinlerde mi yer aldığı kaydı; bu da kondensatın ince moleküler özelliklerinin çeviri makinelerinin sakin RNA'lara erişimini nasıl ayarladığını gösteriyor.
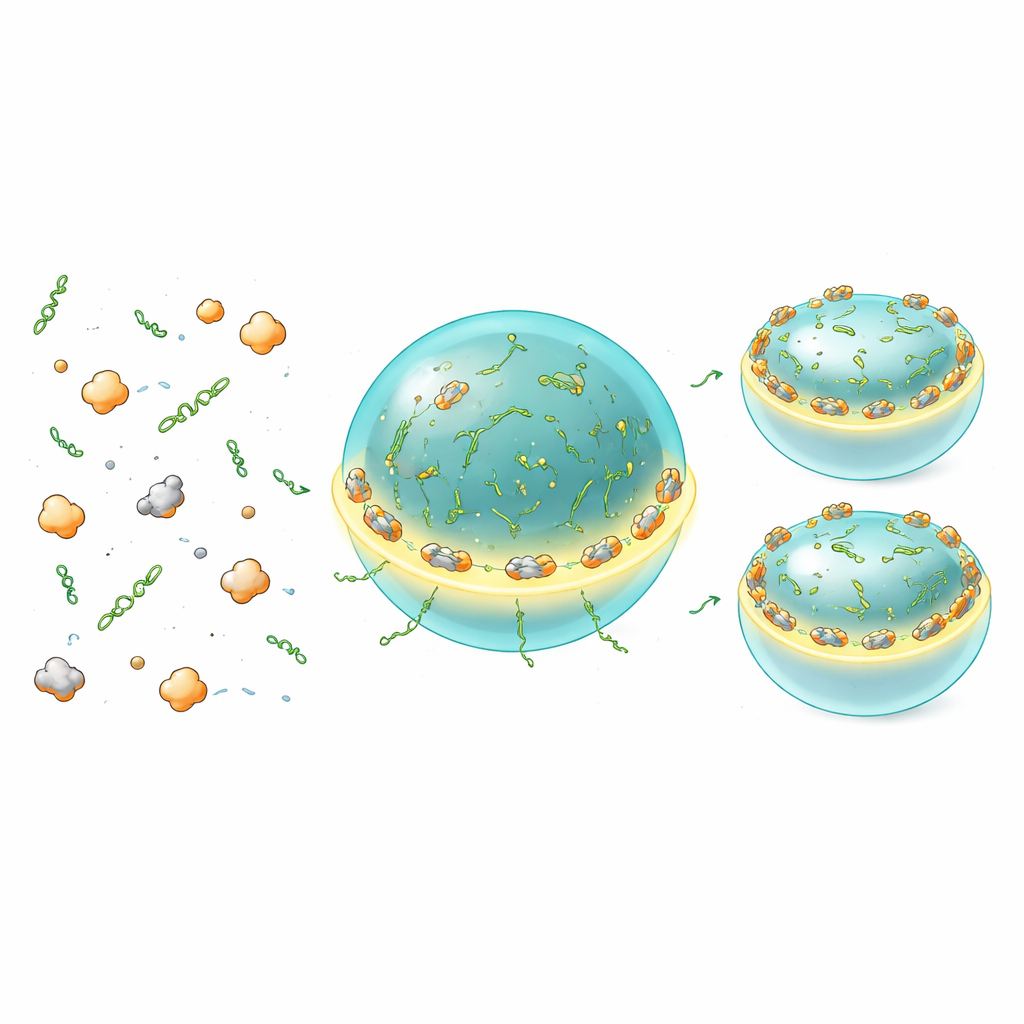
Dengeli büyüme için ince ayarlı dozaj
Toplu olarak bu çalışma Whi3–RNA kondensatlarını basit açık-kapalı anahtarlar yerine yerel olarak üretilen proteini ölçen ayarlanabilir vanalar olarak tasvir ediyor. Mantarda bu, CLN3 siklininin seçilmiş çekirdeklerin etrafında atımlar halinde üretilerek bölünme döngülerinin faz dışı tutulmasını sağlarken, BNI1’in hifa uçlarında aralıklı patlamalar halinde üretilerek büyümeyi destekleyip tek bir noktada kontrolsüz genişlemeyi önlemesi anlamına geliyor. Kondensat oluşumu veya özellikleri bozulduğunda bu ince kontrole sahip olunamıyor: protein üretimi uzay ve zamanda daha uniform hale geliyor, çekirdekler senkron olarak bölünüyor, dallanma desenleri değişiyor ve genel morfoloji bozuluyor. Genel okuyucu için ana mesaj, hücrelerin küçük faz-ayrılmış damlacıkları uzamsal ve zamansal olarak ayarlanabilir reaktörler olarak kullanarak devasa, çokçekirdekli hücrelerin uzun mesafelerde büyüme ve bölünmeyi koordine etmek için proteinlerin nerede ve ne zaman yapılacağını yerel olarak şekillendirebildikleridir.
Atıf: Geisterfer, Z.M., Jalihal, A.P., Cole, S.J. et al. RNA-specific local translation is patterned by condensates for multinucleate cell growth. Nat Cell Biol 28, 507–519 (2026). https://doi.org/10.1038/s41556-026-01887-y
Anahtar kelimeler: biyomoleküler kondensatlar, yerel çeviri, hücre döngüsü kontrolü, fungal hif, faz ayrımı