Clear Sky Science · tr
Lizinin-11 ubikitinasyonu, cGAS–STING ve Toll-benzeri reseptörler 3 ve 4 tarafından tip I/III interferon indüksiyonunu yönlendirir
Hücrelerimiz Alarmı Nasıl Çalar
Virüsler ya da tehlikeli moleküller vücuda girdiğinde, hücrelerimiz birkaç dakika içinde güçlü antiviral alarm sinyalleri olan interferonları başlatıp başlatmamaya karar vermelidir. Bu sinyaller bizi ağır enfeksiyonlardan kurtarabilir—ancak yanlış tetiklendiğinde zarar verici otoimmün hastalıklara da yol açarlar. Bu çalışma, hücre içinde interferon yanıtlarının ne zaman açılacağı ve ne zaman dizginleneceği konusunda karar vermeye yardımcı olan, daha önce gizli kalmış bir moleküler “anahtar panosunu” ortaya koyuyor. Bu anahtar panosunu anlamak, daha iyi aşılar, antiviral tedaviler ve interferon kaynaklı bozukluklar için tedavi ipuçları sunuyor.
Sorunu Hisseden Koruyucular
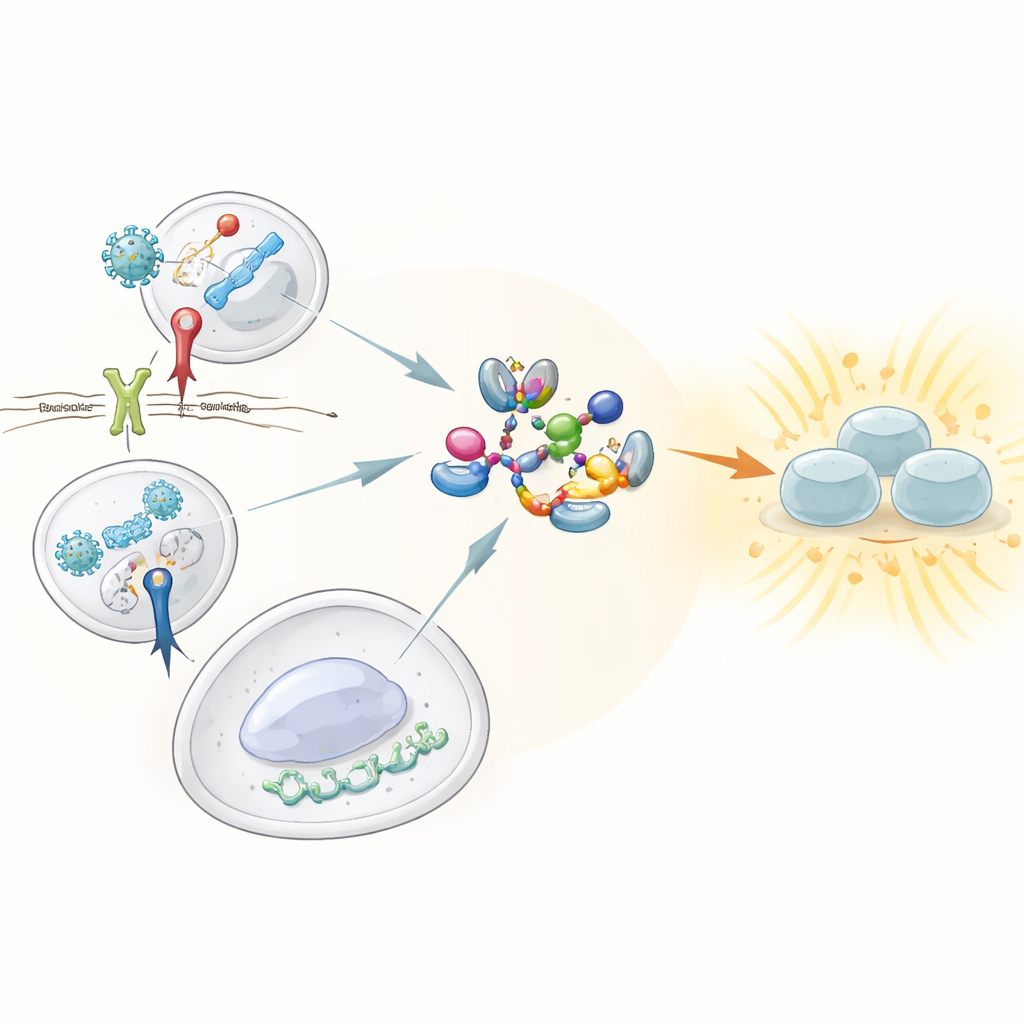
Doğuştan gelen bağışıklık sistemimiz, virüs ve bakterilere özgü işaretleri devriye gezen kalıp tanıma reseptörleri olarak bilinen bekçiler üzerine kurulur. Bunların arasında güçlü interferon yanıtları tetikleyebilme yetenekleriyle üçü öne çıkar: çift sarmallı viral RNA’yı algılayan Toll-benzeri reseptör 3 (TLR3); bakteriyel hücre duvarı bileşenini tanıyan Toll-benzeri reseptör 4 (TLR4); ve hücre içinde yanlış yerde bulunan serbest DNA’yı saptayan cGAS–STING yolu. Üçü de merkezi bir enzim olan TBK1’i aktive etmek zorundadır; TBK1 de transkripsiyon faktörü IRF3’ü açarak tip I ve III interferon üretimini başlatır. Bugüne dek bu algılayıcıların TBK1’i nasıl ortak bir şekilde aktive ederek onun aktif konuma geçtiğini anlamak sınırlıydı.
Gizli Bir Moleküler Bağlayıcı
Araştırmacılar, ANKIB1 adlı bir proteinin bu algılayıcılar ile TBK1 arasında kritik bir bağlayıcı görevi gördüğünü keşfettiler. ANKIB1, diğer proteinlere küçük moleküler etiketler, yani ubikitin zincirleri ekleyen bir enzimdir. Önemli olarak, daha önce hücre bölünmesinde bilinen rolleriyle tanınan "K11" bağlantısına dayanan özgül bir zincir tipi oluşturur. ANKIB1’den yoksun insan hücrelerinde, TLR3 uyarımı veya STING aktivasyonu artık TBK1 ve IRF3’ün uygun şekilde aktive olmasına yol açmıyor ve interferon genleri neredeyse hiç açılmıyordu. ANKIB1’in geri verilmesi yanıtı yeniden sağladı; bu da tek bir enzimin antiviral alarmın bu kolunu başlatmak için hem gerekli hem de yeterli olduğunu gösterdi.
Ara Proteinler İçin Bir Bağlanma Platformu Kurmak
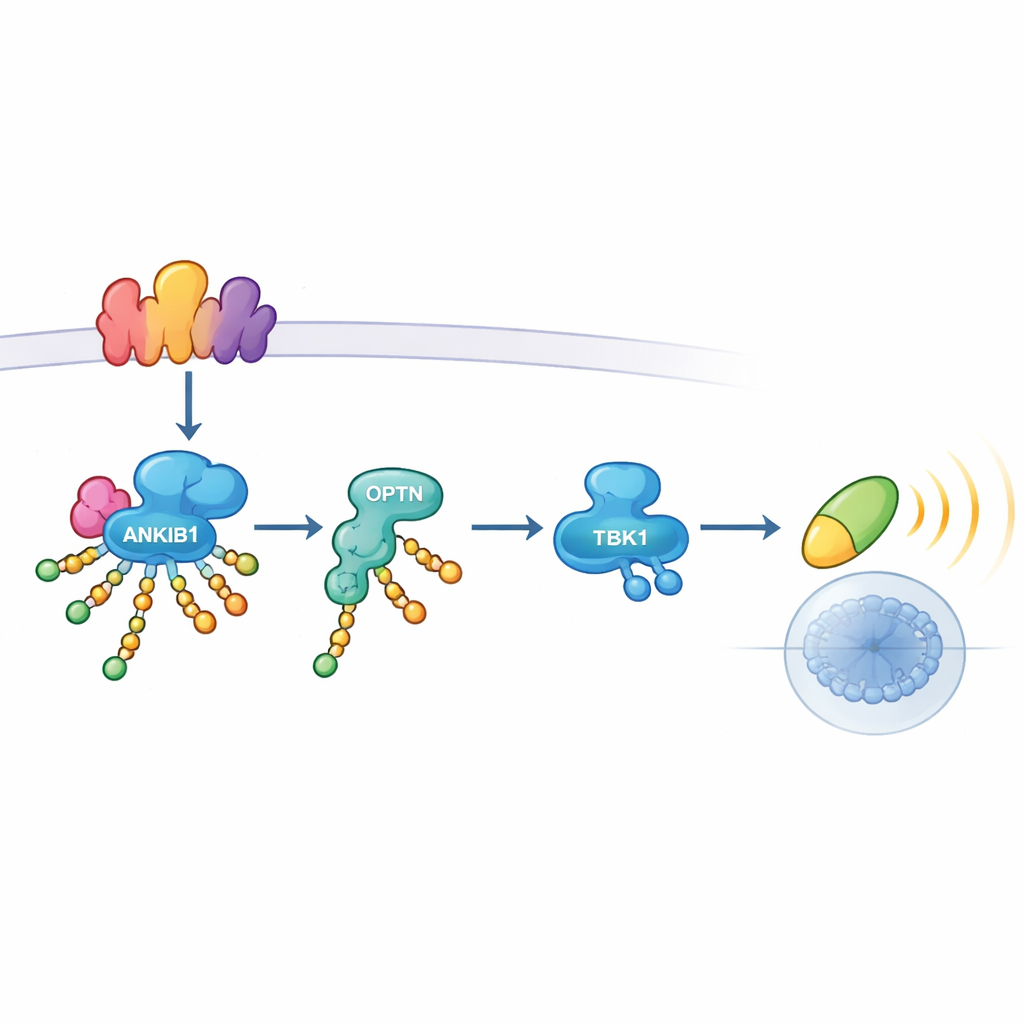
Daha yakından bakıldığında ANKIB1’in etkisini nasıl uyguladığı görülüyor. TLR3 veya STING tehlikeyi algıladığında, sinyalozom adı verilen çok proteinli platformlar toplanır. ANKIB1, ubikitini tanıyan bir bölge aracılığıyla bu platformlara çekilir. Orada, TRIF ve STING gibi adaptör proteinler dahil olmak üzere birkaç kilit bileşeni K11-bağlantılı ubikitin zincirleriyle süsler. Bu zincirler proteinleri yok edilmek üzere işaretlemez; bunun yerine moleküler Velcro gibi davranırlar. Başka bir protein olan Optineurin (OPTN) özellikle bu modifiye bölgelere çekilir. Bir röle adaptörü olarak görev yapan OPTN, TBK1’i komplekse getirir, böylece TBK1 aktive olabilir ve sinyali IRF3 ve interferon genlerine iletebilir. OPTN kaldırıldığında TBK1 aktivasyonu çöktü; bu da ANKIB1 tarafından yapılan K11-bağlantılı işaretlemenin ve OPTN bağlanmasının tek, vazgeçilmez bir eksen oluşturduğunu vurguluyor.
Bu Yol Ne Zaman Önemlidir—Ne Zaman Değildir
Araştırma ekibi bir sonraki adımda bu mekanizmanın tüm antiviral algılayıcılar için evrensel olup olmadığını sordu. ANKIB1’in, OPTN’i TBK1’e bağlayan ana adaptör olarak kullanan TLR3, TLR4’ün TRIF-bağımlı kolu ve cGAS–STING yolu aracılığıyla interferon indüksiyonu için hayati olduğunu buldular. Buna karşılık, viral RNA’yı algılayan başka bir sensör olan RIG-I, farklı bir adaptör protein setine dayanır ve TBK1’i aktive etmek için ANKIB1 veya OPTN’e ihtiyaç duymaz. Farelerde yapılan deneyler hücre temelli bulgularla paralellik gösterdi. Ankib1’den yoksun hayvanlar TLR3 veya STING aktive edildikten sonra çok daha az interferon üretti, ölümcül interferon kaynaklı inflamatuar sendromdan korunmuş oldu; ancak cGAS–STING kaynaklı interferon ile kontrol edilen DNA virüsü herpes simpleks virüs 1 ile enfeksiyona karşı çok daha savunmasız hale geldi. Çoğunlukla RIG-I tarafından algılanan influenza virüsüne yanıtlar büyük ölçüde sağlam kaldı.
Koruma ile Zararı Dengelemek
Birlikte ele alındığında bu sonuçlar, ANKIB1 tarafından oluşturulan K11-bağlantılı ubikitin zincirlerini doğuştan gelen antiviral sinyalizasyonun önemli bir dalında merkezi bir para birimi olarak ortaya koyuyor. OPTN için bağlanma bölgeleri yaratarak ANKIB1, TLR3, TLR4 (TRIF aracılığıyla) ve cGAS–STING’in algıladığı tehlikeyi güçlü interferon üretimine dönüştüren hassas moleküler röleyi bir araya getirmeye yardımcı olur. Bu eksen çift taraflıdır: belirli virüslere karşı savunma için elzemdir, ancak aşırı aktive olduğunda interferon kaynaklı inflamatuar hastalıkları da körükler. ANKIB1’in katalitik aktivitesinin ve özgül bölgelerinin bu işlev için gerekli olması, otoimmün koşullarda zararlı interferon yanıtlarını azaltmak veya zayıf antiviral bağışıklığı güçlendirmek amacıyla geliştirilecek gelecekteki ilaç hedefleri için cazip adaylar sunar.
Atıf: Betrancourt, A., Cinko, M.T., Varanda, A.B. et al. Lysine-11 ubiquitination drives type-I/III interferon induction by cGAS–STING and Toll-like receptors 3 and 4. Nat Cell Biol 28, 608–621 (2026). https://doi.org/10.1038/s41556-026-01886-z
Anahtar kelimeler: doğuştan gelen bağışıklık, interferon sinyalizasyonu, ubikitinasyon, cGAS–STING yolu, viral enfeksiyon