Clear Sky Science · tr
ER yeniden yapılanması yaşlanmanın bir özelliğidir ve ER-fajiye bağlıdır
Hücrenin İç Kıvrımlarının Yaşlanırken Neden Önemli Olduğu
Vücudumuzdaki hücreler, endoplazmik retikulum (ER) olarak adlandırılan labirent benzeri bir membran sistemiyle doludur. Bu yapı yağ ve protein sentezine yardımcı olur, şeker ve kalsiyumu yönetir ve diğer hücre parçalarıyla sürekli iletişim kurar. Bu ağ üzerinden çok sayıda hayati işlem geçtiği için, ER’deki uzun süreli herhangi bir yeniden şekillenme dokularımızın nasıl yaşlandığını, strese karşı ne kadar dayanıklı olduklarını ve nihayetinde sağlıklı kalma süremizi etkileyebilir. Bu çalışma görünüşte basit bir soruyu soruyor: ER kendisi belirli, düzenli bir şekilde mi yaşlanır ve eğer öyleyse bu değişiklik zararlı bir aşınma mı yoksa yerleşik koruyucu bir strateji mi?
Hücrenin Tezgahında Gizli Bir Değişim
Gelişmiş mikroskoplar ve floresan etiketler kullanarak, yazarlar küçük solucan Caenorhabditis elegans içinde ER’yi genç erişkinlikten yaşlılığa geçiş sırasında canlı hayvanlarda izlediler. Genç hücrelerde ER, protein üreten makinelerle dolu geniş, üst üste dizilmiş tabakalar halinde görünür; düzenli dizilmiş fabrika katları gibi. Solucanlar yaşlandıkça bu tabakalar hacimce küçüldü ve yerlerini daha ince, daha tübüler bir ağ aldı; bu ağ daha az yer kaplıyordu. Ölçümler, genel ER içeriğinin belirgin şekilde azaldığını ve şeklin değiştiğini gösterdi; bu durum rastgele hasardan ziyade organelin koordineli bir şekilde küçülmesi ve yeniden yapılandırılması olduğunu işaret ediyor.
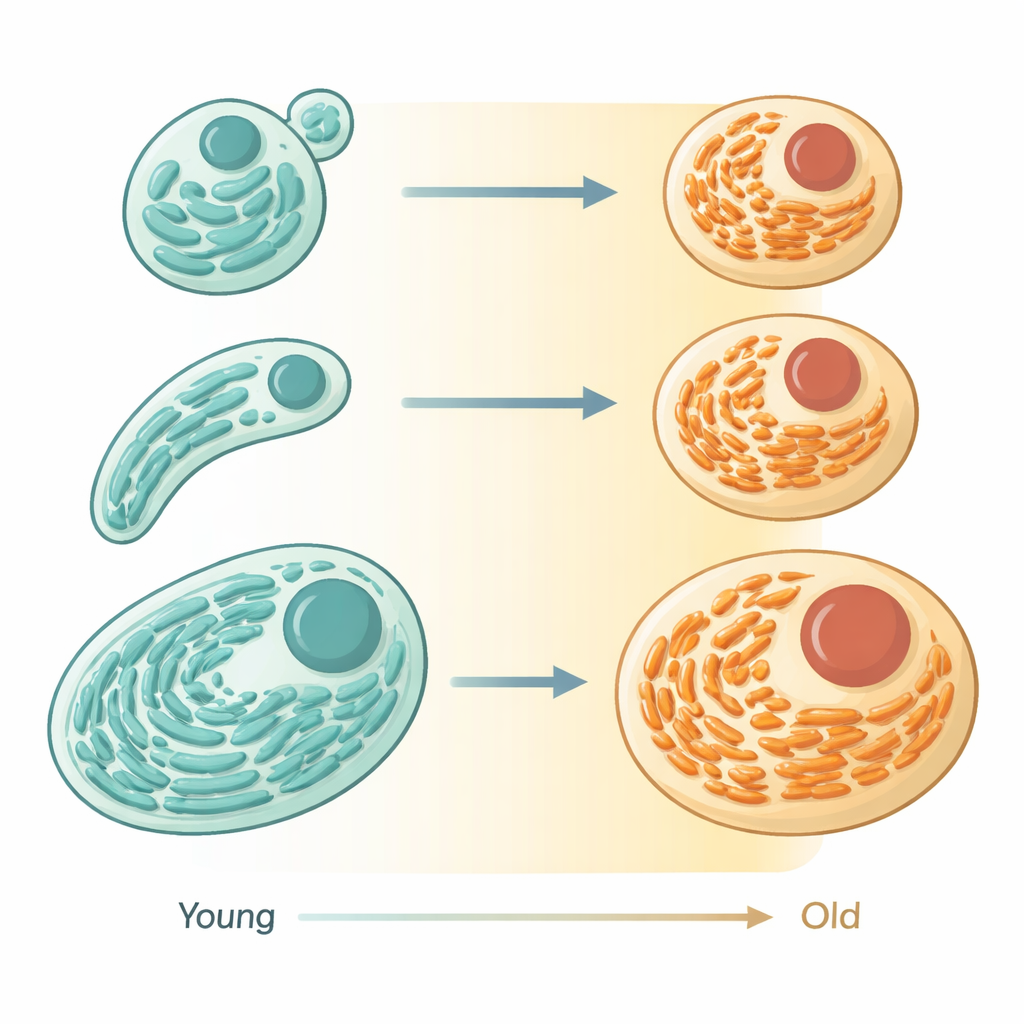
Proteinden Yağla İlgilenmeye
Biyolojide şekil genellikle fonksiyonu işaret eder ve burada da aynı şekilde doğrulandı. Araştırmacılar ER ile ilişkili proteinlerin solucan dokuları boyunca zaman içinde nasıl değiştiğini karşılaştırdı. Diğer proteinlerin yapımı, katlanması ve kalite kontrolünde yer alan proteinler, tabaka benzeri ER kaybıyla eş zamanlı olarak yaşla birlikte azaldı. Buna karşın yağ ve membran metabolizmasına bağlı birçok ER proteini sabit kaldı veya arttı. Bu desenler birlikte, yaşlanan hücrelerin toplu protein üretimini azaltıp ER’nin kaynaklarını yağ ve membran yönetimine yeniden yönlendirdiğini öne sürüyor. Çarpıcı biçimde, yazarlar yaşlanan farelerden elde edilen büyük veri setlerine baktıklarında benzer bir tablo gördüler: salgı ve protein işleme için yer alan ER proteinleri eğilimle azalma gösterirken, lipid metabolizması ve otofaji ile bağlantılı olanlar nispeten korundu ya da arttı.
Yeniden Yapılanmanın Arkasındaki Hücresel Geri Dönüşüm Yolu
Bu geniş ölçekli yeniden şekillenmeyi ne tetikliyor? Ekip değişiklikleri ER-fajiye, yani hücrenin ER parçalarını lizozomlarda parçalanmak üzere geri dönüşüm veziküllerine paketlediği seçici bir oto-faj biçimine bağladı. Solucanlarda temel otofaji genlerinin engellenmesi, ER kütlesinin normal yaşa bağlı kaybını ve tabakalardan tübüllere geçişi önledi; bu da bu geri dönüşüm yolunun yalnızca döküntüleri temizlemediğini, aynı zamanda organeli aktif olarak biçimlendirdiğini gösteriyor. Maya üzerinde yapılan bağımsız deneyler, yaşlandıkça ER bileşenlerinin otofajiye bağlı olarak hücrenin geri dönüşüm merkezine yönlendirildiğini doğruladı. Elektron mikroskobu, bozucu kompartımanlar içinde ER parçacıklarını ortaya koydu ve ağın parçalarının amaçlı olarak çıkarıldığını gösteren fiziksel kanıt sağladı.

Ortak Bir Yaşlanma Programının Dokuya Özgü Kontrolü
ER yeniden yapılanması bağırsak, cilt benzeri hipodermis, kas ve nöronlar gibi birçok solucan dokusunda görüldü, ancak tetikleyiciler dokuya özgü çıktı. Hipodermiste daha önce az bilinen bir membran proteini olan TMEM-131, ER dönüşümünü kollajen işlemesiyle bağladı. TMEM-131 azaltıldığında, bu dokudaki yaşa bağlı ER kaybı büyük ölçüde engellendi; bu da ER’nin kollajen “müşterileri” azaldığında küçültüldüğünü düşündürüyor. Buna karşılık, bağırsakta kilit düzenleyici, açılmamış protein yanıtının merkezi bir stres algılama yolu olan IRE-1–XBP-1 koluydu. Bu sinyal dalı susturulduğunda bağırsaklardaki ER yaşlanma sırasında korundu; bu, bu organda ER stres sinyalinin ER parçalarının ne zaman feda edileceğine karar vermeye yardımcı olduğunu gösteriyor.
Daha Uzun Bir Yaşam İçin ER’yi Yeniden Kablolamak
Çalışma ayrıca ER yeniden yapılanmasını ömür uzamasıyla ilişkilendiriyor. Solucanlarda, insülin benzeri sinyallerin azaltılması, mTOR besin algısının düşürülmesi, germ hattının uzaklaştırılması veya hafifçe protein sentezinin yavaşlatılması gibi iyi bilinen birkaç ömrü uzatan müdahale, ER küçülmesini ve erişkinliğin erken döneminde tübüler ağların artmasını tetikledi; bu değişiklikler yaşlılığı beklemedi. Önemli olarak, ER-faji devre dışı bırakıldığında, mTOR inhibisyonunun maya ve solucanlarda normalde ürettiği uzun ömür etkileri büyük ölçüde azaldı veya kayboldu. Bu, dikkatle yönetilen ER budamasının sadece yaşlanmanın veya tedavinin yan etkisi olmadığını, hücrelerin daha dayanıklı bir duruma ulaşmasının mekanizmalarından biri olduğunu gösteriyor.
Sağlıklı Yaşlanma İçin Anlamı
Gözlemciye göre, yaşlanma sırasında önemli bir hücre yapısının büyük bir kısmını kaybetmek tamamen zararlı gibi gelebilir. Buradaki çalışma daha nüanslı bir tablo çiziyor. ER, seçici oto-yeme ve dokuya özgü düzenleyiciler yoluyla aktif olarak yeniden şekillendiriliyor gibi görünüyor; böylece yaşlanan hücreler daha az yeni protein üretip lipit ve membran yönetimine daha çok yatırım yapıyor ve muhtemelen kronik strese karşı riski azaltıyor. Bu yeniden yapılanma maya ile memeliler arasında korunmuş görünüyor ve en az bazı yaşam süresi uzatma biçimleri için gerekli. Ancak uzun vadede ER’nin küçültülmesi takaslara yol açabilir; diğer organellerin onarımını ve geç dönemdeki çöküşün yönetimini etkileyebilir. ER-faji ve ER dinamiklerini normal ve geciktirilmiş yaşlanmanın temel özellikleri olarak ortaya koyarak, bu araştırma gelecekte daha sağlıklı ve daha dayanıklı dokuları teşvik etmek için ayarlanabilecek yeni bir kontrol setini vurguluyor.
Atıf: Donahue, E.K.F., Hepowit, N.L., Ruark, E.M. et al. ER remodelling is a feature of ageing and depends on ER-phagy. Nat Cell Biol 28, 449–464 (2026). https://doi.org/10.1038/s41556-025-01860-1
Anahtar kelimeler: endoplazmik retikulum, otofaji, hücresel yaşlanma, protein homeostazı, lipid metabolizması