Clear Sky Science · tr
Zaman çözünürlüklü fonksiyonel genomik ve derin öğrenme, otofajinin küresel hiyerarşik kontrolünü ortaya çıkarıyor
Hücreler Kendilerini Nasıl Geri Dönüştürür—Ve Ne Zaman Duracaklarını Nasıl Biler
Hücrelerimiz, kendi parçalarını otofaji adlı süreçle geri dönüştürerek kıt zamanlarda hayatta kalır—kelimenin tam anlamıyla “kendini yeme.” Yetersiz geri dönüşüm hasarlı bileşenlerin birikmesine yol açar; aşırı geri dönüşüm ise hücrenin kendi kendini yemesiyle sonuçlanır. Bu çalışma, yaşlanma ve hastalık için büyük çıkarımları olan, aldatıcı derecede basit bir soruyu soruyor: canlı bir hücre, besinler azalıp arttıkça otofajiyi doğru zamanlarda nasıl açıp kapatıyor?
Binlerce Hücreyi Bir Şölen‑Kıtlık Döngüsü Boyunca İzlemek
Bunu ele almak için araştırmacılar model olarak bira mayasını kullandılar ve açlık ve toparlanma sürecinden geçen yaklaşık altı bin farklı mutant baskı izlediler. Her maya baskısı otofajiyle ilişkili yapıların işaretlendiği floresan etiketler taşıyordu; böylece güçlü bir mikroskop, besinler giderilip sonra geri verilirken her saat görüntü alabiliyordu. Bu görüntüleri elle sınıflandırmak yerine ekip, bir hücrenin görüntü özelliklerine dayanarak otofajik durumda olup olmadığını tanıması için derin öğrenme algoritmaları eğitti; insan yargısından bağımsız olarak. Bu, neredeyse tüm maya genomu için otofaji aktivitesinin hassas zaman seyirlerini üretti ve her mutantın besin değişimlerine ne kadar hızlı ve güçlü yanıt verdiğini ortaya koydu. 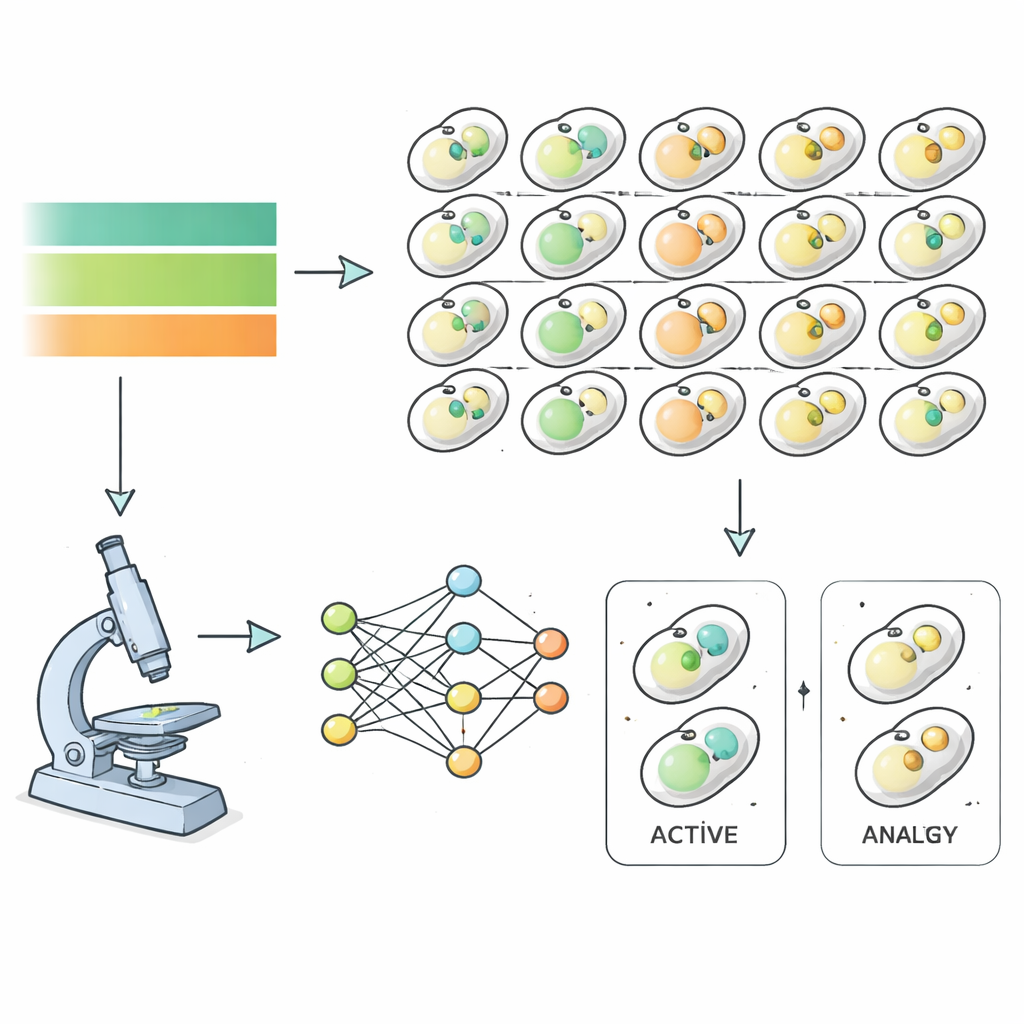
Hücrelerin Geri Dönüşümü Yanlış Yürüttüğü Altı Farklı Yol
Bu zaman seyirlerini matematiksel olarak sığdırarak, yazarlar her mutant için ayrıntılı “kinetik parmak izleri” çıkardı—otofajinin ne kadar hızlı açıldığı, ne kadar süre yüksek kaldığı ve ne kadar keskin kapandığı. Bu imzaları gruplayınca altı geniş davranış tipi ortaya çıktı. Bazı mutantlar açlık ve besin geri dönüşüne çok hızlı yanıt veren “ultra duyarlı”ydı. Diğerleri “hipoduyarlı” olarak yavaş tepki veriyordu. Bir “hiperaktif” grup anormal derecede yüksek temel geri dönüşüm gösterirken, birkaç grup uygun bir yanıt oluşturmakta çeşitli derecelerde başarısız oldu. Önemli olarak, bilinen çekirdek otofaji genleri en şiddetli sınıflara düştü; bu da yöntemin ölçüm gürültüsü yerine gerçek biyolojiyi yakaladığını doğruluyor.
Otofaji Üzerindeki Kontrolün Hiyerarşisini Haritalamak
Otofaji izolasyonda gerçekleşmez; hücrenin daha geniş düzenleyici ağlarına entegre edilmiştir. Ekip dinamik profillerini maya içindeki genetik ve protein etkileşimlerinin büyük haritalarının üzerine yerleştirdi. Kaybı güçlü otofaji kusurlarına yol açan genler, bu ağlarda bilinen otofaji “çekirdek makinasına” yakın olma eğilimindeydi; daha ince etkiler gösteren mutantlar ise daha uzaktaydı; bu, daha dolaylı yönetime işaret ediyor. Her davranış sınıfında hangi hücresel süreçlerin zenginleştiğini inceleyerek, açılmanın RNA, protein üretimi ve enerji metabolizmasıyla ilgili yollar tarafından güçlü şekilde şekillendirildiğini; besinler geri geldiğinde otofajiyi kapatmanın ise geri dönüşüm veziküllerini temizleyen membran trafiği ve füzyon adımlarına daha çok bağımlı olduğunu buldular.
Veziküllerin Nasıl Oluştuğu ve Temizlendiğine Yakından Bakmak
Otofaji iki ana aşamadan geçer: yük dolu veziküllerin inşası ve ardından bunların yıkım için hücrenin geri dönüşüm kompartmanıyla füzyonu. Bu aşamaları ayrıştırmak için araştırmacılar, sinir ağlarının içindeki “latent alanı”—görüntüleri ayırt etmek için kullandığı sıkıştırılmış temsili—araştırdılar. Bu iç temsili iki boyutlu bir haritaya projekte ederek, hücre popülasyonlarının vezikül olmayan bir bölgeden çok sayıda serbest vezikül içeren bir bölgeye ve nihayetinde veziküllerin temizlendiği bir bölgeye nasıl geçtiğini görebildiler. Farklı aşamalarda kilitlenmiş referans mutantlarla istatistiksel karşılaştırmalar kullanarak, her genin esas olarak vezikül oluşumunu, vezikül temizliğini veya her ikisini etkileyip etkilemediğini nicelendirdiler. Bu analiz, vezikül oluşumunun zaman içinde nitrojen düzeylerine karşı son derece duyarlı olduğunu, oysa temizleme mekanizmasının daha istikrarlı davrandığını ve genellikle genel geri dönüşüm akışının başlıca sınırlayıcısı olduğunu gösterdi. 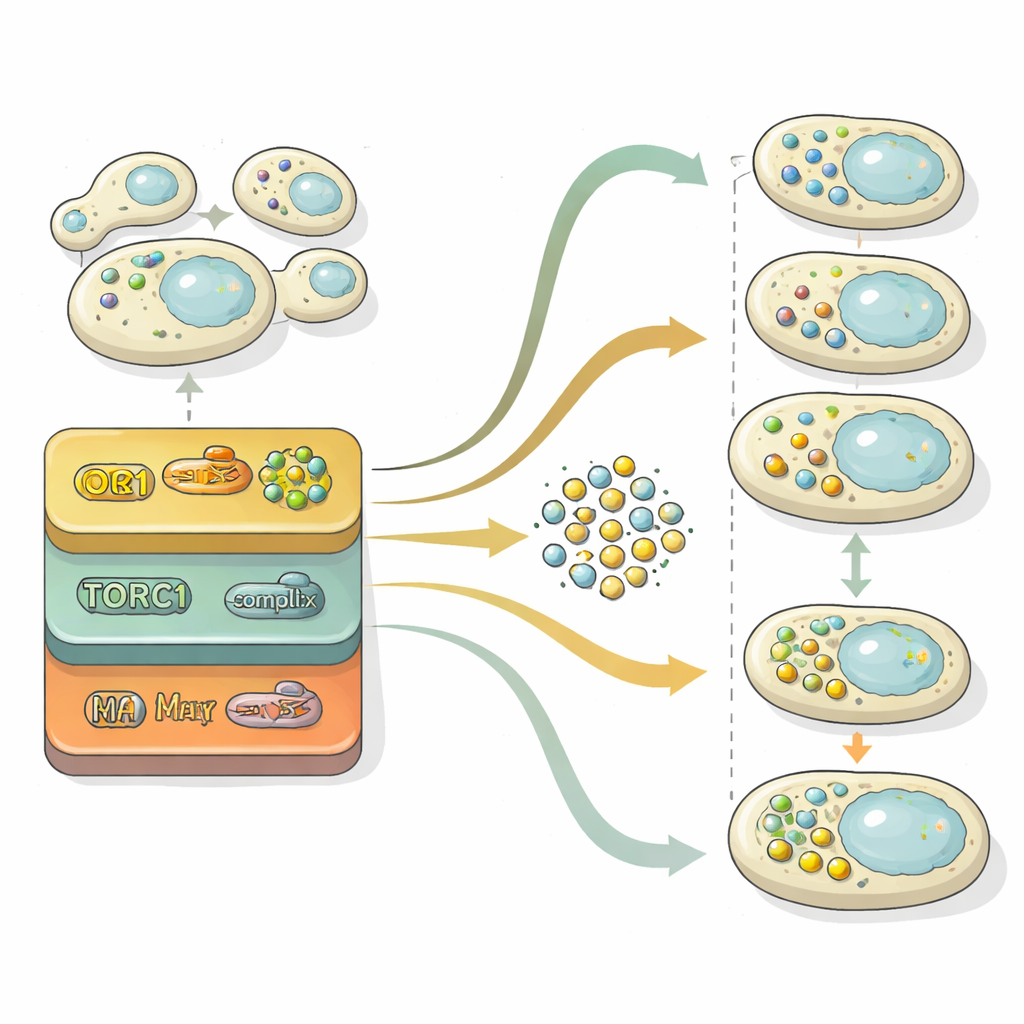
Geri Dönüşüm Üzerinde Gizli Bir Fren: Retrograd Yol
En çarpıcı keşiflerden biri, mitokondrilerden çekirdeğe sinyal ileten sözde retrograd (RTG) yoluyla ilgiliydi. RTG bileşenlerinden yoksun maya hücreleri, besinler bol olsa bile fazla sayıda otofagosom üretti ve besinler geri geldiğinde bunları temizlemede zorlandı. Ayrıntılı takip deneyleri, bu yolun özellikle başlatıcı anahtar ATG1 olmak üzere bazı ana otofaji genlerinin ekspresyonunu kontrol ettiğini ve bunun büyük ölçüde rapamisin gibi ilaçların hedef aldığı iyi bilinen TORC1 besin sensöründen bağımsız olduğunu gösterdi. Etkili olarak, RTG sinyali zengin koşullarda kontrolsüz otofajiyi önleyen ve koşullar iyileştiğinde yanıtın sonlanmasına yardımcı olan zamanla değişen bir fren görevi görüyor.
Sağlık ve Terapi İçin Neden Önemli
Toplu halde bu çalışma, hücrelerin değişen besin koşullarında otofajiyi nasıl ayarladıklarına dair genom çapında, zaman çözünürlüklü bir harita sunuyor. Açılma ve kapanmanın ayna görüntüleri olmadığını ortaya koyuyor: geri dönüşümün nasıl başladığını etkileyen gen sayısı, nasıl durduğunu etkileyenlere göre çok daha fazla ve uzun vadeli denge büyük ölçüde vezikül temizliği ve RTG yolu gibi transkripsiyonel frenlere bağlı. Genel okuyucu için çıkarım şu: hücresel öz‑kanibalizm katmanlı, hiyerarşik kontrol altındadır ve artık bu katmanları yüksek hassasiyetle haritalayabiliyoruz. Bu tür bir sistem düzeyi bakış, sonunda otofajiyi belirli aşamalarda ayarlayan daha nüanslı tedavilere rehberlik edebilir—yararlı geri dönüşümü güçlendirirken kronik, kontrolsüz öz‑sindirimin zararlı etkilerini tetiklememek için.
Atıf: Chica, N., Andersen, A.N., Orellana-Muñoz, S. et al. Time-resolved functional genomics using deep learning reveals global hierarchical control of autophagy. Nat Cell Biol 28, 465–479 (2026). https://doi.org/10.1038/s41556-025-01837-0
Anahtar kelimeler: otofaji, derin öğrenme, mayası genetiği, besin algılama, hücresel geri dönüşüm