Clear Sky Science · tr
Aşı yanıtlarının ayrıntılı fenotiplendirilmesi, nötralize edici antikor heterojenliğinin transkriptomik belirleyicilerini ortaya koyuyor
Bazı aşıların belirli kişilerde neden daha iyi çalıştığı
COVID-19 aşısı olmak için kolumu sıvadığımızda, herkesin bağışıklık sisteminin aynı şekilde tepki verdiğini varsayabiliriz. Gerçekte ise insanlar, koruyucu antikorları ne kadar hızlı ve güçlü biçimde geliştirdikleri açısından büyük farklılıklar gösterir. Bu çalışma, inaktive SARS-CoV-2 aşıları alan yetişkinleri izledi ve aşı yanıtlarının, her biri genlerimizde ve kan hücrelerimizdeki erken bağışıklık sinyalleriyle yönlendirilen ayrı desenlere ayrıldığını gösteriyor. Bu desenleri anlamak, bir gün aşı takvimlerini kişiye özel olacak şekilde ayarlayarak herkesin ihtiyaç duyduğu korumayı almasına yardımcı olabilir.
Aynı aşıdan sonra korunmaya giden üç yol
Araştırmacılar, iki doz inaktive COVID-19 aşısı alan 73 sağlıklı yetişkini izledi. Nötralize edici antikorları —virüsü engelleyebilenleri— aşılamadan önce, ikinci dozdan bir hafta sonra ve yaklaşık bir ay sonra ölçtüler. İnsanları basitçe “yüksek” ve “düşük” yanıt verenler olarak ayırmak yerine, antikor seviyelerinin zaman içindeki değişimine göre veri odaklı yöntemlerle gruplandırdılar. Üç belirgin desen ortaya çıktı: antikorları yavaş ve ılımlı şekilde artan “düşük-gecikmiş” grup; antikorları hızla yükselip sonra dengelenen “hızlı-dengeleyen” grup; ve antikorları en yüksek düzeylere kadar sürekli artan “sürekli-artış” grubu. Bu desenler yaş, cinsiyet veya vücut ağırlığı ile açıklanmıyor; hangi inaktive aşı markasının kullanıldığı ise ancak kısmen etkiliydi.
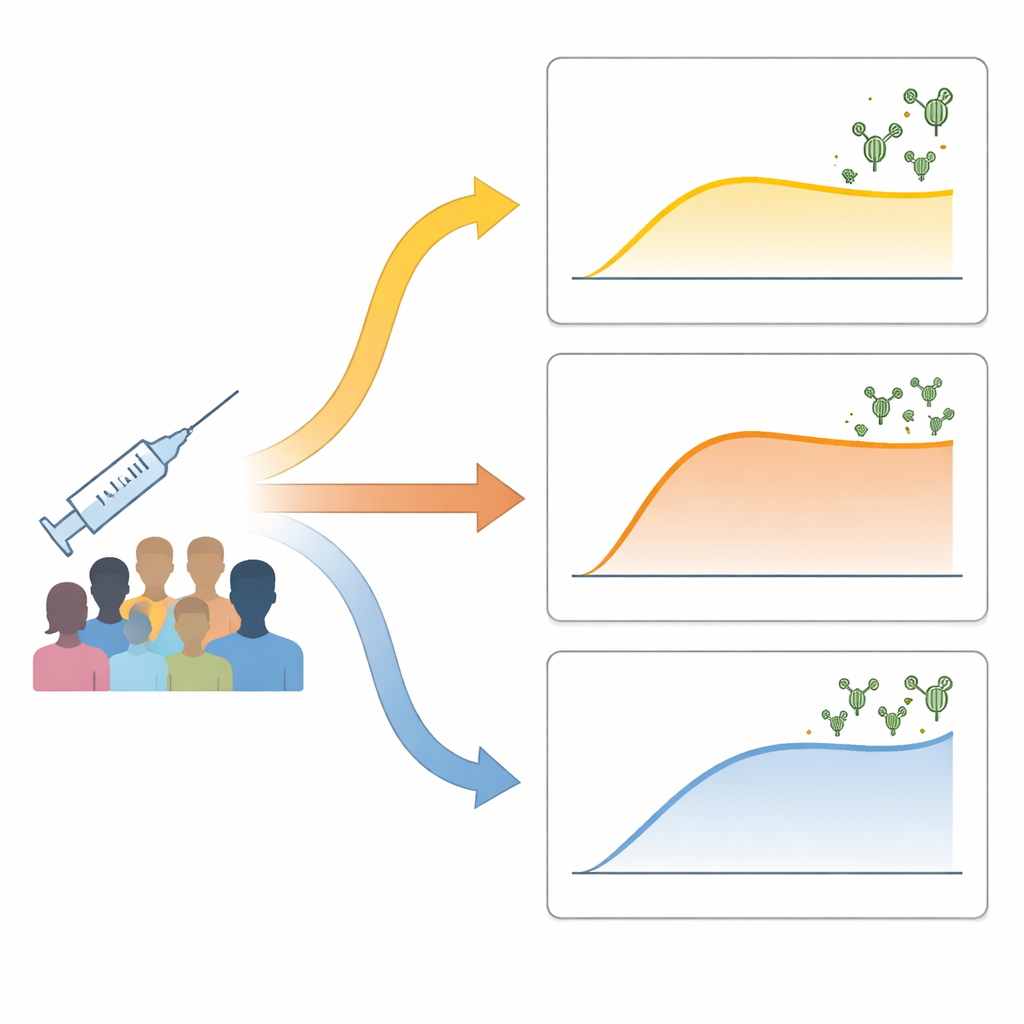
Erken bağışıklık etkinliği sonucun nasıl şekillendirdiği
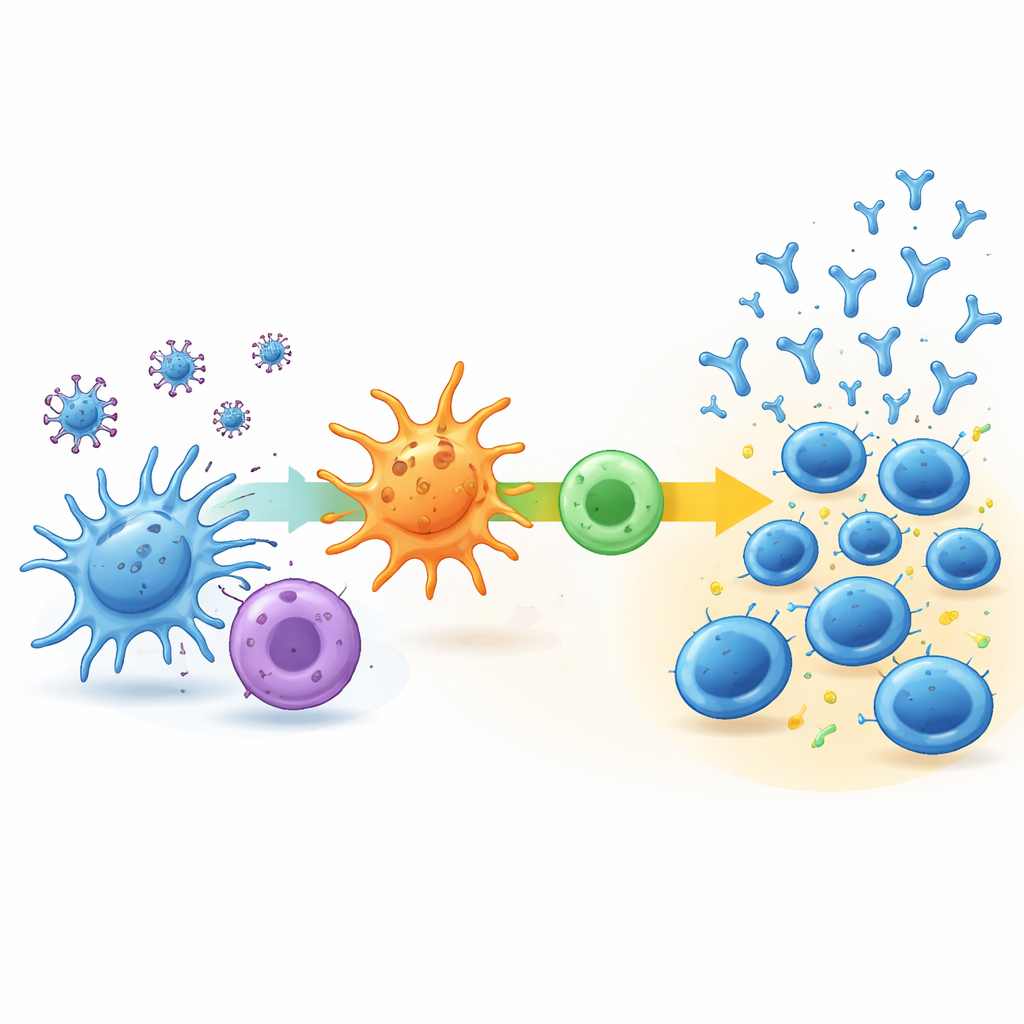
Bu farklı yolları neyin yönlendirdiğini öğrenmek için ekip, kan içindeki bağışıklık hücrelerinin genetik etkinliğini başlangıçta ve ikinci dozdan bir hafta sonra analiz etti. Düşük-gecikmiş grupta çok az değişiklik oldu: temel bağışıklık yolakları neredeyse açılmadı ve kanda bulunan bağışıklık hücresi tipi karışımı büyük ölçüde aynı kaldı. Buna karşılık, hızlı-dengeleyen ve sürekli-artış grupları erken bağışıklık aktivasyonunun açık işaretlerini gösterdi. En güçlü yanıt verenlerde, viral parçaları işleyen, bunları diğer bağışıklık hücrelerine sunan ve antikor üretimini artırdığı bilinen bir yardımcı T hücresi tepkisini destekleyen yolaklarda koordine aktivite vardı. Bu kişiler ayrıca yanıt vermeye hazır daha fazla naïf B hücresi ve yardımcı T hücresine sahip olma eğilimindeydi ve daha sonra biraz daha güçlü virüse özgü T hücre aktivitesi gösterdiler.
RNA ve B hücrelerinde gizli kontrol katmanları
Basit gen açma–kapama değişikliklerinin ötesinde, bilim insanları DNA ile protein arasındaki ara moleküller olan RNA’da gömülü daha ince düzenleme katmanlarına baktı. En üst yanıt veren grupta, virüs parçalarını bağışıklık sistemine sunan bağışıklık genleri farklı “splicing” desenleri ve RNA’larının sonundaki daha kısa kuyruk bölümleri gösterdi. Bu özelliklerin belirli proteinlerin üretilmesini kolaylaştırdığı ve güçlü sinyal iletimini sürdürdüğü düşünülüyor. Ekip ayrıca aynı kan örneklerinden B hücre reseptörlerinin repertuarını —antikor üreten hücrelerin benzersiz antenlerini— yeniden yapılandırdı. Genel çeşitlilik gruplar arasında benzer görünse de, her yanıt deseni bu reseptörlerin biraz farklı kombinasyonlarını ve biçimlerini kullandı; en güçlü yanıt verenler koronavirüs spike proteininin güçlü antikorlarıyla daha önce ilişkilendirilmiş reseptör türlerini tercih etti.
Aşılamadan önce muhtemel düşük yanıt verenleri tespit etmek
Düşük-gecikmiş gruptaki kişilerin standart aşı takviminden sonra daha az korunmuş olabileceğinden, araştırmacılar bunları önceden işaretlemenin mümkün olup olmadığını sordu. En zayıf ve en güçlü yanıt verenler arasında başlangıçta ılımlı farklılık gösteren küçük bir gen setine odaklandılar. Makine öğrenimi yöntemleri kullanarak, aşılamadan önce ölçülen yalnızca sekiz genin etkinliğine dayanan bir model kurdular. Bu model, veri setlerinde düşük-gecikmiş yanıt verenleri yüksek doğrulukla ayırt edebildi; temel hücre sinyalleşmesi ve iltihaplanmayla ilgili iki gen en fazla öngörü gücüne katkıda bulundu. Bu çalışmanın daha büyük ve daha çeşitli gruplarda test edilmesi gerekse de, basit bir kan testinin bir gün daha kişiselleştirilmiş aşı planlarına rehberlik edebileceğini düşündürüyor.
Gelecek aşılar için bunun anlamı
Genel olarak bu çalışma, insanların basitçe “güçlü” veya “zayıf” antikor yanıtları vermediğini; erken, zor görülen bağışıklık olayları tarafından şekillendirilen farklı zaman seyirlerini izlediklerini gösteriyor. En korunmuş bireyler, aşıyı hızla tanımalarına ve kalıcı antikorlar oluşturmalarına yardımcı olan koordine gen ve hücre ağlarını devreye sokarken, düşük yanıt verenler sönük bir erken reaksiyon sergiliyor. Bu iç farklılıkları haritalayarak ve kimin zayıf yanıt vereceğini öngören araçlar geliştirerek, çalışma risk altındaki bireyler için daha erken takviyeler veya alternatif formülasyonlar gibi kişiselleştirilmiş aşılamanın temelini atıyor; böylece aşıların vaadi daha dengeli bir şekilde paylaşılabilir.
Atıf: Wu, Q., Hu, H., Qin, L. et al. Refined phenotyping of vaccine responses reveals transcriptomic determinants of neutralizing antibody heterogeneity. npj Vaccines 11, 61 (2026). https://doi.org/10.1038/s41541-026-01386-z
Anahtar kelimeler: aşı yanıtları, nötralize edici antikorlar, COVID-19 aşılaması, bağışıklıkte heterojenlik, kişiselleştirilmiş aşılar