Clear Sky Science · tr
Antijen çapraz sunumunu güçlendirerek T hücresi genişlemesini sağlayan ve anti‑PD‑1 ile sinerji gösteren kanser aşı adjuvanı
Bağışıklık Sistemini Hassas Bir Tümör Savaşçısına Dönüştürme
Kanser aşıları genellikle bağışıklık sistemine tümörleri tanıyıp yok etmeyi öğretmek olarak tanımlanır, ancak uygulamada bu vaadi nadiren yerine getirmişlerdir. Bu çalışma, bu tür aşıları “süper şarj” ederek daha güçlü, daha uzun süre dayanabilen öldürücü T hücreleri oluşturabilmelerini ve anti‑PD‑1 gibi yaygın immünoterapi ilaçlarıyla daha iyi işbirliği yapabilmelerini sağlayan yeni bir yolu araştırıyor. Yarınki kanser tedavilerinin biyolojik ilaçlar, aşılar ve bağışıklık mühendisliğini nasıl birleştirebileceğiyle ilgilenen okurlar için bu çalışma, bir sonraki nesil, hedefe yönelik immünoterapinin nasıl görünebileceğine dair bir bakış sunuyor.
Kanser Aşılarının Daha İyi Bir Destekleyiciye İhtiyacı Var
Tedavi edici kanser aşılarının amacı hastalığı önlemek değil, halihazırda tümörü olan kişileri güçlü, tümöre özgü bağışıklık yanıtlarıyla tedavi etmektir. Kilit aktörler, tümör hücrelerinde belirgin antijenleri tanıyıp yok edebilen CD8 “öldürücü” T hücreleridir. Ne yazık ki tümör antijenleri, çoğunlukla vücudun kendi proteinlerinin değişmiş versiyonlarına benzediği için zayıf uyarıcıdır. Kanser gelişimi sırasında sürekli maruziyet, T hücrelerini tükenmiş veya toleran hale getirebilir ve aşının etkisini azaltabilir. Bunu aşmak için aşıların, doğal bağışıklık sistemini uyaran, antijen sunumunu iyileştiren ve büyük, dayanıklı bir tümöre özgü T hücresi havuzu oluşturan adjuvanlarla—yardımcı bileşenlerle—eşleştirilmesi gerekir.
İki Güçlü Sinyalden Oluşan Hibrit Bir Bağışıklık Güçlendirici
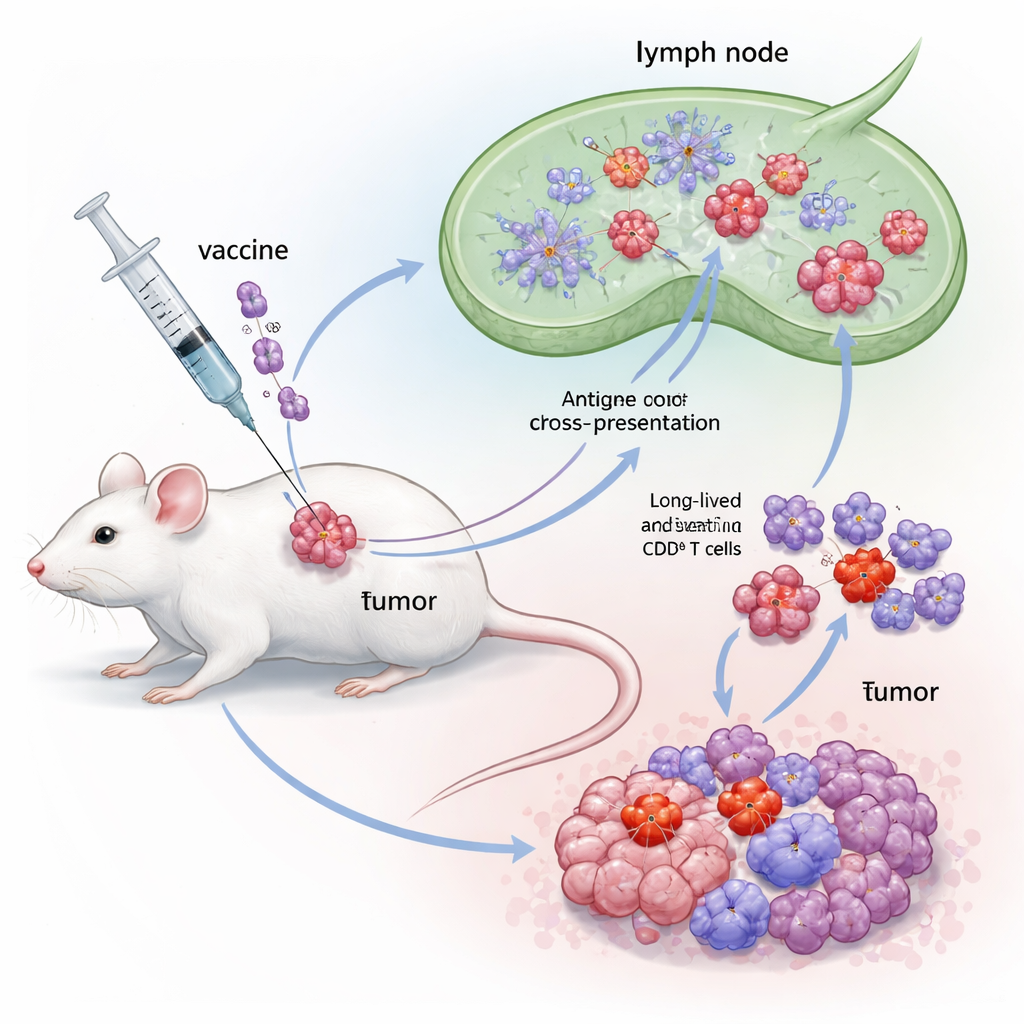
Araştırmacılar, iki immün‑uyarıcı molekülü tek bir proteine birleştirerek Flt3L‑FlaB veya kısaca FB adını verdikleri hibrit bir adjuvan tasarladı. Bir yarısı, Flt3L, cDC1 olarak bilinen özelleşmiş bir dendritik hücre grubunu genişleten doğal bir büyüme faktörüdür. Bu hücreler “çapraz‑sunum” konusunda üstündür—tümör materyalinden parçaları alıp CD8 T hücrelerine güçlü yanıtlar tetikleyecek şekilde sunarlar. Diğer yarısı, FlaB, TLR5 adlı bir innat sensörü aktive eden ve güçlü bir tehlike sinyali işlevi gören bakteriyel bir flagellin fragmanıdır. Bunları birbirine bağlayarak yazarlar, hem cDC1 hücrelerini genişletmeyi hem de bunları yüksek derecede aktif bir duruma geçirmeyi, böylece tümör antijenlerinin T hücrelerine sunulmasını ve bu uyarının süresini iyileştirmeyi hedeflediler.
Yeni Adjuvanın Tümör Modellerinde Test Edilmesi
FB’yi test etmek için ekip, insan papilloma virüsü (HPV) kaynaklı kanserojen proteinler taşıyacak şekilde genetik olarak değiştirilmiş hücrelere dayanan iyi kurulmuş bir fare tümör modeli kullandı. Farelere önce küçük bir tümör implante edildi, ardından HPV E7 antijeni içeren terapötik bir aşı verildi; bu aşı ya yalnız Flt3L, yalnız FlaB veya yeni FB füzyonuyla birlikte uygulandı. Tüm aşılar tümöre yakın verildi. Her tek adjuvan tümör büyümesini bir miktar yavaşlatırken, FB tabanlı aşı öne çıktı: tümör ilerlemesini çok daha fazla geciktirdi, sağkalımı belirgin şekilde uzattı ve dikkate değer bir fare kesiminde tümörden tamamen arınma sağladı. Bağışıklık analizleri, FB aşılamasının kan, lenf düğümleri ve dalakta olağanüstü güçlü E7‑spesifik CD8 yanıtları oluşturduğunu; yüksek düzeyde interferon‑gamma ve güçlü T hücresi proliferasyonu gösterdiğini ortaya koydu—bu bulgular füzyonun yalnızca iki bileşenin etkilerini toplamadığını gösteriyor.
Kalıcı Bağışıklık Hafızası Oluşturma ve Anti–PD‑1 İçin Daha İyi Bir Eş
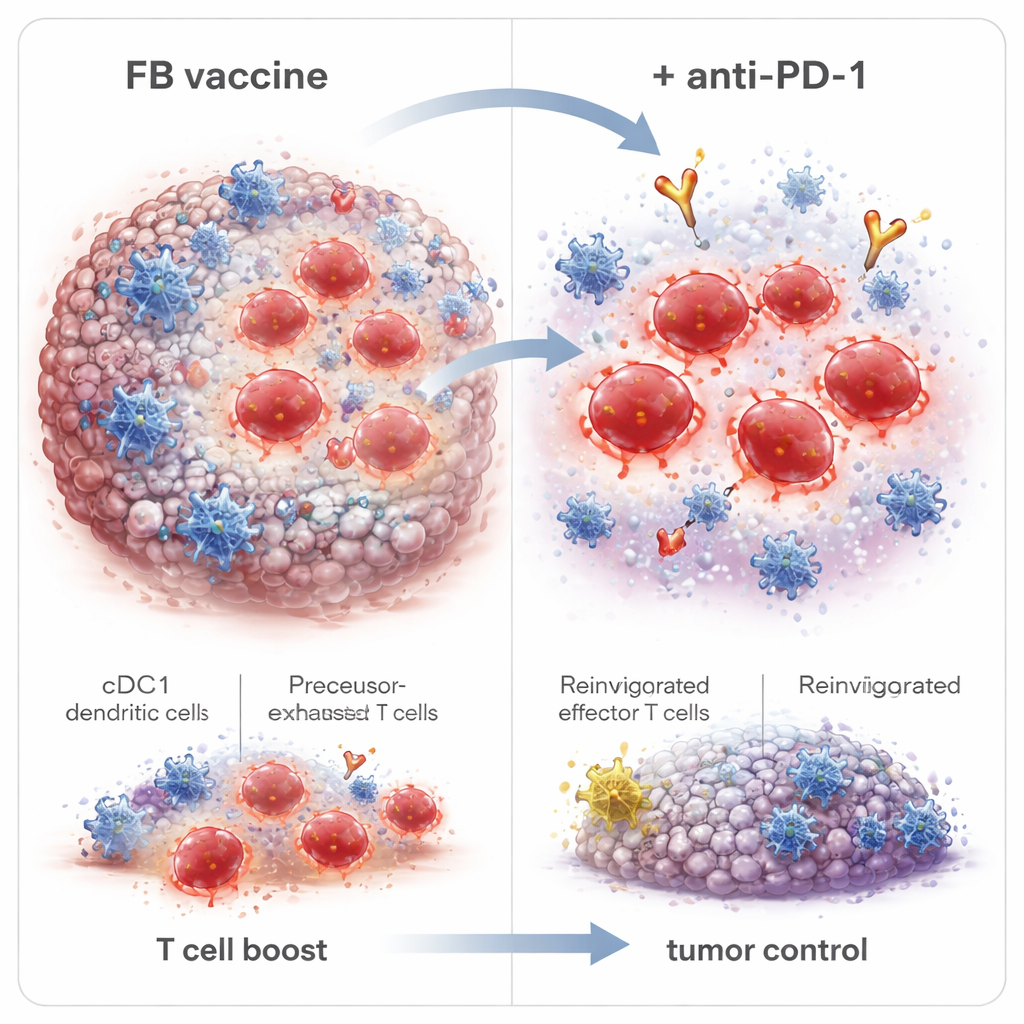
Daha derinlemesine incelendiğinde, bilim insanları FB’nin yalnızca kaç tane CD8 T hücresi ortaya çıkardığını değil, hangi türlerde değişiklik yaptığını buldular. FB, tümörlere hemen saldıran kısa ömürlü efektör hücreleri artırmanın yanı sıra ileride yanıt verebilecek olan hafıza öncüsü ve kök‑benzeri hafıza hücrelerini de güçlendirdi. Önemli olarak, FB tümörler içinde precursor‑exhausted (Tpex) adı verilen bir grubu da genişletti—tükenmişlik ile tam aktivite arasındaki sınırda bulunan ve özellikle anti‑PD‑1 ilaçlara yanıt veren hücreler. Tümör‑arılan farelere aşılamadan uzun süre sonra daha yüksek dozlarda kanser hücreleri ile meydan okunduğunda çoğu yeniden büyümeyi engelledi ve dayanıklı bağışıklık hafızası gösterdi. Lenf düğümlerinden bağışıklık hücrelerinin çıkışını bloke etmek FB’nin faydalarını ortadan kaldırdı; bu, tümör‑öldürücü T hücrelerinin cDC1 tarafından o düğümlerde hazırlandığını ve ardından tümöre göç ettiğini gösteriyor.
Birlikte Daha Güçlü: Aşılar ve Kontrol Noktası Blokajı
Anti‑PD‑1 tedavisi, zaten yanıt verebilecek bir T hücresi havuzu olduğunda en iyi şekilde çalıştığı için ekip FB‑adjuvanlı aşılamayı bir anti‑PD‑1 antikoru ile birleştirdi. HPV tümör modelinde FB aşılamasına anti‑PD‑1 eklenmesi tümör büyümesini daha da yavaşlattı, kanseri tamamen temizleyen fare sayısını artırdı ve son derece yüksek dozlu tümör yeniden meydan okumasına karşı tam koruma sağladı. Zamanlamanın ince ayarı önemliydi: anti‑PD‑1’in birinci aşı dozundan sonra değil ikinci dozdan sonra başlatılması, Tpex hücreleri genişledikten sonra beklemeye uygun olarak tam tümör eradikasyonunu kısmen iyileştirdi. FB adjuvanı ayrıca peptid‑temelli aşılara, kolorektal kanser modelinde tümöre özgü neoantijenlere verilen yanıtları da geliştirdi; bu da bu stratejinin HPV ilişkili hastalıkların ötesinde genişçe uygulanabileceğini düşündürüyor.
Geleceğin Kanser Bakımı İçin Ne Anlama Gelebilir
Uzman olmayanlar için ana mesaj, bu çalışmanın bağışıklık sistemine kanserle savaşmayı “öğretme” biçimini rafine etmesidir. Bir dendritik hücre büyüme faktörünü güçlü bir tehlike sinyaliyle tek, kararlı bir proteinde birleştiren FB adjuvanı, doğru antijen sunan hücrelerden daha çok oluşturur, bunların tümör antijenlerini daha etkili göstermesine yardımcı olur ve hem şimdi güçlü hem de daha sonra kontrol noktası terapisine yanıt vermeye hazır bir öldürücü T hücresi popülasyonu şekillendirir. Bu sonuçlar farelerde elde edilmiş olup insan kullanımına geçmeden önce daha birçok adım gerekmekle birlikte çalışma, çapraz‑sunumu ve T hücresi kökenselliğini yöneten daha akıllı adjuvanların terapötik kanser aşılarını anti‑PD‑1 gibi ilaçlar için çok daha güçlü bir ortak haline getirebileceğine ve hastalarda daha derin, daha uzun süreli tümör kontrolüne yol açabileceğine dair net bir yol haritası sunuyor.
Atıf: Dang, G.C., Loeurng, V., Pa, P. et al. Antigen cross-presentation potentiating cancer vaccine adjuvant for T cell expansion and synergy with anti-PD-1. npj Vaccines 11, 56 (2026). https://doi.org/10.1038/s41541-026-01376-1
Anahtar kelimeler: kanser aşıları, immünoterapi, dendritik hücreler, PD‑1 blokajı, HPV ilişkili tümörler