Clear Sky Science · tr
miR-126 inhibisyonu ile miyeloblastik lösemide vasküler niş kaynaklı TKI direncinin aşılması
Kanser hastaları için neden önemli
Akut miyeloid lösemi (AML), en agresif kan kanserlerinden biridir ve modern hedefe yönelik ilaçlara rağmen birçok hasta nüks eder. Bu çalışma, sonuçları büyük olabilecek görsel olarak basit bir soruyu ele alıyor: sorun yalnızca kanser hücrelerinin kendisi mi, yoksa kemik iliğindeki “mahalleleri” mi? Laboratuvar verilerine dayanan ayrıntılı bir bilgisayar modeli kurarak, yazarlar küçük kan damarlarının lösemi kök hücrelerini ilaçlardan nasıl koruyabildiğini ve tek bir küçük RNA sinyalinin engellenmesinin bu korumayı nasıl dağıtabileceğini araştırıyorlar.
Kemik iliğindeki gizli sığınak
AML, kötü huylu blast hücrelerinin normal kan üretimini bastırdığı kemik iliğinde ortaya çıkar. Bu sürü içinde, kendini yenileyebilen ve tedaviye direnebilen daha küçük bir lösemi kök hücresi popülasyonu gizlenir ve nüksü başlatır. Bu kök hücreler serbestçe yüzmez; küçük arterler ve kılcal damarların çevresindeki özelleşmiş ceplere, topluca vasküler niş olarak bilinen bölgelere yerleşirler. Çalışma, lösemi hücreleri FLT3-ITD mutasyonları taşıyan hastalara odaklanıyor; bu hücreler tirozin kinaz inhibitörleri (TKI) ile tedavi edilir. Bu ilaçlar tümör yükünü keskin biçimde azaltabilse de, birçok hasta yine nüks eder; bu da bazı hücrelerin saklanıyor veya korunuyor olabileceğini düşündürür.
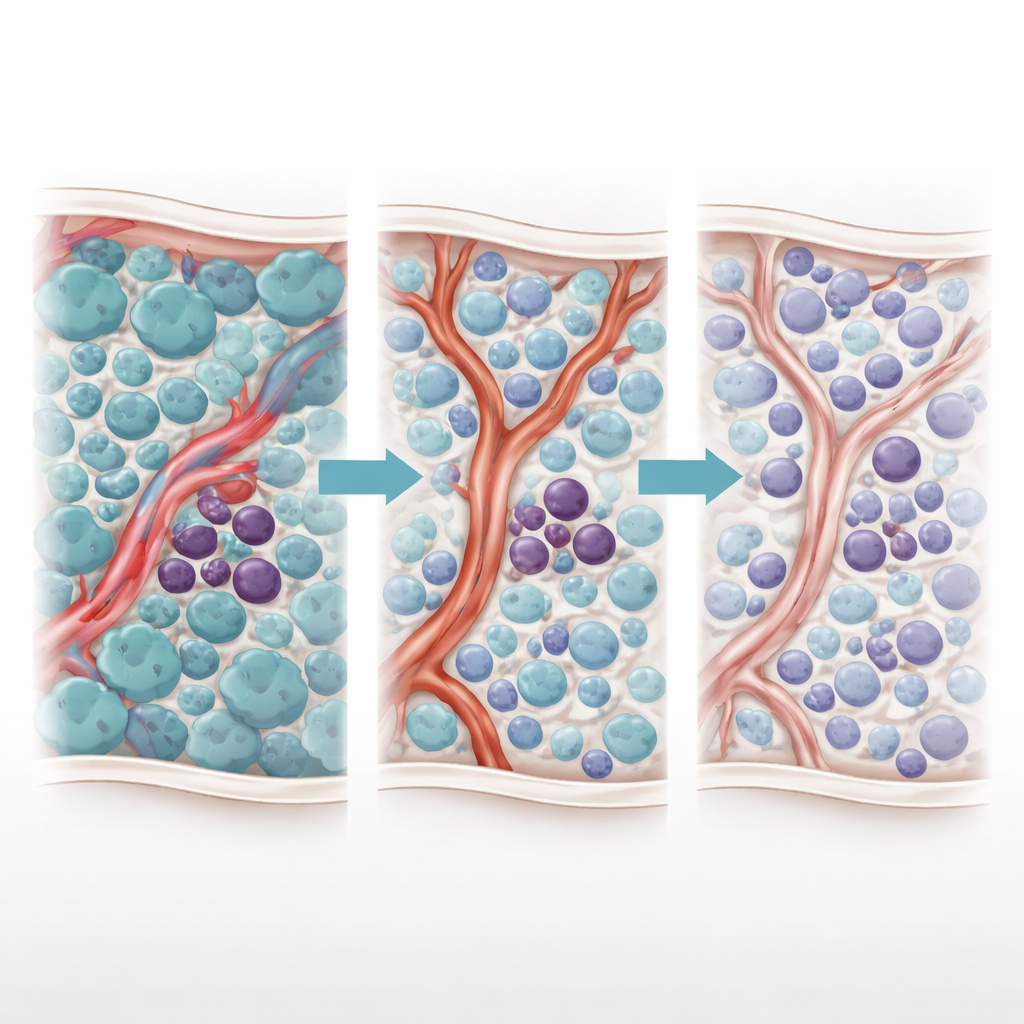
İki yüzlü bir tedavi etkisi
Yazarlar daha önce kafa karıştırıcı bir “Janus olgusu” keşfetmişlerdi—TKI tedavisine karşı iki yüzlü bir tepki. TKI’lar hızla bölünen blast hücreleri öldürürken, inflamatuvar bir molekül olan TNF-α düzeyleri düşer. Bu düşüş beklenmedik bir şekilde çevredeki damar hücrelerinin küçük bir düzenleyici RNA olan miR-126 üretimini artırmasına izin verir. Bu miR-126, endotel hücrelerinden lösemi kök hücrelerine aktarılır ve onları sessiz, bölünmeyen bir duruma iterek yüksek düzeyde ilaç direnci kazandırır. Başka bir deyişle, çoğu kanser hücresini yok eden tedavi, en tehlikelilerini barındıracak şekilde kemik iliğini yeniden şekillendirir.
Sanal bir kemik iliği inşa etmek
Bu dinamiği çözmek için ekip, AML kemik iliğinin ajan tabanlı bir hesaplamalı modelini oluşturdu. Her ana aktör—blast hücreleri, lösemi kök hücreleri ve damarları döşeyen endotel hücreleri—biyolojik olarak bilgilendirilmiş kuralları izleyen bireysel bir “ajan” olarak temsil edildi. TNF-α, miR-126, TKI AC220 ve miR-126’yi bloke eden miRisten adlı ilacın difüze olması simüle edilmiş dokuda yayıldı. Model, miR-126 üreten damarların zengin veya fakir olduğu alanları içeren gerçek vasküler desenleri haritalayan fare görüntüleme verileriyle kalibre edildi. Simülasyonlarda, standart TKI tedavisi Janus etkisini güvenilir şekilde yeniden üretti: blastler azaldı, TNF-α düştü, damarlardan kaynaklanan miR-126 artışı oldu, kök hücreler koruyucu nişlere çekildi ve hastalık daha sonra geri döndü.
Kalkanı hassas zamanlama ile kapatmak
Bu sanal sistemle donanan araştırmacılar, kısır döngüyü kırmanın yollarını test ettiler. miRisten’i TKI ile eş zamanlı eklemek yardımcı oldu ama modelde nadiren hastalığı tamamen iyileştirdi. Daha stratejik bir yaklaşım daha etkiliydi: vasküler miR-126’yı azaltmak için yalnızca miRisten ile kısa bir “ön tedavi”, ardından ya tek başına TKI ya da devam eden kombinasyon tedavisi. Birçok simüle edilmiş vasküler düzen içinde, AC220 başlamadan önce sadece birkaç günlük miRisten ön tedavisi bile nüksü dramatik biçimde azalttı veya ortadan kaldırdı ve toplam ilaç maruziyetini sınırladı. Model ayrıca lösemi kök hücrelerinin damarlara ne kadar yakın oturduğunun kaderlerini güçlü şekilde etkilediğini gösterdi—doğrudan damarların kenarına yaslanan hücreler en büyük korumayı kazanıyor, ta ki miR-126 bloke edilene kadar.
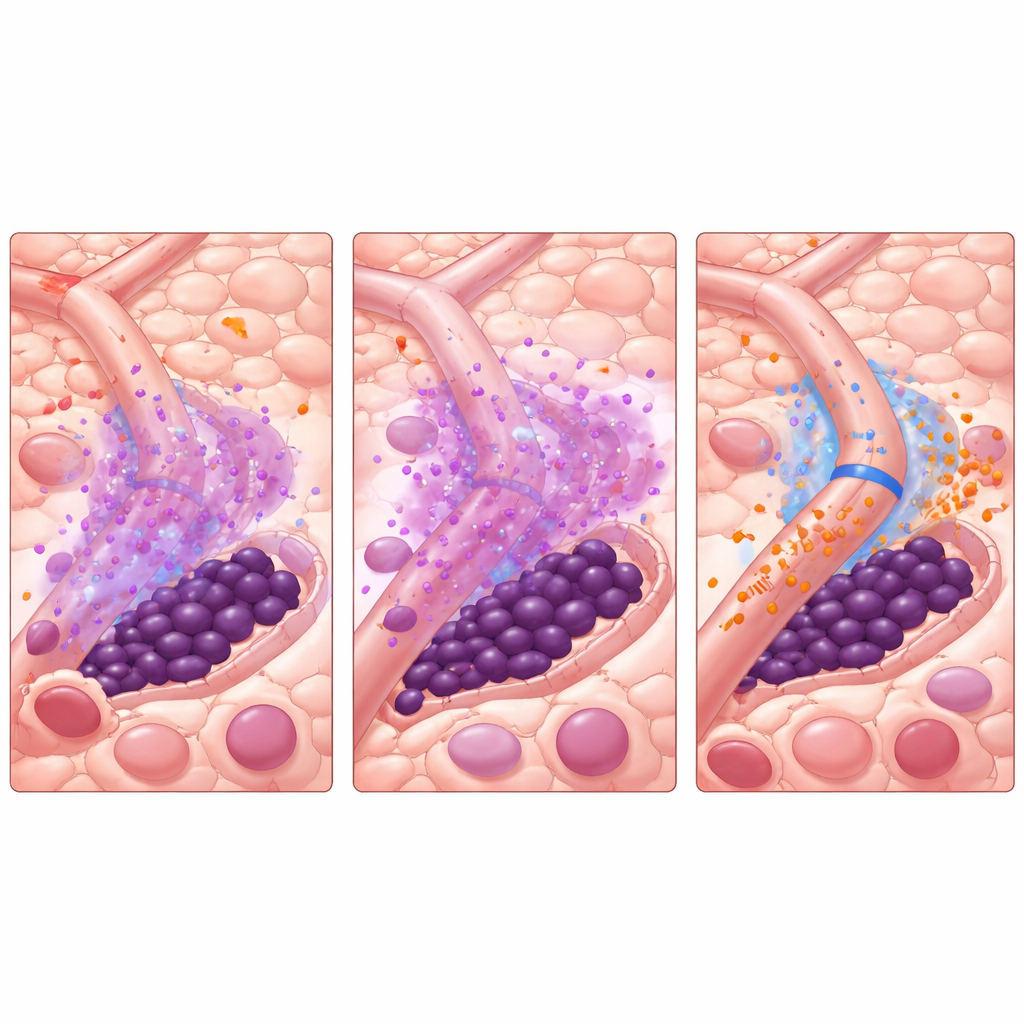
Gelecekteki bakım için ne anlama gelebilir
Basitçe söylemek gerekirse, çalışma bazı lösemi kök hücrelerinin TKI’ların zayıf olmasından değil, kemik iliğinin küçük kan damarlarının tedavi sırasında geçici olarak “koruyucu” moda geçmesinden hayatta kaldığını öne sürüyor. Mevcut TKI’yı vermeden önce kısa süreli olarak tek bir sinyal olan miR-126’yı kapatarak, bu kalkanı soymak, kök hücreleri saklandıkları yerden çıkarmak ve onları mevcut ilaçlarla öldürülebilir hale getirmek mümkün olabilir. Bu çalışma laboratuvar verilerine dayanan bilgisayar simülasyonlarına dayanıyor—henüz klinik denemelerde doğrulanmadı—ancak somut bir strateji sunuyor: mikroçevreyi hedef alan bir ilacı standart tedaviden hemen önce ve tedavi sırasında zamanlamak. Doğrulanırsa, bu yaklaşım sadece FLT3-mutant AML’li hastaların sonuçlarını iyileştirmekle kalmayıp, tümörün mahalleleri tedaviden kaçmasına yardımcı olan diğer hematolojik ve solid kanserlerde benzer taktiklere ilham verebilir.
Atıf: Froid, M., Branciamore, S., Chen, Z. et al. Overcoming vascular niche–mediated TKI resistance in acute myeloid leukemia through miR-126 inhibition. npj Syst Biol Appl 12, 38 (2026). https://doi.org/10.1038/s41540-026-00675-6
Anahtar kelimeler: akut miyeloid lösemi, lösemi kök hücreleri, kemik iliği mikroçevresi, tirozin kinaz inhibitörü direnci, miR-126 inhibisyonu