Clear Sky Science · tr
Hücresel FBA, böbrek tümörlerinde heterojen Warburg nişlerini ve kolon kanserinde laktat tüketimini ortaya koyuyor
Tümör metabolizmasının mekânda önemi
Kanser hücreleri, tek bir tümör içinde bile birbirinin aynısı davranmaz. Bazıları kan damarlarına yakın yaşarken, bazıları yetersiz beslenen derin bölgelerdedir; bu konumlar onların yakıt elde etme ve kullanma biçimini şekillendirir. Bu çalışma, gelişmiş uzamsal gen ifadeleri verilerinden o gizli “metabolik haritayı” okumaya yönelik yeni bir yaklaşım sunuyor. Böylece yazarlar, farklı tümörlerin önemli bir molekül olan laktatı nasıl işlediğine dair şaşırtıcı desenler ortaya koyuyor ve kanserlerin sadece laktatı atık olarak dışarı verdiği klasik bakışı sorgulatıyor.
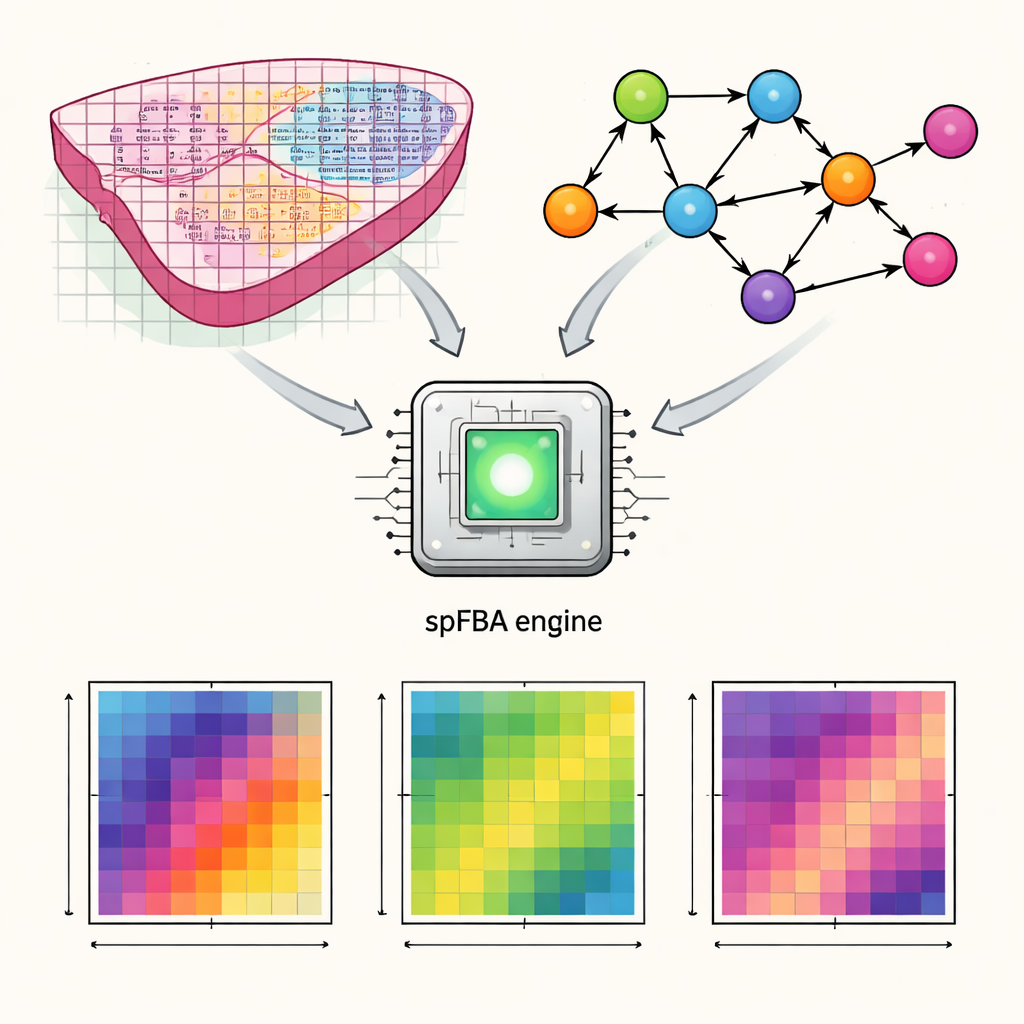
Gen haritalarını metabolik aktiviteye dönüştürmek
Yazarlar, uzamsal Akış Denge Analizi (spFBA) adını verdikleri hesaplamalı bir çerçeve geliştirdiler. Uzamsal transkriptomik teknolojiler, dokunun ince bir kesitinde binlerce küçük noktada hangi genlerin aktif olduğunu ölçer. spFBA, bu uzamsal gen etkinliği haritalarını, glukoz, oksijen ve amino asitler gibi besinlerin hücre içinde nasıl dönüştüğünü tanımlayan ayrıntılı insan metabolizması modelleriyle birleştirir. Bir dokunun her bölgesinin aynı metabolik hedefi paylaştığını varsaymak yerine, spFBA her noktayı bağımsız ele alır ve kimya yasaları ile kütle dengesi altında orada hangi reaksiyon desenlerinin mümkün olduğunu keşfeder. Çıktı, her konum için farklı metabolik reaksiyonların hangi yönde ve ne kadar güçlü akma olasılığı olduğunu gösteren bir dizi “akış zenginleştirme skoru”dur.
Böbrek tümörlerinde yöntemin denenmesi
spFBA’nın biyolojik açıdan mantıklı sonuçlar verip vermediğini görmek için ekip önce berrak hücreli böbrek hücreli karsinomu ele aldı; bu, glikoliz ve laktat salınımına güçlü biçimde dayanan bir böbrek kanseri olup Warburg etkisiyle ilişkilidir. On adet böbrek tümörü örneğine ait yayımlanmış uzamsal verileri kullanarak, tahmin edilen metabolik desenlerin doku yapısına uyup uymadığını sordular. İnfer edilen metabolik akışlara göre gruplanan noktaların, mikroskop altında görülen histolojik düzen ve yalnızca gen ifadesine dayalı kümelemelerle iyi uyum gösterdiğini buldular. Önemli olarak, spFBA tümör ile normal böbrek dokusu arasındaki beklenen metabolik farkı geri kazanıyordu: tümör bölgeleri daha yüksek glukoz kullanımı, daha güçlü biyokütle üretimi (hücre büyümesinin bir vekili) ve güçlü laktat salgılama gösteriyordu. Aynı zamanda oksijen kullanımı belirgin düzeyde kaldı; bu da aynı tümörün farklı parçalarının yerel kan teminine bağlı olarak fermantasyon ve solunumu karıştırabildiğini ortaya koydu.
Kolorektal kanserler farklı bir laktat öyküsü gösteriyor
Araştırmacılar ardından aynı iş akışını, primer kolorektal kanser ve eşleştirilmiş karaciğer metastazına ait yeni yüksek çözünürlüklü uzamsal veri setlerine ve başka bir teknolojiyle üretilmiş bağımsız bir halka açık kolorektal veri setine uyguladılar. Burada sonuçlar çarpıcı biçimde farklıydı. Laktatı atık olarak dışarı vermek yerine, çoğu kolorektal kanser bölgesinin—hem orijinal kolon tümöründe hem de karaciğer metastazlarında—çevrelerinden laktat aldığı tahmin edildi. Yakındaki destekleyici doku içindeki stromal hücreler küçük miktarlarda laktat salgılama eğilimindeyken, tümör hücreleri güçlü tüketiciler olarak hareket etti. Reaksiyon düzeyindeki akış desenlerini izleyerek yazarlar, bu metastatik hücrelerin laktatı yalnızca mitokondride sıradan enerji üreten döngüde yakmadığını gösteriyor. Bunun yerine laktatı yağ ve hücre büyümesi için gereken diğer bileşenlerin yapımına besleyen öncül maddelere dönüştürüyorlar; bu, laktatın biyosentez için hammadde haline geldiği bir “sözde ters Warburg etkisi”dir.
Metabolik nişler ve tümör-stroma sınırı
spFBA uzamsal düzeni koruduğu için belirli metabolik değiş tokuşların nerede gerçekleştiğini noktasal olarak gösterebilir. Böbrek tümörlerinde yöntem bir arada var olan metabolik “mahalleleri” ortaya koydu: hem solunum hem de fermantasyon yapan, daha iyi oksijenlenmiş, kan bakımından zengin yüzeysel arayüzler ve daha derin, kötü damarlanmış çekirdekler ki bunlar daha güçlü şekilde fermantasyona dayanıyor. Kolorektal karaciğer metastazlarında spFBA, tümör ile stroma arasındaki sınırda glutamat ve laktat işlenmesinin yön değiştirdiği keskin karşıtlıkları vurguladı; bu, invaziv ön tarafta yoğun bir alışverişe işaret ediyor. Tüm veri setlerinde, tahmin edilen büyümeyle ilişkili akışlar, bölünmeyi ölçen bağımsız gen-temelli göstergelerle koreleydi; bu da modelin biyolojik gerçekçiliğini destekliyor. Kritik olarak, aynı algoritma böbrek kanserinde laktat salgılanmasını, kolorektal kanserde ise laktat alınmasını öngördü; bu, gözlenen farkların yerleşik model yanlılığından değil veriden kaynaklandığını gösteriyor.
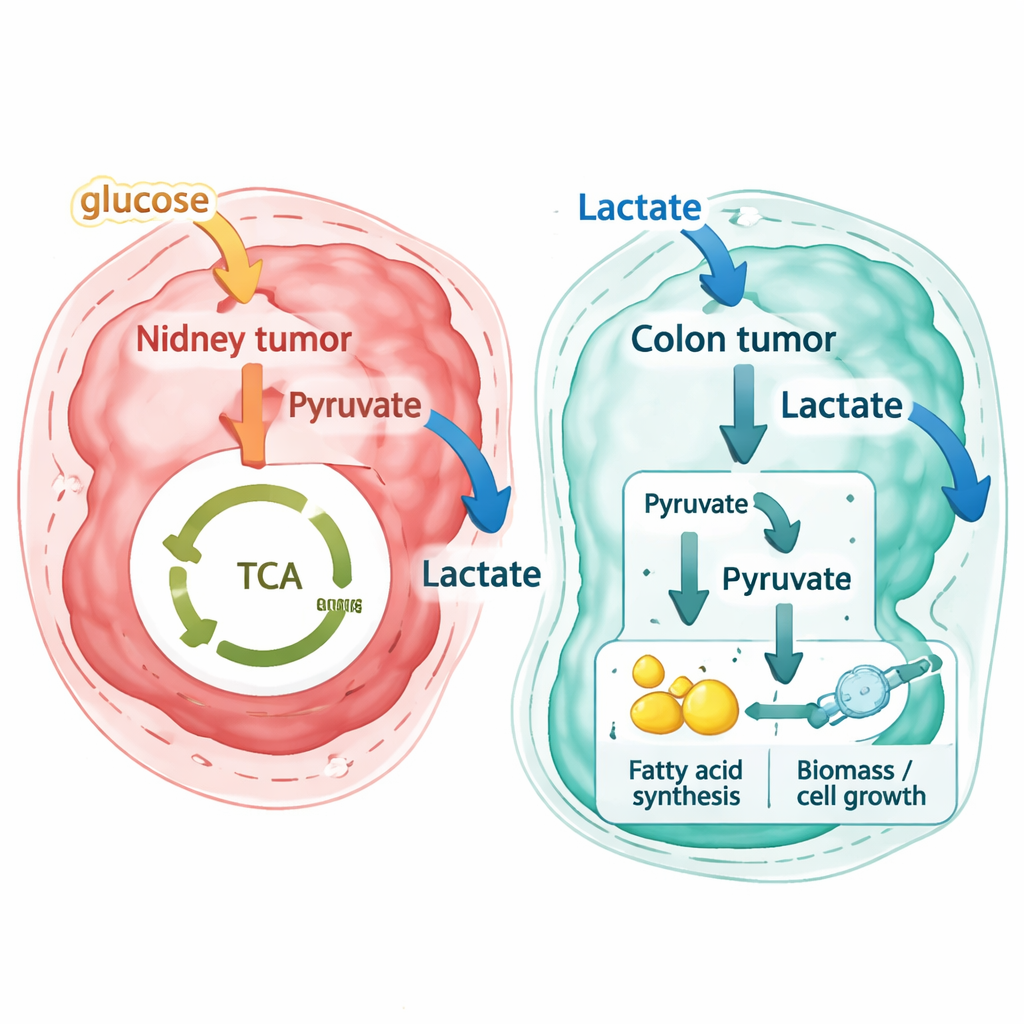
Kanseri anlama ve tedavi etme açısından bunun anlamı
Uzman olmayanlar için ana mesaj şudur: kanser metabolizması yalnızca anormal değil—ayrıca son derece yereldir. Aynı tümör birden fazla metabolik nişe ev sahipliği yapabilir ve farklı organlardaki benzer görünümlü tümörler aynı molekülleri zıt biçimlerde kullanabilir. Bu çalışma, uzamsal gen ifade verilerini ayrıntılı metabolik modellerle üst üste koyarak araştırmacıların tümörlerin hangi besinlere, örneğin laktata, muhtemelen aç olduğunu çıkarabileceğini gösteriyor. Kolorektal kanserde tümör hücrelerinin laktatı yaygın biçimde tüketip bunu büyümeyle ilişkili süreçlere yönlendirmesi, diyetin, bağırsak mikroplarının ve karaciğerin kendi metabolizmasının hastalık seyrini nasıl şekillendirdiği ve laktat kullanımının engellenmesinin bu tümörleri tedaviye karşı daha savunmasız kılıp kılamayacağı gibi yeni soruları gündeme getiriyor.
Atıf: Maspero, D., Marteletto, G., Lapi, F. et al. Spatial FBA reveals heterogeneous Warburg niches in renal tumors and lactate consumption in colorectal cancer. npj Syst Biol Appl 12, 32 (2026). https://doi.org/10.1038/s41540-026-00654-x
Anahtar kelimeler: kanser metabolizması, uzamsal transkriptomik, laktat, Warburg etkisi, kolorektal kanser