Clear Sky Science · tr
Dinamik ağ analizi, geliştirilmiş immünojenezin altında yatan pMHC arayüzünde uzun menzilli kalıntı eşleşmelerini ortaya koyuyor
Çok Küçük Viral Parçacıklar Bağışıklık Savunmamızı Nasıl Yönlendirir
Öldürücü T hücrelerimiz, enfeksiyon veya kanser belirtileri aramak için vücutta devriye gezer. Bunu, hücre yüzeylerinde MHC sınıf I molekülleri tarafından sunulan peptit adı verilen küçük protein parçacıklarını tarayarak yaparlar. Bu çalışma, ince ama önemli bir soruyu gündeme getiriyor: bu peptitlerden birindeki tek küçük değişiklik, T hücrelerinin çok daha güçlü—veya hiç—yanıt vermesini nasıl sağlayabilir? Cevap yalnızca statik yapıdan ibaret değil; tüm moleküler düzenlemenin zaman içinde nasıl hareket ettiği ve esnediğini de içeriyor.
Kilit, Anahtar ve Hareketli Parçalar
Çalışmayı anlamak için, peptit–MHC (pMHC) kompleksini bir kilit, T hücre reseptörünü (TCR) ise bir anahtar olarak hayal etmek yardımcı olur. Peptit MHC molekülündeki bir oluğa oturur ve birlikte TCR’nin yokladığı yüzeyi oluştururlar. Önceki araştırmalar, hem doğru peptit dizisinin hem de belirli MHC varyantının bir T hücresinin yanıt verip vermeyeceğini güçlü biçimde etkilediğini göstermiştir. Bilim insanları, küçük değişiklikler taşıyan ve bağışıklık yanıtlarını ayarlamak için kullanılan “değiştirilmiş peptit ligandları” da tasarlamışlardır; bunlar kanser immünoterapisinde de ilgi görmüştür. Ancak bu komplekslerin statik şekilleri hakkında çok şey bilsek de, peptitteki bir noktadaki hareketlerin TCR’nin gerçekten bağlandığı arayüzün uzak parçalarını nasıl etkilediği konusunda çok daha az şey biliyoruz.
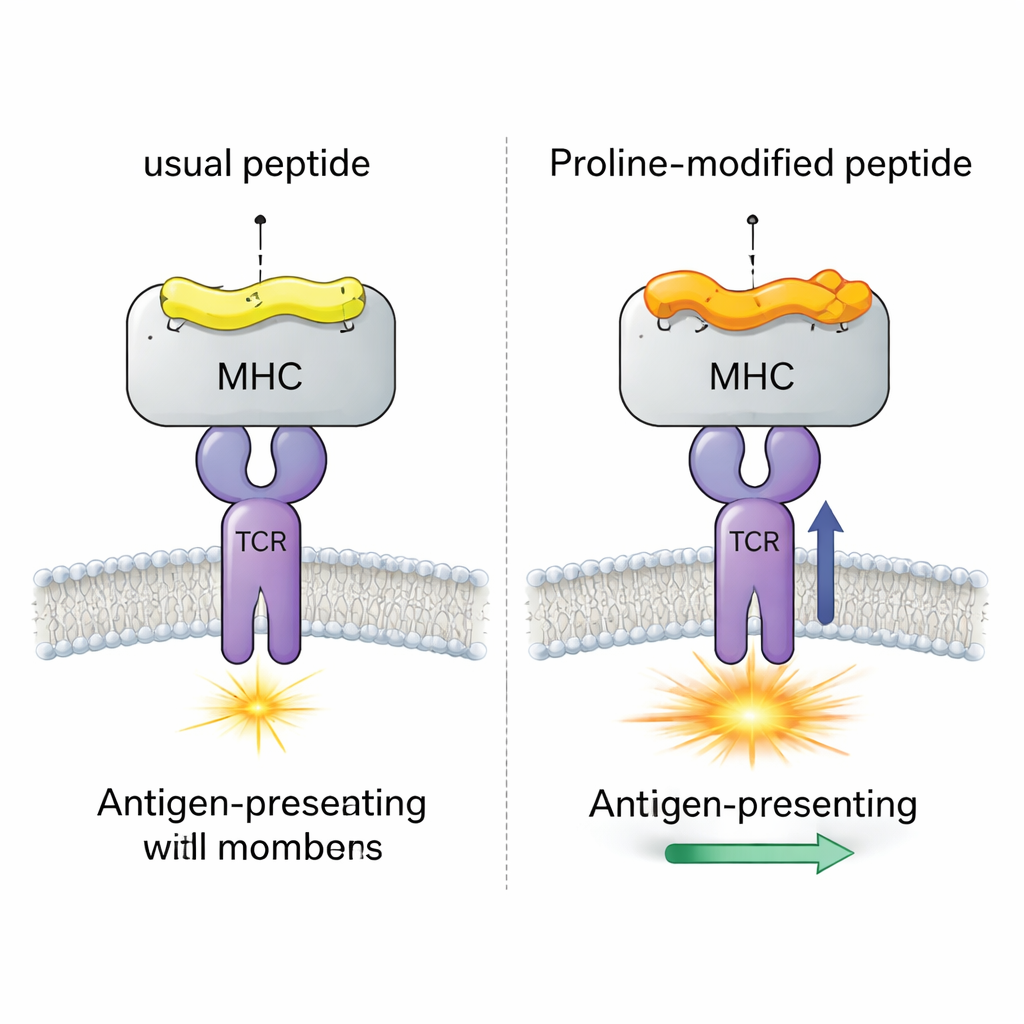
Dört Neredeyse Özdeş Peptitle Viral Bir Deneme
Araştırma ekibi, normalde güçlü CD8+ T hücre yanıtları tetikleyen gp33 adlı peptidi içeren iyi çalışılmış bir fare virüsü (LCMV) sistemine odaklandı. Aynı MHC molekülüne (H-2Db) bağlı, birbirine çok yakın dört peptit versiyonunu karşılaştırdılar. Bir versiyon orijinal viral peptittir; biri T hücrelerinin neredeyse tanımadığı bir bağışıklıktan kaçış mutasyonunu taşır; ve ikisi, peptidin başlangıcına yakın tek bir amino asidin proline olarak değiştirildiği “prolin-değiştirilmiş” aşı adaylarıdır. Önceki deneyler, bu prolin değişiminin peptit–MHC kompleksinin birleşme gücünü ve P14 adlı model TCR’nin yanıtını artırdığını göstermişti, ancak ayrıntılı mekanizma belirsiz kalmıştı.
Moleküllerin Titremesini İzlemek: Simülasyonlar ve Kristalografi
Olanı ortaya çıkarmak için yazarlar, her pMHC kompleksinin hareket halindeki uzun, atom-bazlı bilgisayar simülasyonlarını yüksek çözünürlüklü kristal yapılarla birleştirdiler. Her amino asit kalıntısının zaman içinde ne kadar salındığını ve peptidin üçüncü pozisyonu proline dönüştürüldüğünde bu salınımların nasıl değiştiğini incelediler. Birçok eşleştirilmiş simülasyon boyunca hareket desenlerini korelasyonlayarak, uzakta olsalar bile birlikte hareket eden kalıntıların bir “dinamik haritasını” kurdular. Ardından bu haritayı, her kalıntının bir düğüm ve kenarların istatistiksel olarak bağlantılı hareketleri temsil ettiği bir ağ haline getirdiler ve bu ağı sosyal ağ analizinde kullanılanlara benzer grafik teorisi araçlarıyla analiz ettiler.
Bağışıklık Kilidi İçinde Uzun Mesafeli İletişim
Ana bulgu, peptidin üçüncü kalıntısının prolina değiştirilmesinin yalnızca o yerel bölgeyi sertleştirmekten ibaret olmadığıdır. Bu değişiklik, peptit bağlama oluğunu sınırlayan MHC helikslerinden birine nasıl hareket iletildiğini değiştirir. Bu da TCR’nin izi altında yer alan ve tanıma için kritik olan altıncı peptit kalıntısının davranışını etkiler. “İyi” prolin-modifiye versiyonlarda bu kalıntı, TCR bağlanması için optimal olan konformasyonlar da dahil olmak üzere daha geniş bir konformasyon yelpazesini örnekler. Prolin içermeyen bağışıklıktan kaçış varyantında ise bu kalıntı daha kilitli durumda olup nadiren TCR-dostu yönelimi benimser. Ağ analizi, bu etkinin MHC oluğundaki belirli amino asitler aracılığıyla aktığını, prolin değişikliğinin yapıldığı yeri TCR temas bölgesine bağlayan dinamik olarak eşlenmiş bir kalıntı zinciri oluşturduğunu ortaya koyar.
Aşılar ve İmmünoterapi İçin Neden Önemli
Bu sonuçlar, immünojenezin—bir peptidin T hücrelerini ne kadar güçlü tetiklediğinin—sadece bir anda şekillerin uyup uymasıyla ilgili olmadığını, aynı zamanda kompleksin zaman içinde nasıl “nefes aldığı” ve esnediğiyle de bağlantılı olduğunu gösterir. Bir pozisyondaki ince bir değişiklik moleküler ağ boyunca dalga halinde yayılabilir ve anahtar temas kalıntılarının TCR ile uyumlu pozları benimseme olasılığını artırabilir. Yazarların hesaplamalı iş akışı, bu tür uzun menzilli eşleşmeleri sistematik olarak tespit etmenin bir yolunu sunar ve değiştirilmiş peptitlerin aşı ve kanser tedavisi tasarımına rehberlik edebilir. Basitçe söylemek gerekirse, bir peptidi nereye dokunacağımızı dikkatle seçerek, kilidin tamamını bağışıklık sisteminin anahtarı için daha “açılmaya hazır” bir dinamik duruma yönlendirebiliriz.
Atıf: Resink, T., Sala, B.M., Sun, R. et al. Dynamical network analysis reveals long-range residue couplings at the pMHC interface underlying enhanced immunogenicity. npj Syst Biol Appl 12, 15 (2026). https://doi.org/10.1038/s41540-026-00653-y
Anahtar kelimeler: T hücresi tanıması, peptit MHC, protein dinamikleri, değiştirilmiş peptit ligandları, immünojenezi